Перемещение пальца, культи пальца и пястной кости поврежденной кисти не получило широкого распространения в силу ряда обстоятельств [1]. Существенным сдерживающим фактором является высокая вероятность развития ишемических осложнений в случае использования рубцовоизмененных и деформированных сегментов в качестве донорских. Сосудистые расстройства приводят к частичным или полным некрозам кожных лоскутов и перемещенного сегмента в 11% случаев даже в условиях наличия малоизмененных или интактных тканей [2-4]. Эффективность применяемых способов профилактики таких осложнений нередко оказывается низкой, что служит причиной отказа от перемещения рубцовоизмененных комплексов. Вследствие этого данные операции выполняются лишь при некоторых типах дефектов кисти, сохранении пальцевых артерий и определенном состоянии мягких тканей, костного остова донорского сегмента [1; 5]. Специалисты отдают предпочтение увечному и технически более «удобному» для перемещения, чаще второму или смежному с восстанавливаемым, пальцу или его культе. Тем самым достигается уменьшение донорского изъяна, степени выраженности расстройств кровообращения трансформированного сегмента за счет меньшего травмирования сосудисто-нервных пучков и перемещенных кожных лоскутов [1; 5]. Однако существующие технологии не позволяют переместить короткие культи пальцев и пястных костей, расположенных на отдалении от реципиентной области, а также деформированные пальцы при повреждении магистральных сосудов и тяжелых нарушениях кровообращения тканей [5]. Указанные обстоятельства препятствуют более широкому применению метода, открывающего новые перспективы использования тканевых и функциональных резервов поврежденной кисти для реконструкции пальца, минимизации донорского ущерба и улучшения исходов операции. В связи с этим возникает необходимость в разработке новых подходов к расширению возможностей перемещения патологически измененных сегментов кисти и профилактике ишемических осложнений на сформированном пальце.
Цель исследования – расширить пределы применимости метода реконструкции пальцев кисти за счет перемещения ее сегментов, в том числе рубцовоизмененных и деформированных.
Материалы и методы. Проанализированы результаты лечения 184 больных, которым на 189 кистях выполнены первичная и вторичная реконструкция 203 пальцев методом перемещения различных сегментов травмированной кисти с применением традиционных (85 пальцев) и оригинальных (118 пальцев) способов. Чаще всего наблюдались механические повреждения кисти (101 – 54,9%). Кроме того, отмечались огнестрельные ранения (23 – 12,5%), последствия ожогов (27 – 14,7%), отморожение (30 − 16,3%) и комбинированная травма (3 – 1,6%). Правая кисть была повреждена у 80 больных (43,5%), левая – у 68 (37,0%), двусторонние культи пальцев и кисти имели место у 36 (19,6%) больных. Лиц мужского пола среди пострадавших было 161 человек (87,5%), женского – 23 (12,5%). Травму в быту получили 100 человек (54,3%), на производстве – 79 (42,9%), при несении военной службы – 5 (2,7%). Средний возраст пострадавших составил 28,18 ±3,74 года.
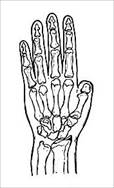
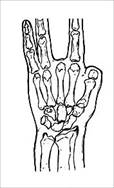
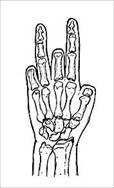
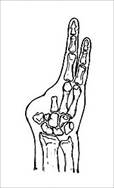
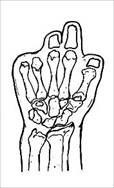
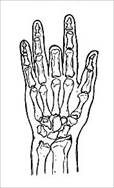
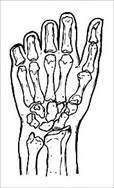
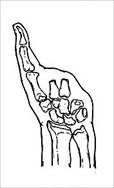
Анализ клинического материала позволил нам выделить следующие типы дефектов кисти, которые представлены на рис. 1.
|
|
|
|
|
|
|
Тип I (58 - 30,8%) |
Тип II (36 - 19,0%) |
Тип III (35 - 18,5%) |
Тип IV (1 - 0,5%) |
Тип V (47 - 24,9%) |
|
|
|
|
|
|
|
Тип VI (1 - 0,5%) |
Тип VII (3 - 1,6%) |
Тип VIII (1 - 0,5%) |
Тип IX (7 - 3,7%) |
Рис. 1. Типы дефектов кисти
Характер перемещаемых сегментов при различных типах дефектов и видах реконструкции представлен в таблице 1. Реконструкция большого пальца выполнена в 177 случаях, второго – 12, третьего – 5, четвертого – 8, пятого – в 1 случае. Восстановление одного пальца (чаще первого) реализовано в 186 случаях, первого и одного из трехфаланговых – 5, первого и двух трехфаланговых пальцев – 1, двух трехфаланговых пальцев – в 2 случаях.
Таблица 1
Характер перемещаемых сегментов при различных типах дефектов кисти и видах реконструкции
|
Характер перемещаемых сегментов |
Типы дефектов кисти |
Всего кистей: |
||||||||
|
I |
II |
III |
IV |
V |
VI |
VII |
VIII |
IX |
||
|
Первичная реконструкция: |
||||||||||
|
интактный палец |
8 |
8 |
||||||||
|
поврежденный палец |
3 |
2 |
1 |
1 |
7 |
|||||
|
перемещение сегмента после лоскутной пластики |
3 |
1 |
4 |
|||||||
|
Вторичная реконструкция: |
||||||||||
|
интактный палец типично |
18 |
18 |
||||||||
|
дефектный палец типично |
22 |
5 |
27 |
|||||||
|
культя пальца типично |
13 |
12 |
1 |
14 |
40 |
|||||
|
культя пястной кости типично |
2 |
4 |
11 |
1 |
18 |
|||||
|
дистрагированный палец |
3 |
3 |
||||||||
|
дистрагированная культя пальца* |
9 |
12 |
8 |
29 |
||||||
|
дистрагированная культя пястной кости* |
1 |
4 |
6 |
14 |
3 |
1 |
6 |
35 |
||
|
Всего кистей: |
58 |
36 |
35 |
1 |
47 |
1 |
3 |
1 |
7 |
189 |
*Перемещались одна и более культей или их частей в пределах одной кисти.
Уровни ампутации восстанавливаемого пальца представлены в таблице 2. Из таблицы также видно, что перемещение культей пальцев и пястных костей после дистракции применено при более дистальных уровнях ампутации восстанавливаемого пальца, чем при использовании типичных методик. Как правило, типично перемещали культю второго или смежного пальца, а после дистракции – ульнарно расположенные культи на проксимальных уровнях.
Таблица 2
Характер перемещаемых сегментов при различных уровнях культей восстанавливаемых пальцев
|
Уровни ампутации восстанавливаемого пальца |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
Всего пальцев |
|
Методы реконструкции пальцев |
|||||||||
|
Первичная реконструкция: |
|||||||||
|
перемещение интактного пальца |
3 |
5 |
8 |
||||||
|
перемещение дистальной части поврежденного пальца |
1 |
2 |
1 |
1 |
5 |
||||
|
перемещение культи пальца |
1 |
1 |
2 |
||||||
|
Перемещение сегмента после лоскутной пластики |
1 |
1 |
2 |
4 |
|||||
|
Вторичная реконструкция: |
|||||||||
|
перемещение интактного пальца |
4 |
10 |
3 |
1 |
18 |
||||
|
перемещение дефектного пальца |
1 |
1 |
8 |
7 |
1 |
2 |
7 |
27 |
|
|
перемещение культи пальца типично |
1 |
1 |
18 |
15 |
2 |
1 |
3 |
41 |
|
|
перемещение культи пястной кости типично |
3 |
7 |
4 |
1 |
2 |
17 |
|||
|
перемещение пальца после дистракции |
1 |
1 |
1 |
3 |
|||||
|
перемещение культи пальца после дистракции |
1 |
14 |
13 |
4 |
1 |
33 |
|||
|
перемещение культи пястной кости после дистракции |
13 |
20 |
9 |
3 |
45 |
||||
|
Всего пальцев: |
1 (0,5%) |
2 (1,0%) |
4 (1,9%) |
64 (31,5%) |
81 (39,9%) |
26 (12,8%) |
9 (4,4%) |
16 (7,9%) |
203 (100%) |
*Цифрами отмечены следующие уровни ампутации: 1 – средняя фаланга; 2 – дистальная треть основной фаланги; 3 – средняя треть основной фаланги; 4 – проксимальная треть основной фаланги; 5 – дистальная треть пястной кости; 6 – средняя треть пястной кости; 7 – проксимальная треть пястной кости; 8 - кости запястья.
В случае вторичной реконструкции выполнено перемещение сегментов первого (12 – 6,5%), второго (98 – 53,3%), третьего (46 – 25,0%), четвертого (26 – 14,1%), пятого (2 – 1,1%), а первичной – второго (14), третьего (2), четвертого (3) пальцев и их культей. Дистальный фрагмент культи первого луча подвергался только осевому перемещению в предварительно сформированный из кожного лоскута мягкий остов с целью реконструкции первого пальца. Подавляющее большинство донорских сегментов (дефектных пальцев, культей пальцев и пястных костей) имели рубцовые изменения мягких тканей различной степени выраженности (166 – 90,2%), глубины и протяженности поражения. Это усугубляло или обусловливало деформации сегментов, а также нарушения функции и кровоснабжения вследствие вторичных изменений сосудов или их повреждений, что значительно повышало вероятность развития ишемических осложнений. По этой причине сегменты перемещали по Хильгенфельдту-Шушкову [6] на постоянной ладонной сосудисто-нервной ножке, сформированной типично, содержащей полоску кожи шириной 1,5-2 см, служащей дополнительным источником питания и обеспечивающей лимфовенозный отток. Профилактику ишемических осложнений осуществляли также путем максимального сохранения или микрохирургического восстановления поврежденных ладонных пальцевых артерий, тыльных подкожных вен, формирования дополнительной тыльной питающей кожно-сосудистой или венозной ножки, а также хирургической тренировки (отсроченного перемещения) сегмента к ишемии. Такой подход применен в условиях вторичной реконструкции и рубцовых изменений тканей. Он состоял в остеотомии и мобилизации донорского сегмента на ладонной кожно-сосудистой питающей ножке с последующей фиксацией его к своему же месту в положении ротации, что создает умеренную ишемию вследствие сдавления сосудов ножки, контролируемую клиническими и инструментальными методами. В большинстве случаев в хирургическую тренировку сегмента включали его дистракцию с использованием аппарата Илизарова. Это обеспечивает дозированную ишемическую нагрузку на ткани и удлинение питающих ножек (тыльной и ладонной) на необходимую величину (а.с. № 1775883; пат. РФ №№ 2069545; 2093092; 2072807; 2152184; 2145812; 2120246; 2391930). Перемещение преформированного таким образом сегмента выполняется вторым этапом через 14-21 дней, а при проведении дистракции – после ее завершения. В зависимости от состояния кровообращения комплекса его перемещали на одной (ладонной) или двух (ладонной и тыльной) постоянных питающих ножках. Указанные операции были особенно оправданными в условиях выраженных рубцовых изменений мягких тканей, тяжелых деформаций сегментов, облитерации или повреждений сосудов, когда затруднительно или невозможно их выделение и применение прецизионной (микрососудистой) техники. На основании экспериментальных, морфологических, биофизических (тепловидение, лазерная доплеровская флоуметрия, реовазография) и статистических методов исследования разработан способ механической тренировки перемещаемого донорского пальца к ишемии [пат. РФ № 2566190]. Длительность тренировки составила 4-6 дней, при этом осуществлялось наложение артериального жгута на донорский палец 4 раза в день в течение 5 дней: в первый день длительность окклюзии составляет 10 минут, во второй – 15 минут, в третий день – 20 минут, в четвертый – 25 минут, с пятого – 30 минут. Критерием эффективности тренировки является разница значений прироста температуры дистального отдела пальца за 3 минуты после снятия жгута по сравнению с концом окклюзии между завершающей и первой ишемической нагрузкой не менее 1,7 оС, независимо от исходного состояния, времени тренировки и количества пережатий.
Результаты и обсуждение
Приживление всех сегментов, даже самых тяжело поврежденных, достигнуто при первичной реконструкции. После вторичной реконструкции отмечались некроз всей перемещенной культи пальца (1), частичный некроз ногтевой фаланги перемещенного дефектного пальца (1), частичный некроз мягких тканей на тыльной поверхности пальца (1), культи пальца (2). Во всех случаях ишемические осложнения различной степени тяжести, чаще венозного характера (34,3%), наблюдались при перемещении рубцовоизмененных и деформированных сегментов. Лишь в случае полного некроза сегмента (1 − 0,49%) функция схвата кисти не была восстановлена, а все другие осложнения были адекватно купированы и существенно не отразились на конечных результатах лечения. При использовании оригинальных подходов к перемещению и ишемической тренировке достигнуто приживление всех сегментов.
Эффективность лечения оценивали по усовершенствованной методике А.Е. Белоусова (1984). Отличные исходы получены в 41,6%, хорошие – 16,9%, удовлетворительные – 34,8%, неудовлетворительные – в 6,7% случаев. В случае первичного перемещения неудовлетворительных результатов не наблюдалось. Результаты перемещения дефектного пальца, культи пальца и пястной кости достоверно не отличались (Р>0,05). Проведен сравнительный анализ результатов традиционных и оригинальных методик. Сравниваемые группы достоверно не отличались по возрасту (Р=0,99), полу (Р=0,99), этиологии повреждения (Р=0,61-0,71) и типам дефектов кисти (Р=0,6-0,8). Выявлено, что применение оригинальных методик позволило переместить культи пальцев с более проксимальным уровнем ампутации (Р=0,02). Кроме того, использование дистракции сегмента дало возможность переместить культю пальца и пястной кости с наиболее ульнарным расположением (соответственно Р=0,01 и Р=0,0001). Дискриминационная чувствительность на восстановленном пальце после перемещения культи пальца составила 6,28±0,77 мм, пястной кости – 7,3±0,6 мм, а интактного пальца – 3,1±0,3 мм. Неудовлетворительные результаты были обусловлены наличием тотального дефекта первой пястной кости, а не характером, степенью деформации, нарушения кровообращения перемещаемого сегмента и изначального нарушения его функции. Функция схвата кисти и стабильность костного остова пальца, подтвержденные биомеханическими, рентгенометрическими и морфологическими исследованиями, достигнуты при многообразных дефектах кисти механической, огнестрельной и термической этиологии, в том числе в условиях обширных рубцов и нарушений магистрального кровообращения сегмента, с минимальным донорским изъяном.
Полученные нами функциональные результаты соизмеримы с известными из литературы [1], хотя показания к методу нами были значительно расширены за счет перемещения патологически измененных сегментов.
Приводим клинический пример.
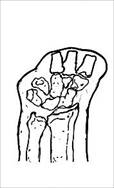
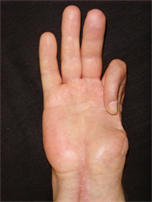
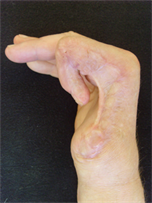
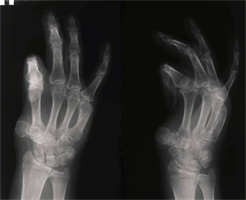
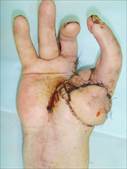
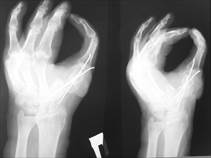
Мужчина, 42 лет, находился в клинике с диагнозом: тотальный дефект лучевого края правой кисти, сгибательные дермато-тено-артрогенные контрактуры 2, 3, 4 пальцев, дефект мягких тканей и костного остова, повреждение ладонных пальцевых артерий 2 пальца, разгибательная контрактура правой кисти после тяжелой механической травмы (рис. 2-4).
|
|
|
|
|
|
Рис. 2 |
Рис. 3 |
Рис. 4 |
Рис. 2. Внешний вид кисти больного до операции (ладонная поверхность)
Рис. 3. Внешний вид кисти до операции (латеральная поверхность)
Рис. 4. Рентгенограммы кисти до операции
Через 2 года и 5 месяцев после травмы выполнено одноэтапное перемещение в позицию первого наиболее дефектного второго пальца на ладонной и тыльной питающих ножках после устранения его деформации, пластики кожно-жировым лоскутом и тренировки к ишемии по разработанной методике.
Перемещенный сегмент и кожные лоскуты прижились полностью, раны зажили первичным натяжением, что позволило сформировать приемлемого вида большой палец и первый межпальцевой промежуток (рис. 5 и 6). Восстановлен схват кисти, несмотря на имевшуюся изначальную тяжелую деформацию, афункциональность донорского сегмента и, казалось бы, непригодность его для реконструкции (рис. 7).
|
|
|
|
||
|
Рис. 5 |
Рис. 6 |
Рис. 7 |
Рис. 5. Ближайший результат перемещения второго пальца
Рис. 6. Рентгенограммы кисти после операции
Рис. 7. Схват кисти через 1 год после перемещения пальца
Литературные данные и наш опыт свидетельствуют о применимости первичной артериальной или венозной реваскуляризации донорского сегмента лишь в условиях целостности сосудов, сохранения интактных тканей или отсутствия их грубых рубцовых изменений, когда вероятность возникновения и тяжесть ишемических осложнений не столь высоки [7-9]. Как следует из результатов проведенного исследования, гипоксическое прекондиционирование сегмента является эффективной мерой профилактики ишемических послеоперационных осложнений. Оно заключается в активации механизмов адаптации на различных уровнях системной организации тканей в результате короткого воздействия слабого, неповреждающего ишемического стимула. Дозируемая управляемая ишемическая нагрузка на ткани, достигаемая при хирургической тренировке перемещаемого комплекса, повышает их устойчивость к гипоксии, вызывает клеточную метаболическую адаптацию, продольную ориентацию сосудов питающей ножки и увеличение в них кровотока, что в итоге улучшает приживляемость тканей сегмента. Кроме того, достигается удлинение питающих ножек, что позволяет переместить отдаленно расположенную культю пястной кости необходимых размеров и любого трехфалангового пальца на проксимальных уровнях, в том числе на двух питающих ножках, через сохранившиеся пальцы или культи, и выполнить реконструкцию первого и/или одного из других пальцев с минимальным донорским изъяном [10].
Полученные результаты показали, что разработанные подходы позволяют расширить показания к перемещению сегментов кисти и получить адекватные функциональные результаты, в том числе при рубцовых деформациях крайне тяжелой степени.
Заключение
Использование ишемического прекондиционирования и преформирования рубцовоизмененных донорских сегментов обеспечило их 100% приживление и восстановление схвата у подавляющего большинства (93,3%) пострадавших с многообразными типами дефектов кисти механической, огнестрельной и термической этиологии.
Библиографическая ссылка
Александров Н.М., Киселев Д.В., Петров С.В. ВОССТАНОВЛЕНИЕ СХВАТА КИСТИ МЕТОДОМ ПЕРЕМЕЩЕНИЯ ПАЛЬЦЕВ, КУЛЬТЕЙ ПАЛЬЦЕВ И ПЯСТНЫХ КОСТЕЙ ПРИ ПОВРЕЖДЕНИЯХ И ИХ ПОСЛЕДСТВИЯХ // Современные проблемы науки и образования. 2018. № 4. ;URL: https://science-education.ru/en/article/view?id=27806 (дата обращения: 25.04.2026).
DOI: https://doi.org/10.17513/spno.27806