Scientific journal
Modern problems of science and education
ISSN 2070-7428
"Перечень" ВАК
ИФ РИНЦ = 0,936
MORPHOFUNCTIONAL ASPECTS OF GRANULE CELLS OF THE DISTRACTED CAPSULE OF FIBROANKYLOSED HAND JOINTS AND COLON MUCOSA IN PATIENTS WITH THE CROHN'S DISEASE
Исследование структурно-физиологического состояния соединительной ткани является одной из приоритетных задач биологии и медицины, имеющей важное значение при регенерации после повреждения [1-3]. Поэтому изучение регуляторных механизмов при регенераторном процессе повреждённых тканей представляется актуальным и в дальнейшем позволит, с одной стороны, спрогнозировать исход патологического процесса, с другой – оптимизировать лечение и своевременно проводить профилактику осложнений. С этих позиций особый интерес представляют тучные клетки (ТК), которые относятся к доминантным популяциям соединительной ткани и рассматриваются как «полифункциональные железы» с разнонаправленным действием, продуцирующие как компоненты экстрацеллюлярного матрикса (ЭЦМ) в виде протеогликана – необходимого компонента межклеточного вещества, так и широкий спектр биологически активных веществ (БАВ), оказывающих активное влияние на состояние микроциркуляции, клеточное окружение [4-6].
Тучные клетки являются долгоживущей популяцией с уникальной способностью в зависимости от микроокружения переключать свою функцию со структурообразовательной – синтез гепарансульфатного протеогликана в условиях адаптационной нормы на – провоспалительную с секрецией медиаторов разнонаправленного действия в условиях дисрегенерации, уровень относительной клеточной экспрессии которых обусловливает их биологическую целесообразность [7,8]. В формировании дальнейших трансформаций тучных клеток решающее значение имеет клеточное микроокружение. При этом изменения, возникающие в самих клеточных дифферонах, не являются генетически детерминированными. Дискутабельным остается вопрос об их стимулирующей либо ингибирующей роли в отношении развития регенераторного процесса, исходом которого и при болезни Крона (БК) и фиброзном анкилозе (ФА) является процесс фиброзообразования [9,10].
Необходимость сравнительного анализа структурных изменений слизистой оболочки толстого кишечника при различных формах течения болезни Крона и микроморфологии дистрагированной капсулы фиброзно-анкилозированных суставов не случаен. В первом случае хроническое иммуноопосредованное гранулематозное воспаление слизистой толстой кишки закономерно при благоприятном течении приводит к трансмуральному фиброзированию с локальным полным нарушением функции поражённого участка кишки, во втором случае – фиброзный анкилоз сустава является следствием разрушающего воздействия механических факторов на сустав – в итоге полное нарушение его функции. Структурным субстратом нарушения функции в обоих случаях является локальное развитие плотной соединительной ткани с некоторым сходством по характеру изменений регенераторного процесса при участии тучно-клеточной популяции и клеток фибробластического ряда, что показано в собственных работах и в исследованиях иностранных авторов [11,12].
Цель исследования: провести сравнительную морфофункциональную характеристику тучных клеток в условиях хронического воспалительного процесса при болезни Крона и в асептических условиях аппаратной дистракции капсулы фиброзноанкилозированных межфаланговых суставов кисти.
Материал и методы исследования: материалом исследования I группы пациентов служили 49 биоптатов слизистой оболочки (СО) толстой кишки 16 детей школьного возраста с разными фенотипическими вариантами БК в стадии клинической ремиссии (стенотическая (БКст) и свищевая форма (БКсв)), II группы – образцы мелких фрагментов капсулы проксимальных межфаланговых суставов (КПМФС) кисти у 11 пациентов после полученной механической травмы (7 женщин и 4 мужчин 30–60 лет). После предварительного препарирования стенки капсулы от коллатеральных связок интраоперационно по нейтральной линии с лучевой или локтевой стороны забирался фрагмент капсулы в количестве 1 кусочка. Образцы отбирали в момент установки (группа до дистракции – КПМФС) и через 2 месяца после снятия дистракционного аппарата (группа после дистракции – КПМФСд) из области ПМФС. Контролем I группы наблюдаемых послужили 12 детей того же возраста, поступившие в клинику с жалобами на боли в животе, для уточнения характера которых было выполнено эндоскопическое исследование с последующим морфологическим анализом, в результате которого была диагностирована слизистая оболочка без выраженных воспалительных изменений. В качестве контроля II группы послужили 6 аутопсийных образцов мелких фрагментов КПМФС кисти пациентов, скончавшихся от сердечно-сосудистых заболеваний.
После предварительной фиксации материала в растворе нейтрального формалина образцы ткани подвергались стандартной гистологической проводке (аппарате «Excelsior ES»), изготовлялись парафиновые блоки. Серийные срезы толщиной 4–6 микрон окрашивались гематоксилин-эозином. Параллельно проводилась количественная, качественная и функциональная оценка тучных клеток при помощи окраски по Гимзе, основным коричневым по М.Г. Шубичу с последующим выявлением и подсчётом тучных клеток, принимая во внимание их зрелость, степень дегрануляции и локализацию с нахождением в экстрацеллюлярном матриксе и периваскулярно. Морфометрический анализ микропрепаратов проводился в 10 полях зрения при увеличении 400, с последующей оценкой и анализом полученных данных методами непараметрической статистики. Для установления различий по исследуемым параметрам между независимыми группами был использован U-критерий Манна –Уитни, при сравнении двух зависимых групп Т-критерий Вилкоксона. Результаты представлены медианой (Ме) первой (25) и третьей (75) квартилями.
Результаты и их обсуждение
При морфологическом исследовании биоптатов СО толстой кишки детей как при благоприятном, так и неблагоприятном течении болезни Крона на стадии ремиссии в собственной пластинке СО отмечалось увеличение клеточной плотности инфильтрата в относительно количественных показателей нормы в 1,6 (р=0,004) и 2,4 (р=0,023) раза, соответственно.
Это происходит в основном за счет присутствия клеток лимфоцитарного ряда с наличием небольшого количества плазмоцитов и единичных эозинофильных гранулоцитов. При сравнении неосложненного (БКн) и осложненного течения БК наиболее высокая клеточная плотность инфильтрата отмечалась при формировании осложнений с неравномерным характером распределения клеточных элементов с появлением единичных клеток с агрессивным потенциалом – полиморфно-ядерных лейкоцитов, превышая значения в неосложненной группе в 1,5 раза (р=0,025). Так, при неосложнённой форме течения заболевания в собственной пластинке СО наблюдалось уменьшение общего количества тучных клеток относительно группы контроля в 1,2 раза (р=0,023), а в группе детей с осложнённой формой течения заболевания отмечался разнонаправленный характер их распределения (рис. 1).
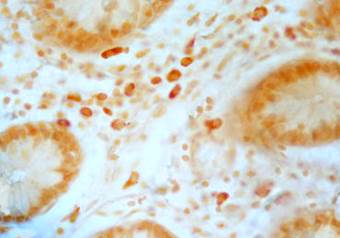
Рис. 1. Тучные клетки в слизистой оболочке толстой кишки при осложненной форме болезни Крона (окраска по Шубичу, ув. 1000)
В ранее опубликованных нами работах было отмечено, что повышенное содержание молодых фибробластов на фоне сниженного содержания зрелых форм в диффероне клеток фибробластического ряда способствует перестройки матричного геля, изменённый состав которого приводит к разрегулированности межтканевых и межклеточных взаимодействий в собственной пластинке СО. При анализе морфометрических данных внутри группы с осложненным течением отмечалась достоверная разница в 2,2 раза (р=0,000032) по количественному и качественному cоставу тучно-клеточной популяции между стенозирующей и свищевой формами – со снижением общего количества тучных клеток при развитии стенотической формы и увеличение их численности при формировании свищевой по сравнению с контролем.
Следует отметить нарастание удельного веса юных форм клеток вблизи сосудов микроциркуляторного русла и в прилегающих участках экстрацеллюлярного матрикса при обоих видах осложнений. Характерно отсутствие параэпителиально расположенных зрелых тучных клеток. Зрелые максимально дегранулированные клетки располагались преимущественно в экстрацеллюлярном матриксе (рис. 2, 3).
Вероятно, на фоне нарушения регуляции макрофагально-фибробластической активности тучные клетки вносят свой вклад не только в замедление репарации, но и способствуют пролонгации образования свищей при самом неблагоприятном течении воспалительного процесса.
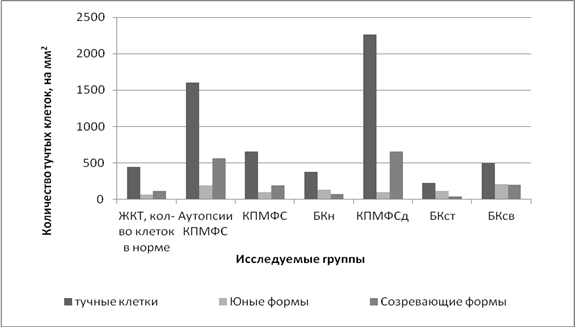
Рис. 2. Количество тучных клеток в экстрацеллюлярном матриксе
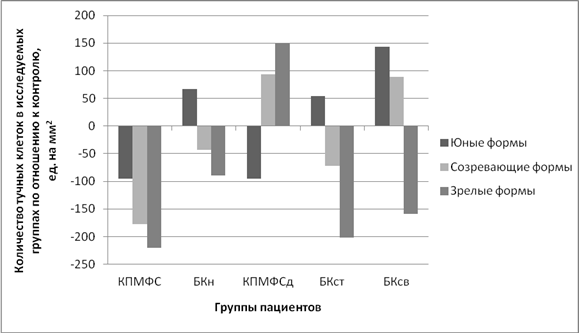
Рис. 3. Характеристика дифферона тучноклеточной популяции при различной патологии
Таким образом, тучные клетки оказывают регулирующее влияние на созревание соединительной ткани в зоне воспаления. Однако дискутабельным остается вопрос об их стимулирующей либо ингибирующей роли в отношении активности клеток макрофагально-фибробластического ряда.
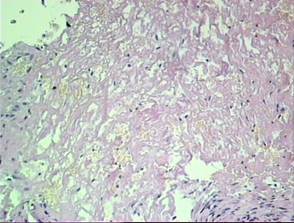
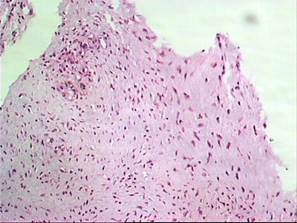
Гистологическая картина микропрепаратов недистрагированных тканей характеризовалась наличием участков неравномерно клеточной плотной волокнистой соединительной ткани с немногочисленными тучными клетками и редко расположенными мелкими сосудами (рис. 4). Общее количество клеточных элементов в дистрагированных тканях достоверно превышало их уровень, имевшийся до дистракции, в 1,35 раз (p=0,0179).
Известно, что фиброзирование суставов приводит к повышению количества тучных клеток. В капсуле фиброзноанкилозированного ПМФС пациентов до проведения дистракции тучные клетки визуализировались в количестве 4–7 в поле зрения, что в 2,7 раза было меньше, чем в исследованном контроле (р=0,0058), при этом большая часть из них представляла максимально и частично дегранулированные формы, которые определялись как периваскулярно, так и среди волокон (рис. 5).
|
|
|
|
а) До дистракции. Окраска гематоксилин-эозин, ув. Х200 |
б) После дистракции Окраска гематоксилин-эозин, ув. х200 |
Рис. 4. Ткань капсулы межфалангового сустава. Окраска гематоксилин-эозин, ув. Х200
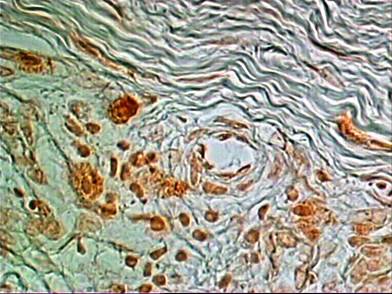
Рис. 5. Тучные клетки в ткани дистрагированной капсулы (окраска по Шубичу, ув. 1000)
После дистракции дифферон тучноклеточной популяции был представлен преимущественно зрелыми формами, количество которых увеличилось в 3,4 раза (p=0,0058). При этом повысилась доля дегранулированных форм ТК, превышая их уровень до дистракции в 6 раз (p=0,0033) и значения в контрольной группе в 2 раза (p=0,0007) и максимально дегранулированных форм ТК в 3 раза (p=0,0030) по сравнению с этапом до дистракции, превышая значения в группе контроля в 1,3 раза (p=0,0011) (рис. 2). В дистрагированных тканях обнаруживались единичные распадающиеся формы тучных клеток, представленные скоплением метаболических гранул.
Заключение
Известно, что более полный анализ тканей возможен с учетом дифферонной организации, когда клетки рассматриваются от инициального момента в развитии до этапа зрелости. Распределение внутри самого тучно-клеточного дифферона определяется процентным соотношением юных, созревающих и зрелых форм клеток. В условиях физиологической регенерации (нормы) оно представлено следующим соотношением: юные тучные клетки составляют не более 10,5 %, созревающие – 40,6 %, зрелые формы не менее – 48,9 %. При этом равномерное распределение тучных клеток в экстрацеллюлярном матриксе слизистой оболочки с преимущественным накоплением около базальной мембраны всех видов эпителия и включением их продуктов в ее состав характерно для стабилизации эпителиально-стромальных соотношений в собственной пластинке слизистой оболочки. Характер распределения (вблизи сосудов микроциркуляторного русла, или параэпителиально) тучных клеток с анализом учета их зрелости позволяет говорить о направленности изменений в этом клеточном диффероне при воспалительно-деструктивном процессе.
Специфика дифференцировки тучных клеток детерминирует их функции и гетерогенность субпопуляции. Такое уникальное свойство тучных клеток имеет двойственное значение, так как, с одной стороны, оно указывает на реализацию компенсаторно-приспособительных реакций при развитии патологического процесса, направленных на активацию механизмов регенерации, а с другой – свидетельствует о поддержании воспалительного процесса с сохранением синтеза протеолитических ферментов и биологически активных веществ, вызывающих дальнейшее повреждение ткани.
Регулирующее влияние лаброцитов на клетки-продуценты экстрацеллюлярного матрикса, в частности на функцию фибробластов с активацией в них биосинтетических процессов, направленных на фиброзообразование, выявлено в обоих случаях как вследствие перенесённого выраженного воспаления слизистой оболочки толстой кишки при болезни Крона, так и при повреждении мягких тканей суставов. В условиях отсутствия воспалительного процесса при ремиссии болезни Крона, когда ткань полностью освобождена от воспалительного инфильтрата, морфофункциональное состояние тучно-клеточной популяции проявляется уменьшением общего количества тучных клеток при стенотической форме, увеличением общего количества на фоне нарастания дегранулированных форм в группе пациентов с наличием свищей. Однако имеющееся сниженное количество тучных клеток в группе пациентов со стенотической формой, видимо, ориентировано на функцию по выделению компонентов экстрацеллюлярного матрикса и факторов, оказывающих влияние на рост и размножение клеток фибробластического ряда, что создаёт оптимальные условия для обеспечения структурного гомеостаза в целом и способствует дальнейшему восстановлению функции повреждённого органа. Напротив, в группе больных с наличием свищей при регенерации слизистой оболочки определяемое повышенное количество тучных клеток является негативным фактом, так как в этом случае характер их секрета несёт в себе провоспалительный потенциал с синтезом БАВ, что создаёт условия, несовместимые для адекватной дифференцировки клеток фибробластического ряда и макрофагального пула, что способствует дальнейшей дезинтеграции тканевых компонентов.
При изучении дифферона тучных клеток в дистрагированных тканях получены результаты, указывающие на то, что их выраженное увеличение происходит за счёт накопления зрелых клеток с нахождением распадающихся форм по сравнению с недистрагированными тканями, где наблюдалась редукция тучно-клеточной популяции. Высокая биологическая активность тучных клеток в этом случае направлена на активацию процессов регенерации, что, несомненно, приводило к улучшению функционального состояния ткани и восстановлению функции сустава.
Таким образом, при сравнении параметров регенерации дистрагированных тканей и СО толстой кишки на стадии клинической ремиссии детей с БК различного течения отмечалась одинаковая направленность регенераторного процесса, характеризующаяся тенденцией к росту. При этом необходимо отметить совпадение по всем показателям, включая тучно-клеточную популяцию СО толстой кишки с осложнённой формой заболевания с формированием свищей и дистрагированных тканей. Исходом завершения заболевания при дистракции ткани (с увеличенным содержанием тучных клеток) является фиброз, а при БК осложнённого течения с образованием свищей – воспаление с пролонгацией активности процесса.
Так, на стадии ремиссии при БК у больных с осложнённой формой в виде наличия стеноза в собственной пластинке СО толстой кишки и капсуле недистрагированных тканей наблюдается рассогласование внутридифферонных соотношений, проявляющееся изменением качественного и количественного состава клеток тучноклеточной популяции как элементов системы, продуцирующих компоненты экстрацеллюлярного матрикса. При этом одинаково уменьшается число зрелых и созревающих форм клеток при одновременном повышении числа юных форм. Максимально гранулированные формы зрелых клеток практически не определяются. Обращает на себя внимание тот факт, что все клеточные формы занимают в основном периваскулярное положение или равномерно распределены в матриксе. Формирование численного дефицита ТК может приводить к существенным структурно-функциональным изменениям внеклеточного матрикса соединительной ткани, деятельности мышечной оболочки и эпителиальной ткани слизистой оболочки кишки, оказывая определенное влияние на развитие адаптивного ремоделирования внеклеточного матрикса соединительной ткани.
Библиографическая ссылка
Широкова Н.Ю., Давыденко Д.В., Орлинская Н.Ю., Бугров С.Н., Шумилова О.В., Петров С.В., Новиков А.В. МОРФОФУНКЦИОНАЛЬНЫЕ ОСОБЕННОСТИ ТУЧНЫХ КЛЕТОК ДИСТРАГИРОВАННОЙ КАПСУЛЫ ФИБРОЗНОАНКИЛОЗИРОВАННЫХ СУСТАВОВ КИСТИ И СЛИЗИСТОЙ ОБОЛОЧКИ ТОЛСТОЙ КИШКИ У ПАЦИЕНТОВ С БОЛЕЗНЬЮ КРОНА // Современные проблемы науки и образования. 2017. № 5. ;URL: https://science-education.ru/en/article/view?id=26942 (дата обращения: 15.05.2026).