Scientific journal
Modern problems of science and education
ISSN 2070-7428
"Перечень" ВАК
ИФ РИНЦ = 0,936
TWO-STAGE SURGICAL TREATMENT OF THE PATIENT WITH THE NEUROFIBROMATOSIS OF 1 TYPE (CLINICAL OBSERVATION)
Нейрофиброматоз I типа (болезнь Реклингхаузена) является одним из наиболее часто встречающихся заболеваний из группы факоматозов [1; 2]. Частота встречаемости составляет 1 случай на 2500-7800 человек [3]. Данное заболевание обусловлено генетической природой – мутацией гена NF 1 в 17g хромосоме. Тип наследования заболевания – аутосомно-доминантный с пенетрантностью, близкой к 100%. Ген NF 1 в 17g хромосоме ответственен за продукцию белков, подавляющих опухолевый рост в организме человека. Однако в результате его мутации происходит сбой, и ген кодирует синтез крупного белка-нейрофибромина. В дальнейшем происходит дисбаланс роста клеток в сторону пролиферации [4], вместо подавления опухолевых клеток, последние остаются жить и развиваться, превращаясь в опухоль больших размеров. Как правило, данные опухоли доброкачественные, однако в 3-15% случаев имеют тенденцию к озлокачествлению, что обусловлено высокой частотой новых мутаций.
Впервые заболевание было описано немецким врачом Friedrich Daniel von Recklinghausen в 1882 г. Оно характеризуется широким диапазоном и вариабельностью клинических проявлений с вовлечением органов и систем, высоким риском осложнений, вплоть до летального исхода. С целью диагностики и последующего хирургического лечения, и улучшения результатов лечения данной патологии нередко требуется мультидисциплинарный подход.
Заболевание характеризуется множественными образованиями по ходу периферических нервов. При пальпаторном исследовании образования имеют округлую форму в виде узелков в толще кожи, варьирующихся по своим размерам и локализации [5; 6]. Данные нейрофибромы могут иметь болезненный или безболезненный характер. Видимые нейрофибромы чаще появляются в пре- и пубертатные периоды. До 30 лет отмечается интенсификация роста нейрофибром, особенно в период полового созревания или во время беременности. В дальнейшем их рост стабилизируется. Сама опухоль представлена округлой формой, различных размеров, доходящих до 7 см и более. При пальпаторном исследовании она не смещается продольно, а только в поперечном направлении вместе с нервным стволом, при этом могут возникнуть сильные боли в области иннервации того или иного нервного ствола или корешка.
Несмотря на то что нейрофибромы развиваются в образованиях периферической нервной системы, у части пациентов опухоли различной гистоструктуры, такие как глиомы зрительных нервов, эпендимомы, менингиомы, шванномы, могут расти и в отделах центральной нервной системы [5; 7].
Клиническая диагностика основывается на обнаружении диагностических критериев, опубликованных Национальным институтом здоровья США в 1987 году. Заболевание может быть подтверждено при наличии у больного по крайней мере двух из перечисленных ниже признаков:
- не менее 5 пятен цвета кофе с молоком, диаметром более 5 мм у детей препубертатного возраста и не менее шести таких пятен диаметром более 15 мм в постпубертатном периоде;
- две и более нейрофибромы любого типа или одна плексиформная нейрофиброма;
- множественные мелкие пигментные пятна типа веснушек, локализованные в крупных кожных складках (подмышечных или паховых);
- глиома зрительного нерва;
- два и более узелка Лиша (пигментированных гамартом на радужной оболочке), обнаруживаемых при исследовании с помощью щелевой лампы;
- костные аномалии (истончение кортикального слоя трубчатых костей, часто приводящее к формированию ложных суставов);
- наличие у родственников первой степени родства нейрофиброматоза I типа по вышеуказанным критериям [8].
До настоящего времени нет специфической терапии нейрофиброматоза. Квалифицированная медицинская помощь основана только на симптоматической терапии. При выраженном болевом синдроме проводят консервативную терапию, а при неэффективности проведения последней прибегают к хирургическим методам лечения. Лучевая и химиотерапия проводится в случаях озлокачествления опухоли [9; 10].
В данной работе рассматривается клинический случай периферической формы нейрофиброматоза I типа с поражением периферических нервов, образованием нейрофибромы мягких тканей лица, вызывающей грубый косметический дефект, и экстравертебральной опухолью С6 корешка спинномозгового нерва.
Пациент М., 29 лет, поступил весной 2017 г. в отделение нейрохирургии № 1 Новосибирского НИИТО им. Я.Л. Цивьяна с жалобами на сильные тянущие боли в левой руке, наиболее выраженные в II и III пальцах кисти, а также наличие большого объемного мягкотканного образования в лобной области справа, ежегодно увеличивающееся в объеме, и нависающее над правым глазным яблоком, а также наличием множества узелков на коже рук, туловища.
Анамнез заболевания: со слов пациента, больным считает себя с рождения. Родословная отягощена по отцовской линии – у отца нейрофиброматоз I типа (болезнь Реклингхаузена). С детства отмечает большое количество безболезненных образований узловой формы на коже рук, туловища. В возрасте 3 лет был оперирован по поводу новообразования в лобной области справа, проведено удаление опухоли (гистологическое заключение не предоставил). В 2015 г. стала беспокоить боль в шейном отделе позвоночника и в левой руке, после проведенного обследования МРТ шейного отдела позвоночника было выявлено объемное образование на уровне С6-С7 позвонков слева. В период с 21.01.16 г. по 05.02.16 г. проходил лечение в больнице по месту жительства, где было выполнено оперативное лечение: ламинэктомия на уровне C6-C7 позвонков, удаление гистологически подтвержденной нейрофибромы на уровне C6-C7 слева. Через полгода был выполнен послеоперационный контроль МРТ шейного отдела позвоночника и диагностирован продолженный рост новообразования. В связи с низкой чувствительностью нейрофибромы к лучевой терапии онкологом рекомендовано проведение повторного оперативного лечения.
В неврологическом статусе со стороны черепно-мозговых нервов нарушений не выявлено. Сила в конечностях составляла 5 баллов. При обследовании выявлена также корешковая симптоматика в виде выраженных болей по дорсальной поверхности левого предплечья с иррадиацией к II и III пальцам. Субъективно нарушений чувствительности выявлено не было.
Локальный статус: по задней поверхности шеи в проекции остистых отростков С3-Th1 позвонков визуализирован послеоперационный кожный рубец бледно-розового цвета без признаков воспаления. На теле при пальпаторном обследовании подкожно определяются множественные округлые образования различного размера и плотности. При надавливании паравертебрально на уровне С6-C7 позвонков слева определяется резкая болезненность с иррадиацией в руку.
В лобной области справа имелось образование мягко-эластической консистенции, безболезненное при пальпации, напоминающая «гроздь винограда» (рис. 1).
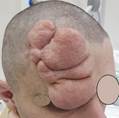
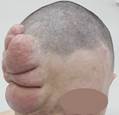
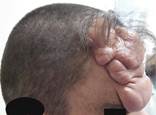
Рис. 1. Фотография больного до операции
В общеклинических анализах крови, мочи, биохимическом исследовании крови патологических изменений не обнаружено.
По данным МРТ головы (рис. 2), до операции в правой лобной области определяется экстракраниальное объемное образование, растущее из мягких тканей размером 7,03х2,85х1,13 см.
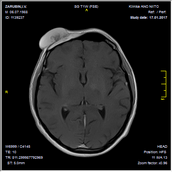
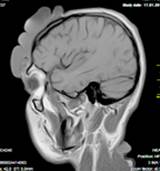
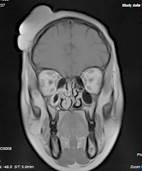
Рис. 2. МРТ головы больного с контрастированием перед операцией.
В лобной области справа определяется мягкотканное образование
По данным МРТ шейного отдела позвоночника (рис. 3), в левом межпозвонковом отверстии на уровне C6-С7 позвонков с экстрафораминальным распространением определяется контрастируемое объемное образование размером 2,45х1,95х2,65 см.
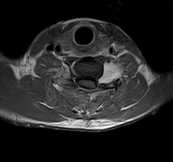
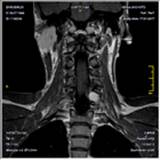
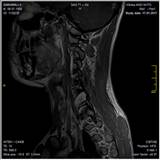
Рис. 3. МРТ шейного отдела позвоночника больного с контрастированием до операции. На уровне С6-С7 позвонков слева определяется новообразование, накапливающее контраст
После проведенного клинико-неврологического обследования, а также учитывая данные МРТ шейного отдела позвоночника и головы, было принято решение выполнить хирургическое лечение в два этапа. Первым этапом решено удалить образование на уровне С6-С7 спинномозгового корешка слева. Вторым этапом, совместно с пластическими хирургами, выполнить удаление объемного образования мягких тканей в лобной области справа с последующей пластикой обширного дефекта, образовавшегося после резецированния опухоли в пределах мягких тканей, перемещенным или свободным лоскутом.
19.01.2017 г. пациенту проведен запланированный первый этап хирургического вмешательства: частичная резекция суставной пары C6-C7 позвонков, верхнего края полудужки С7 позвонка, микрохирургическое удаление объемного образования на уровне С6-С7 позвонков слева с интрафораминальным распространением под нейрофизиологическим мониторингом.
Интраоперационно: под резецированным суставом обнаружено эластичное объемное образование серо-бледного цвета, плотной консистенции, имеющее выраженную капсулу, плотно спаянную с окружающими тканями, твердой мозговой оболочкой, визуально напоминающее нейрофиброму. Под увеличением х10-х12 с использованием микрохирургического инструментария выполнено поэтапное выделение и удаление опухоли. В ходе ее удаления обнаружено, что ткань распространяется в позвоночный канал, прилежит к дуральному мешку слева, но не компримирует его. Капсула передних отделов опухоли рыхло спаяна с позвоночной артерией, последняя отделена от патологической ткани, при этом ее целостность не нарушена. Опухоль выделена, отсечена от корешка в дистальных его отделах и удалена тотально.
Послеоперационный период протекал спокойно. В неврологическом статусе отмечена положительная динамика в виде уменьшения тянущих болей в левой руке. На послеоперационной МРТ шейного отдела с контрастированием, выполненной на 9-е сутки, подтверждено тотальное удаление опухоли (рис. 4).
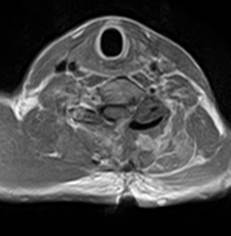
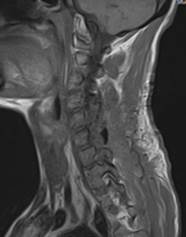
Рис. 4. МРТ шейного отдела позвоночника больного после операции.
Признаков опухоли нет
Спустя 12 дней, 02.02.2017 г., совместно с пластическими хирургами выполнен второй этап хирургического вмешательства, направленный на микрохирургическую резекцию опухоли в лобной области справа и комбинированную пластику дефекта мягких тканей ротационным лоскутом и полнослойным трансплантатом с передней брюшной стенки.
Интраоперационно: после удаления мягкотканного компонента опухоли образовался дефект кожи 12,0х8,0 см (площадь дефекта 96 см2). Затем выкроен «языкообразный» лоскут в левой лобной, височной и частично в затылочных областях. Лоскут отсепарован от надкостницы и перемещен на область дефекта, где был фиксирован единичными узловыми швами. В правой надбровной области частично ушит образовавшийся дефект мягких тканей. По форме оставшегося дефекта реципиентной зоны изготовлен шаблон. По нему на передней брюшной стенке в гипогастральной области проведен забор кожного трансплантата, последний помещен в место оставшегося дефекта кожи и пришит к краям кожи послойно. Питание ротационного лоскута не было нарушено, на полнослойный трансплантат наложена давящая повязка (рис. 5).
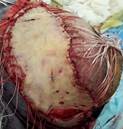
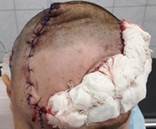
Рис. 5. Интраоперационные фотографии больного. Фиксированный узловыми швами кожный трансплантат с последующим наложением давящей повязки
Послеоперационный период протекал на фоне удовлетворительного состояния без осложнений. Давящая повязка с лоскута снята на 10-е сутки. Пациент выписан на 11-е сутки после выполнения второго этапа операции. Заживление раны первичным натяжением изображено на рисунке 6. Состояние кожного трансплантата и перемещенного лоскута через 6 месяцев показано на рисунке 7.
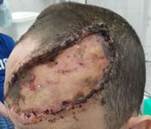
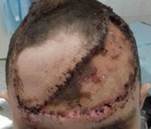
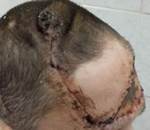
Рис. 6. Перемещенный лоскут и кожный трансплантат на 11-е сутки после второго этапа хирургического лечения
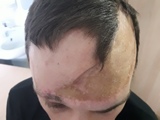
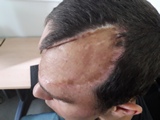
Рис. 7. Фотография пациента через 6 месяцев после хирургического лечения.
Алопеция по всей площади кожного трансплантата
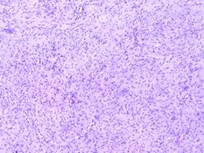
Гистологическое исследование материала: материал объемного образования, полученный после первого этапа хирургического вмешательства, представлен опухолевой тканью солидно-ретикулярного строения, образованной вытянутыми веретеноподобными клетками с палочковидными и округлыми ядрами. Между опухолевыми клетками выраженная миксоидная коллагенизированная соединительнотканная строма, большое количество разнокалиберных сосудов, слабо выраженная диффузная лимфоидная инфильтрация (рис. 8А).
Материал, полученный в результате второго этапа хирургического лечения, представлен микроскопически фрагментами кожи с эпидермисом и подлежащей дермой с придатками кожи. В дерме определяется рост опухоли солидно-ретикулярного строения, образованной пучками вытянутых шванновских клеток с волнистыми ядрами и плотным хроматином в них. Между опухолевыми клетками выраженная миксоидная коллагенизированная соединительнотканная строма, большое количество разнокалиберных сосудов, слабо выраженная диффузно-очаговая лимфоидная инфильтрация. Встречается большое количество замурованных в ткани опухоли дистрофически измененных нервных стволиков (рис. 8Б).
 А
А 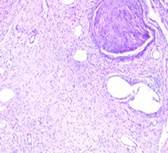 Б
Б
Рис. 8. А (после первой операции), Б (после второй операции).
Морфологическая картина соответствует нейрофиброме, Grade 1.
Окраска гематоксилином и эозином. Увеличение х100
Представленный клинический случай, безусловно, относится к нейрофиброматозу I типа (периферическая форма), что подтверждает врожденная наследственность (у отца имелось аналогичное заболевание), ярко выраженные признаки данной патологии и патоморфологическое исследование новообразований. Использование современной микрохирургической техники, мультидисциплинарный подход в содружестве с пластическими хирургами позволили достигнуть не только хорошего клинического (в виде тотального удаления нейрофибром указанных локаций), но и косметического результата.
Библиографическая ссылка
Васильев И.А., Ступак В.В., Пендюрин И.В., Копылов И.С., Цегельников М.М., Селякова М.С. ДВУХЭТАПНОЕ ХИРУРГИЧЕСКОЕ ЛЕЧЕНИЕ ПАЦИЕНТА С НЕЙРОФИБРОМАТОЗОМ I ТИПА (КЛИНИЧЕСКОЕ НАБЛЮДЕНИЕ) // Современные проблемы науки и образования. 2017. № 5. ;URL: https://science-education.ru/en/article/view?id=26818 (дата обращения: 15.05.2026).



