Scientific journal
Modern problems of science and education
ISSN 2070-7428
"Перечень" ВАК
ИФ РИНЦ = 0,936
LOCKING INTRAMEDULLARY OSTEOSYNTHESIS IN TREATMENT OF FEMUR FRACTURE CONSEQUENCES
Актуальность исследования базируется на довольно большой частоте переломов бедренной кости от 8 до 16 % травм костей скелета [1]. Следует отметить, что в 60 % случаях перелом локализуется в средней трети диафиза [2]. Реабилитация пациентов с данными повреждениями остается сложной задачей. В нашей стране на долю переломов бедренной кости как причины первичной инвалидности населения приходится 13–15 % случаев от общего числа стойкой утраты трудоспособности вследствие травм опорно-двигательного аппарата [3].
В результате применения современных методик остеосинтеза при лечении пациентов с повреждениями диафиза бедренной кости частота формирования псевдоартрозов как осложнений достигает по данным разных авторов 12 % [4, 5]. Одной из таких методик является блокируемый интрамедуллярный остеосинтез (БИОС), зарекомендовавший себя как надежная технология в лечении данной категории пациентов. Он позволяет достигать необходимой первичной стабильности костных отломков при практически любой локализации и сложности перелома непосредственно после операции, и в последующем осуществлять раннюю мобилизацию поврежденной конечности и пациента.
БИОС с поперечным блокированием и обязательным рассверливанием костномозгового канала также зарекомендовал себя при лечении последствий переломов бедренной кости. По данным ряда авторов такой подход к лечению несросшихся переломов и ложных суставов бедренной кости является предпочтительным и позволяет достичь консолидации в большинстве случаев, а доля несращения составляет до 15 % [5, 6]. Настораживает сопоставимая частота несращения бедренной кости при применении одинаковой методики остеосинтеза у пациентов со свежим переломом и его последствиями. При острых переломах, шинированых стандартным интрамедуллярным стержнем с поперечным блокированием, консолидация протекает по пути вторичного заживления костных отломков, что вполне приемлемо и достаточно. Напротив, для нормализации нарушенных процессов репарации у пациентов с несросшимися переломами и ложными суставами бедренной кости необходимо создавать условия для физиологической аутокомпрессии.
Цель исследования – установление причин и частоты возникающих осложнений после БИОС у пациентов с последствиями переломов бедренной кости.
Материалы и методы исследования, технологии остеосинтеза. Работа включала ретроспективный сравнительный анализ 89 случаев лечения больных с последствиями перелома бедренной кости, которым выполнялся блокируемый интрамедуллярный остеосинтез в травматолого-ортопедическом отделении №1 ФГБУ «СарНИИТО» МЗ РФ г. Саратов с января 2009 по февраль 2015 г. Пациенты включены в исследование сплошным методом. Средний срок наблюдения составил 22±8 месяцев (размах значений – от 10 до 49 месяцев).
В подавляющем большинстве случаев (83 пациента, 93,6 %) имел место прямой механизм травмы: в результате дорожно-транспортных происшествий – 62 (74,7 %) пациента с переломами диафиза бедренной кости; падения с высоты –15 (18,1 %) и спортивная травма – 6 (7,2 %); непрямой – 6 (6,4 %) случаев. По полу пациенты распределены соответственно: мужчины – 58 (65,2 %), женщины– 31 (34,8 %). Возраст пациентов – от 18 до 65 лет, средний возраст составил 36,1±15,1 года.
Всех пациентов, исходя из характера последствий и выбранной первоначально методики оперативного лечения, можно разделить на две группы. Первую группу составил 51 больной (57,3 %) с несросшимися переломами и ложными суставами диафиза бедренной кости после накостного металлоостеосинтеза. Во вторую группу вошли 38 пациентов (42,7 %), которым ранее выполнялся интрамедуллярный остеосинтез. Примеры рентгенограмм пациентов первой и второй групп с последствиями переломов средней трети бедренной кости представлены на рисунке.

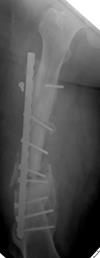
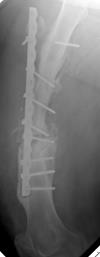

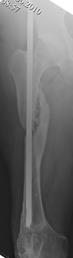
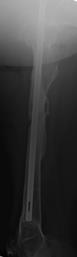
Рентгенограммы бедра пациентов первой (А) и второй (Б) групп в переднезадней и боковой проекциях
Исходя из классификации псевдоартрозов Weber& Cech [7], основанной на регенераторных процессах в зоне повреждения, у пациентов были диагностированы ложные суставы как с сохраненной васкуляризацией концов фрагментов бедренной кости –«жизнеспособные» (viabletypes), так и с признаками гипопластического костеобразования –«нежизнеспособные» псевдоартрозы (non-viabletypes).
Чаще других у пациентов встречались «жизнеспособные» псевдоартрозы, на их долю пришлось 67,4 % (60 больных) наблюдений, на долю «нежизнеспособных» ложных суставов – 11,2 % (10 больных). Количество несрасщённых переломов составило 21,6 % в первой и 21,1 % во второй группе (табл. 1).
Таблица 1
Распределение пациентов в группах в зависимости от характера последствий
|
Последствия |
I группа (n=51) |
II группа (n=38) |
Всего (n=89) |
|||
|
Абс. |
%% |
Абс. |
%% |
Абс. |
%% |
|
|
«Жизнеспособный» ложный сустав |
34 |
66,7 |
26 |
68,4 |
60 |
67,4 |
|
«Нежизнеспособный» ложный сустав |
6 |
11,7 |
4 |
10,5 |
10 |
11,2 |
|
Несрасщенный перелом |
11 |
21,6 |
8 |
21,1 |
19 |
21,4 |
В первой группе в ходе предшествующего оперативного вмешательства в 23 (45,1 %) случаях были установлены простые нейтрализующие пластины, DCP (Dynamic compression plate) применялись в 17 (33,3 %) случаях, а в остальных – 11(21,5 %) остеосинтез выполнялся при помощи технологии LCP (Locking compression plate). Во второй группе, в 20 случаях (52,6 %) были установлены неблокируемые интрамедуллярные стержни различной модификации, а у 18 (47,4 %) пациентов стержни с блокированием в дистальном и проксимальном отделах.
Для подбора типа и размера фиксатора проводили объективное обследование пациента с измерением длины здоровой и поврежденной конечностей. Затем по рентгеновским снимкам выполняли более точные измерения длины бедренной кости и ширины костно-мозгового канала на уровне анатомического сужения при сохранности последнего. В ходе оперативного вмешательства применяли универсальный (круглого сечения, с поперечным блокированием дистальной и проксимальной частей) интрамедуллярный стержень различных производителей.
На первом этапе оперативного вмешательства из разрезов кожи по старым послеоперационным рубцам осуществляли удаление ранее установленной металлоконструкции, после чего у пациентов первой группы осуществляли полноценную ревизию зоны повреждения. В ходе нее выполняли удаление нежизнеспособных костных отломков, интерпозита, представленного фиброзной тканью, осуществляли вскрытие костномозговых каналов с обязательным удалением замыкательной пластинки по всему периметру торцевой части отломков. Выполняли минимальную краевую резекцию концов отломков. У пациентов второй группы проводили аналогичные манипуляции за исключением необходимости формирования костно-мозгового канала. Затем в интрамедуллярный канал заводился проводник, по которому осуществлялось рассверливание гибкими риммерами с шагом в 1 мм до достижения запланированного диаметра, у пациентов второй группы он был на 2 мм больше ранее установленного стержня. Суть манипуляций заключалась в превращении псевдоартроза в свежий перелом, что способствует стимуляции процессов регенерации костной ткани.
В зависимости от применяемого интрамедуллярного стержня осуществляли его блокирование при помощи целенаправителей или электромагнитной навигации. При наличии плотного торцевого упора и «жизнеспособного» псевдоартроза применяли первично динамический или компрессионный вариант установки. Во всех остальных случаях выполняли статическую фиксацию с последующей обязательной динамизацией в сроке от 2-х до 3-х месяцев. Для контроля заживления костной раны у пациентов использовали клинические и инструментальные методы исследования (рентгенография, МРТ, КТ). Исходы лечения оценивались по системе СОИ-1 [8], включающей 16 параметров и анкеты Освестри.
Результаты исследования и обсуждение. При анализе исходов предыдущего лечения в большинстве случаев не всегда возможно установить основные причины (несращение кости, последующий перелом и миграция металлоконструкции или несостоятельный остеосинтез), повлекшие за собой неудовлетворительный результат. Однако мы можем выделить основные из них: металлоостеосинтез – применение устаревших конструкций, неправильно подобранная металлоконструкция, недостаточная репозиция, нарушение технологии проведения оперативного вмешательства; некорректная лечебная тактика в послеоперационном периоде – проведение реабилитации, несоответствующей применяемой технологии лечения.
Ближайшие результаты оперативного лечения удалось оценить у 87 (97,6 %) пациентов обеих групп (табл. 2).
Таблица 2
Осложнения блокируемого интрамедуллярного остеосинтеза в ходе лечения пациентов с последствиями перелома бедренной кости*
|
Вид осложнения |
Первая группа (n=51) |
Вторая группа (n=38) |
|
СПЕЦИФИЧЕСКИЕ |
||
|
перелом стержня |
2 (3,9 %) |
2 (5,3 %) |
|
перелом винтов |
8 (15,7 %) |
4 (10,5 %) |
|
миграция стержня |
1(1,9 %) |
- |
|
миграция винтов |
13 (25,5 %) |
10 (26,3 %) |
|
НЕСПЕЦИФИЧЕСКИЕ |
||
|
Нагноение |
8 (15,7 %) |
4 (10,5 %) |
|
Остеомиелит |
2 (3,9 %) |
- |
|
Флеботромбоз |
8 (15,7 %) |
7 (18,4 %) |
|
Несращение |
21 (41,7 %) |
11 (28,6 %) |
|
Контрактура |
2 (3,9 %) |
- |
|
Укорочение конечности |
4 (7,8 %) |
2 (5,3 %) |
*Сумма значений может превышать 100 % по причине сочетания нескольких осложнений у одного пациента.
В первой группе пациентов после накостного металлоостеoсинтеза положительные результаты лечения получены у 39 пациентов (76,5 %), из них: отличные – у 3 пациентов (5,9 %), хорошие – в 14 случаях (27,5 %), удовлетворительные – в 12 случаях (23,5 %); неудовлетворительные – у 12 пациентов (23,5 %). Неудовлетворительные результаты оперативного вмешательства заключались в глубоком нагноении, которое впоследствии привело к развитию хронического остеомиелита в 2 (3,9 %) случаях. Потеря опороспособности конечности после перелома интрамедуллярного фиксатора по линии несращенного перелома наблюдали у 2 (3,9 %) пациентов. Значимая миграция металлоконструкции при ретроградной установке стержня у пациента с выраженным остеопорозом выявлена у 1 (2 %) больного. Укорочение конечности более 3 см по результатам лечения было выявлено в 3 (5,9 %) случаях. В 4 (7,8 %) наблюдениях боль в области несращенного перелома приводила к значимым снижениям функциональной пригодности конечности, что и стало причиной неудовлетворительного исхода оперативного вмешательства. Среднее значение по результатам анкеты Освестри через 2 месяца после оперативного вмешательства составило 33,7±4,2 балла, через 6 месяцев-39±5,1 и по итогам всего периода лечения 43,2±5,3 балла. В ближайшем послеоперационном периоде средний процент реабилитации по СОИ-1 составил 73,6±4,5 %, через 6 месяцев с момента оперативного вмешательства – 78,3±4,8 % и к 12 месяцем – 79,4±13,2 %.
Во второй группе пациентов после первично выполненного интрамедуллярного остеосинтеза положительные результаты лечения получены у 31 пациента (81,6 %), в том числе отличные у 4 пациентов (10,5 %), хорошие – у 15 (39,5 %), удовлетворительные – у 12 (31,6 %); неудовлетворительные – у 7 пациентов (18,4 %). В 1 (2,6 %) случае неудовлетворительный результат оперативного вмешательства возник по причине глубокого нагноения послеоперационной раны, которое потребовало дополнительного оперативного вмешательства, направленного на купирование воспалительного процесса. Укорочение конечности более 5 см по результатам лечения было выявлено в 2 (5,3 %) случаях. В 2 (5,3 %) наблюдениях причиной значимого снижения опороспособности оперированной конечности стал перелом интрамедуллярного стержня по линии несращения. В 2 (5,3 %) наблюдениях боль в области несращенного перелома приводила к резкому снижению функции конечности, что и стало причиной неудовлетворительного исхода оперативного вмешательства. Среднее значение по результатам анкеты Освестри через 2 месяца после оперативного вмешательства составило 36,2±4,8 балла, через 6 месяцев – 42,4±6 и по итогам всего периода лечения – 44,6±7,6 балла. В ближайшем послеоперационном периоде средний процент реабилитации по СОИ-1 составил 75,6±5,2 %, через 6 месяцев с момента оперативного вмешательства – 81,9±9 % и к 12 месяцем – 86,2±7,8 %.
Основные причины неудач, по нашему мнению, заключаются в нарушении процессов остеорегенерации в зоне повреждения за счет длительного функционирования системы «кость-имплантат» в условиях шунтирования нагрузок посредством статических стержней [9]. Несвоевременная или зачастую невыполненная динамизация металлоконструкции только способствует продолжению шинирования сегмента и выключению его из циклических нагрузок, так необходимых для консолидации [10].
Заключение. Анализ исходов лечения 89 пациентов с несросшимися переломами и ложными суставами бедренной кости после реостеосинтеза БИОС выявил значительный объем осложнений после удаления ранее установленных интрамедуллярных стержней и пластин. Замена внутрикостного фиксатора с одного доступа и рассверливание канала приводит в 28,6 % к несращению. Объемные оперативные вмешательства, в ходе которых выполняется удаление пластин с последующей обработкой и открытой адаптацией концов отломков, не приносят успеха в 41,7 % случаев. Таким образом, для профилактики неблагоприятных исходов оперативного вмешательства необходимо менять идеологию остеосинтеза, где интрамедуллярный стержень за счёт своих конструктивных особенностей позволит достигать баланса жесткой фиксации отломков и аутокомпрессии. На начальных этапах после оперативного вмешательства конструкция работает как остов, на котором посредством мышечной аутокомпрессии, а затем и осевой нагрузки на конечность стимулируются процессы регенерации костной ткани в зоне повреждения.
Библиографическая ссылка
Зуев П.П., Барабаш А.П., Барабаш Ю.А. БЛОКИРУЕМЫЙ ИНТРАМЕДУЛЛЯРНЫЙ ОСТЕОСИНТЕЗ ПРИ ЛЕЧЕНИИ ПОСЛЕДСТВИЙ ПЕРЕЛОМОВ БЕДРЕННОЙ КОСТИ // Современные проблемы науки и образования. 2017. № 5. ;URL: https://science-education.ru/en/article/view?id=26736 (дата обращения: 29.04.2026).



