Scientific journal
Modern problems of science and education
ISSN 2070-7428
"Перечень" ВАК
ИФ РИНЦ = 0,936
ANALYSIS OF CHANGE OFADAPTATIVE REACTIONS IN THE TREATMENT OF CERVICAL CANCERWITH EXTRACORPOREAL DETOXIFICATION METHODS AND NONSPECIFIC IMMUNOTHERAPY
Рак шейки матки (РШМ) продолжает оставаться наиболее частой злокачественной опухолью женских половых органов. В последние годы отмечена негативная тенденция за счет роста заболеваемости у женщин молодого возраста с ежегодным приростом на 2–7 % [2, 9].
Во многих онкологических клиниках инициальным лечением местно-распространенных форм рака шейки матки (МРРШМ) являются неоадъювантная химиотерапия (НАХТ) или химиолучевое лечение [12]. Однако стандартное внутривенное введение химиопрепаратов далеко не всегда позволяет перевести опухоль в резектабельное состояние и выполнить стандартное радикальное хирургическое вмешательство из-за формирования резистентности опухоли к цитостатикам [5,6].
Экстракорпоральные методы детоксикации, в частности, плазмаферез, может повысить эффективность цитостатической терапии за счет деблокирования рецепторного аппарата клетки и уменьшения резистентности к химиопрепаратам, неизбежно развивающейся в процессе любого лечения, особенно в условиях опухолевой интоксикации [11]. В исследованиях Г.А. Неродо, проведенных в Ростовском научно-исследовательском онкологическом институте, показано, что проведение сеанса плазмафереза перед неоадъювантной химиотерапией у больных асцитными формами рака яичников способствует оптимизации состояния общей реактивности организма, обеспечивая компенсацию эндогенной интоксикации и позволяя сохранять дозовую интенсивность химиотерапии у больных с высоким риском развития осложнений [7,8,10].
Вирус папилломы человека является обязательным этиологическим фактором рака шейки матки. При этом известно, что в случае развития рака шейки матки иммунный статус организма позволяет персистирующей папилломовирусной инфекции индуцировать начало и прогрессирование опухолевого процесса.
Ковчуром П.И. доказано положительное влияние иммуномодулятора «аллокин-альфа» на иммунный статус организма больных пре- и микроинвазивным раком шейки матки, что позволяет считать возможным применение этого препарата в комплексном лечении больных инвазивными формами местно-распространенных форм рака шейки матки [3].
Важным аспектом механизма действия плазмафереза и неспецифической иммунотерапии при проведении лекарственного лечения рака шейки матки T1b2-2bN0-1M0 стадий может служить формирование симптомокомплекса общей неспецифической адаптационной реакции (ОНАР), типы которой характеризуются различной направленностью морфо-функциональных изменений и состоянием неспецифической резистентности в организме: от патологических стрессорных (в острой и хронической форме) с низким уровнем резистентности до физиологических антистрессорных, соответствующих ОНАР тренировки, спокойной и повышенной активации с характерным высоким уровнем резистентности [1].
Цель исследования: изучить и сравнить структуру и характер интегральных адаптационных реакций больных раком шейки матки T1b2-2bN0-1M0 стадий при проведении различных модификаций неоадъювантной химиотерапии.
Материалы и методы
В представленной работе проанализирована структура общей неспецифической адаптационной реакции 47 больных местно-распространенными формами рака шейки матки T1b2-2bN0-1M0 стадий. Больные были репродуктивного возраста (от 25 до 48 лет). Всем больным лечение начинали с неоадъювантной химиотерапии по схеме: цисплатин, блеомицетин. В первой группе (12 больных) и во второй группе (15 больных) началу курса НАХТ предшествовал сеанс гравитационного лечебного плазмафереза. Отличием второй группы от первой явилось дополнительное проведение курса неспецифической иммунотерапии препаратом «аллокин-альфа», который начинали на следующий день после окончания курса химиотерапии (суммарная курсовая доза составила 6 мг). В третью группу вошли 20 больных, получавших только неоадъювантную химиотерапию по общепризнанной стандартной методике.
В процессе лечения идентификация структуры общей неспецифической адаптационной реакции проводилась индивидуально у каждой пациентки всех групп. Определяли тип общей неспецифической адаптационной реакции по морфологическому составу крови (формула Шиллинга), сигнальным параметрам порядка общей неспецифической адаптационной реакции – уровнем лимфоцитов, параметрами напряжения и неполноценности общей неспецифической адаптационной реакции – уровнем лимфоцитов, параметрами напряжения и неполноценности общей неспецифической адаптационной реакции – эозинофилов, моноцитов и общего числа лейкоцитов. Подсчет элементов вели в мазках крови, окрашенных по Романовскому – Гимза, используя метод миандров с обеих сторон мазка по 100 клеток.
Результаты и обсуждение
В исходном состоянии у больных первой группы доля реакций тренировки превосходила в 3 раза частоту выявления стресса и в 1,5 раза – других антистрессорных реакций.
Структура общей неспецифической адаптационной реакции после проведения дискретного плазмафереза включала исключительно антистрессорные реакции: увеличение в 5,5 раз частоты развития реакции спокойной активации и в 2,2 раза повышенной активации. На фоне отсутствия стресса и переактивации полученные данные свидетельствовали о физиологическом влиянии плазмафереза на адаптивный статус пациенток (рис.1).
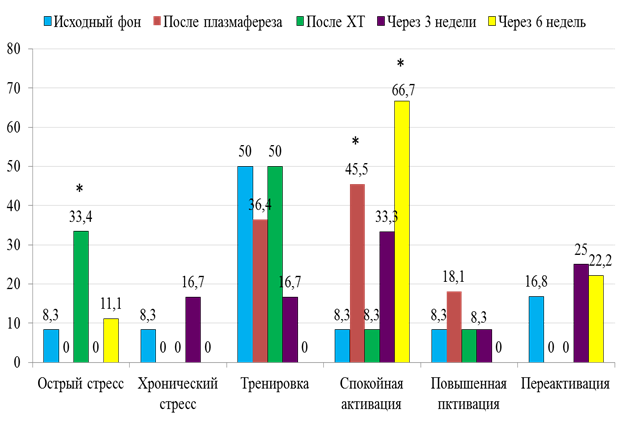
Рис.1. Структура адаптационных реакций у больных 1 группы.
* – различия достоверны по сравнению с исходным фоном
Непосредственно сразу после проведения курса неоадъювантной химиотерапии структура общей неспецифической адаптационной реакции в первой группе существенно изменилась в связи с формированием у трети пациенток острой формы стресса. В структуре антистрессорных реакций вновь преобладала реакция тренировки, а спокойная и повышенная активация выявлялись в единичных случаях. Через 3 недели в первой группе больных острой формы стресса не отмечали ни в одном случае, а частота хронического стресса была в 4,5 раза меньше, чем антистрессорных реакций. Из реакций физиологического типа самой частой была спокойная активация, при этом отмечено формирование переактивации, доля которой была в 3 раза больше, чем повышенной активации. Через 6 недель (от исходного фона) достоверно преобладала частота развития реакций спокойной активации, которая отмечена у большинства больных и была выше доли стрессорных реакций в 6 раз.
Включение в программу лечения сеанса дискретного плазмафереза во второй группе больных перед проведением курса неоадъювантной химиотерапии в сочетании с иммунотерапией сопровождалось изменением фоновой структуры общей неспецифической адаптационной реакции. Количество антистрессорных реакций уменьшилось за счет перехода в хроническую форму стресса. Ни в одном случае не отмечено острой формы стресса, при этом доля хронического стресса увеличилась в 2 раза. Изменения коснулись и структуры антистрессорных реакций: в 2 раза уменьшилась доля реакций тренировки, тогда как количество реакций спокойной активации достоверно возросло. Несмотря на увеличение доли хронического стресса, общегрупповая структура общей неспецифической адаптационной реакции свидетельствовала о достаточно высоком биоадаптивном потенциале организма перед проведением химиотерапии.
После проведения первого курса неоадъювантной химиотерапии ситуация коренным образом изменилась подобно той, что наблюдалась в первой группе больных, получавших химиотерапию без иммуномодуляторов. Применение иммунотерапии в схеме лечения позитивно отразилось на структуре общей неспецифической адаптационной реакции. Через 3 недели после проведения химиоиммунотерапии идентифицированы антистрессорные реакции тренировки и спокойной активации в 80 % случаев, причем частота последней превышала в 1,7 раза тренировку. Через 6 недель (т.е. через 3 недели после второго курса неоадъювантной химиотерапии) ситуация продолжала оставаться стабильной с той особенностью, что спокойная активация сменилась повышенной (рис. 2).
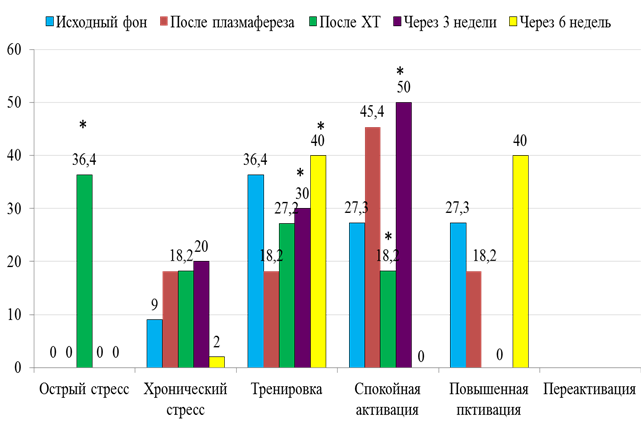
Рис. 2. Структура адаптационных реакций у больных 2 группы.
* – различия достоверны по сравнению с исходным фоном
Таким образом, применение иммунотерапии способствовало удержанию устойчивости антистрессорных реакций.
Достаточно выражено проявился эффект стрессогенности химиотерапии без предварительного плазмафереза в третьей группе больных. Формирование острого и хронического стресса увеличилось относительно исходного фона в 4 раза и составило 61,5 % общегрупповой структуры общей неспецифической адаптационной реакции. В структуре антистрессорных реакций доминировала реакция тренировки. Также соотношение адаптационных реакций подтверждало ингибирование защитных механизмов адаптации при проведении стандартной цитотоксической терапии.
Через 3 недели после проведения первого курса предоперационной химиотерапии в 46 % случаев были выявлены переходы из стресса в спокойную и повышенную активацию. По истечении 6 недель (т.е. после второго курса неоадъювантной химиотерапии) вновь возросла частота развития стресса в хронической форме (в 5,6 раз), не зарегистрирована реакция тренировки, а доля спокойной и повышенной активации в сумме превышала всего в 1,3 раза долю стресса (рис. 3).
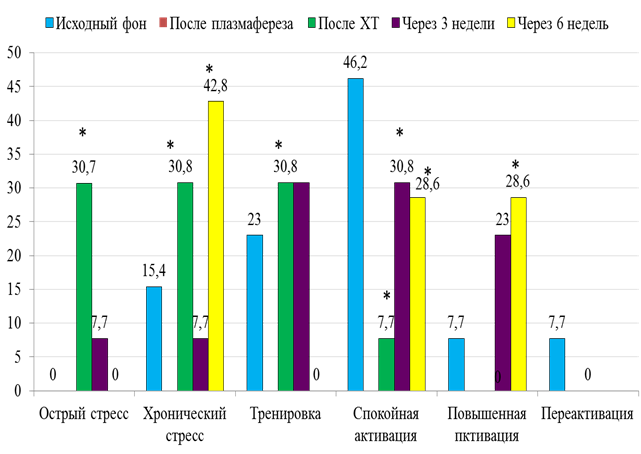
Рис. 3. Структура адаптационных реакций у больных 3 группы.
* – различия достоверны по сравнению с исходным фоном
Выводы
Исходя из вышеизложенного, можно заключить, что неоадъювантная химиотерапия в лечении больных местно-распространенными формами рака шейки матки IB-IIIB стадий с включением в программу лечения экстракорпоральных методов детоксикации, в частности, сеансов лечебного плазмафереза и иммунотерапии препаратом «аллокин-альфа» обеспечивает синергию и пролонгацию активности механизмов антистрессорной защиты, а также улучшение противоопухолевой устойчивости организма больной.
Упреждающая детоксикация является необходимым лечебным звеном при местно-распространенном злокачественном росте, так как позволяет сдерживать стрессогенное влияние химиотерапии на организм.
Включение в программу лечения неспецифической иммунотерапии способствует устойчивости антистрессорных реакций организма.
Библиографическая ссылка
Меньшенина А.П., Шихлярова А.И., Моисеенко Т.И., Франциянц Е.М., Ушакова Н.Д., Вереникина Е.В., Адамян М.Л., Чалабова Т.Г., Черкасова А.А. АНАЛИЗ ИЗМЕНЕНИЯ АДАПТАЦИОННЫХ РЕАКЦИЙ ПРИ ПРОВЕДЕНИИ ЭКСТРАКОРПОРАЛЬНЫХ МЕТОДОВ ДЕТОКСИКАЦИИ И НЕСПЕЦИФИЧЕСКОЙ ИММУНОТЕРАПИИ В ЛЕЧЕНИИ РАКА ШЕЙКИ МАТКИ // Современные проблемы науки и образования. 2017. № 2. ;URL: https://science-education.ru/en/article/view?id=26238 (дата обращения: 16.05.2026).



