Scientific journal
Modern problems of science and education
ISSN 2070-7428
"Перечень" ВАК
ИФ РИНЦ = 0,936
THE COMPARISON OF THE RADIATION DOSE TO THE IPSILATERAL LUNG FOR VARIOUS MODES OF 3-D RADIATION TREATMENT OF THE BREAST CANCER PATIENTS
В связи с ростом осведомленности населения, увеличением числа скрининговых программ, развитием технологий получения изображений и более эффективной терапией наблюдается более раннее выявление РМЖ и большая продолжительность жизни; все это объясняет возрастающий интерес к снижению токсичности ЛТ.
Лучевые повреждения нормальных тканей являются неизбежным следствием воздействия ионизирующего излучения (ИИ). Частота и степень тяжести лучевых повреждений зависят от совокупности многих факторов: методики облучения, значения разовых и суммарных поглощенных доз, индивидуальной радиочувствительности, сопутствующей патологии и т.д. Развитие острых и хронических постлучевых осложнений коррелирует с суммарной очаговой дозой (СОД), дозой за фракцию и объемом легочной ткани, подвергшейся облучению [4; 8; 10].
Лучевой пульмонит включает в себя целый ряд клинических признаков и симптомов. Проявления варьируют от случайных рентгенологических находок до обширных поражений легочной ткани у пациентов с выраженными клиническими проявлениями. Симптомы острого лучевого пульмонита обычно появляются через 2-3 месяца после лучевой терапии, но могут начинаться и через месяц, и через 6 месяцев после окончания лечения [4-6].
Лучевой пульмонит – это воспалительный процесс, который может полностью разрешиться (самостоятельно или под воздействием антибактериальной и гормональной терапии) или прогрессировать до необратимого фиброза. В случае прогрессирования легочного фиброза могут ухудшаться показатели легочных функциональных тестов. При поражении небольшого участка легочной ткани смежные участки легкого могут компенсировать дыхательную функцию и предупредить развитие серьезных клинических изменений [9].
Процесс фиброзирования легочной ткани протекает в сроки 6-24 месяца и обычно стабилизируется к двум годам. Легочный фиброз может протекать бессимптомно или с признаками нарушения дыхательной функции в зависимости от объема легочной ткани, вовлеченной в процесс фиброзирования, и компенсаторных возможностей легочной ткани, не подвергавшейся облучению. Легочная ткань становится функционально неполноценной и может стать потенциальной причиной развития легочной гипертензии, ведущей к развитию сердечной недостаточности [2; 3].
Клинические наблюдения показывают необходимость избегать дозы на весь объем легкого более чем 20 Гр если нет уверенности, что необлученное легкое компенсирует дыхательную функцию. Goldman U. et al. сообщают в своей работе о 3D конформной лучевой терапии, проведенной с ограничением по левому легкому V20 ≤30% 88 пациенткам с ранними стадиями левостороннего РМЖ, только об одном случае умеренного острого пульмонита, потребовавшего лечения кортикостероидами и антибиотиками. Кроме того, в некоторых работах есть указания на связь развития постлучевых осложнений со стороны легких и возрастом пациентов [7].
Таким образом, снижение лучевой нагрузки на легкое при проведении лучевой терапии у больных РМЖ является актуальной задачей практикующих врачей-радиотерапевтов.
Цель настоящего исследования – проспективное сравнение трех различных вариантов полного облучения МЖ с/без включения надключичных и подключичных ЛУ: стандартное положение на спине на свободном дыхании (ССД), положение на спине с управляемой задержкой дыхания на высоте вдоха (СЗД) и положение на животе (ЖСД). Оценить влияние различных методик на дозиметрические показатели лучевой нагрузки на левое легкое.
Материалы и методы
В ФГБУ «РНЦРХТ» Минздрава России для анализа были подготовлены планы ЛТ 20 пациенток с РМЖ с левосторонней локализацией. Для каждого исследуемого случая были рассчитаны 8 дозиметрических планов на основе трех серий КТ-сканов:
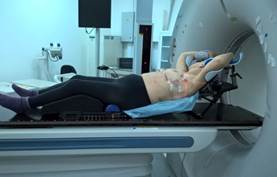
1. В положении лежа на спине с использованием индивидуально модифицированного breast-board на свободном дыхании, с/без включения в зону облучения над- и подключичных ЛУ (план 1/2), рис. 1А.
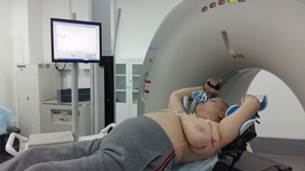
2. В положении лежа на животе с использованием рrone-board с/без включения подмышечных ЛУ (план 3/4), рис. 1Б.
3. В положении лежа на спине с использованием индивидуально модифицированного breast-board с задержкой дыхания, с/без включения в зону облучения над- и подключичных ЛУ (ptv 1.0 cm, план 5/6 и ptv 0,5 cm, план 7/8), рис. 1В.
 А
А 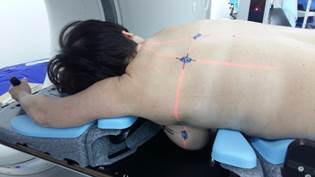 Б
Б
 В
В
Рис. 1. Укладка пациента в процессе предлучевой подготовки: А – положение на спине, на свободном дыхании; Б – положение на животе; В – положение на спине с управляемой задержкой дыхания на высоте вдоха
Для активного управления задержкой дыхания на высоте вдоха применялось устройство АВС (Elekta, Sweden), конструктивно состоящее из персонального компьютера с установленным на нем специальным программным обеспечением, спирометра, дыхательной трубки (для дыхания пациента на протяжении всей процедуры ЛТ). Встроенный в дыхательную трубку клапан после прохождения через спирометр порогового объема воздуха (установленного индивидуально в ходе тренировки) прерывает дыхательный цикл на заданной величине. Использовалось среднее фракционирование. Доза за фракцию 3 Гр, физическая суммарная очаговая доза (СОДфиз) на молочную железу – 42 Гр, в случае включения над- и подключичных лимфатических узлов ЛУ СОДфиз – 39 Гр. При этом, учитывая использование среднего фракционирования, произведен перерасчет биологически эффективных доз проявления лучевых реакций и осложнений со стороны легких с учетом α/β, по формуле:
![]() =
=![]() ,
,
где ![]() - суммарная доза в режиме стандартного фракционирования,
- суммарная доза в режиме стандартного фракционирования, ![]() – изоэффективная доза в режиме среднего фракционирования, d1 – доза фракция в режиме стандартного фракционирования, d1 - доза фракция в режиме среднего фракционирования.
– изоэффективная доза в режиме среднего фракционирования, d1 – доза фракция в режиме стандартного фракционирования, d1 - доза фракция в режиме среднего фракционирования.
V30 стандартного фракционирования соответствовало для ранних лучевых реакций (пульмониты, α/β=9) - V28pulm, для осложнений (пневмофиброз, α/β=3,1) - V25pulm.
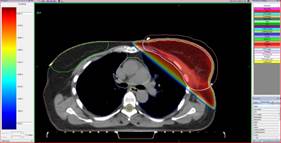
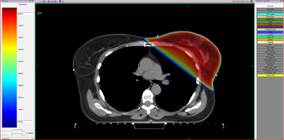
КТ-данные передавались на станцию дозиметрического планирования (Xio, Elekta). Легкие оконтуривались с помощью функции автоматического оконтуривания программы Monaco (Elekta). Все этапы предлучевой подготовки проводились одной и той же командой, включавшей врача-топометриста, радиотерапевта и медицинского физика (рис. 2).
 А
А 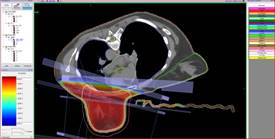 Б
Б
 В
В
Рис. 2. Дозиметрическое распределение при различных методиках: А – положение на спине, на свободном дыхании; Б – положение на животе; В – положение на спине с управляемой задержкой дыхания на высоте вдоха
Использовалось среднее фракционирование. Доза за фракцию 3 Гр, СОД на молочную железу 42 Гр DVH (дозо-объемные гистограммы) были сгенерированы для всех оконтуренных структур во всех планах для каждого пациента. Для ипсилатерального легкого были рассчитаны: процент от объемов, получивших дозы ≥28 Гр (V28легкое при α/β 9) для ранних пульмонитов. А также процент от объемов, получивших дозы ≥ 25 Гр (V25легкое α/β 3,1) для поздних осложнений – пневмофиброз.
Статистический анализ проводили с помощью программы STATISTICA 12.
Для сравнения дозо-объемных параметров использовали описательную статистику, дисперсионный анализ (ANOVA), направленный на поиск зависимостей в экспериментальных данных путём исследования значимости различий в средних значениях, который позволял сравнивать средние значения трёх и более групп. Для всех статистических тестов P<0,05 было статистически значимым.
Результаты
При сравнении Dmean легкое наилучшие результаты достигнуты в группе ЖСД, наихудшие в позиции на ССД (табл. 1, рис. 3).
Таблица 1
Dmean легкое при различных вариантах облучения
|
Группы |
Кол-во |
Средняя доза, сГр |
Медиана, сГр |
Мин. доза, сГр |
Макс. доза, сГр |
Std. Dev. |
Standard |
|
Все серии КТ-сканирования |
160 |
906,94 |
892,8 |
122,4 |
1674,3 |
290,76 |
25,9 |
|
ССД + ВФ |
20 |
1172,07 |
1163,6 |
793,5 |
1615,0 |
218,97 |
54,74 |
|
ССД - ВФ |
20 |
1040,42 |
1023,7 |
707,9 |
1394,8 |
173,89 |
43,47 |
|
ЖСД - AxNod |
20 |
412,11 |
419,8 |
122,4 |
603,5 |
144,41 |
37,28 |
|
ЖСД + AxNod |
20 |
742,0 |
713,9 |
535,4 |
901,9 |
119,65 |
30,89 |
|
СЗД + ВФ ptv 1.0 cm |
20 |
1085,53 |
1008,5 |
792,5 |
1674,3 |
241,17 |
60,29 |
|
СЗД - ВФ ptv 1.0 cm |
20 |
1011,33 |
921,8 |
795,1 |
1523,3 |
202,97 |
50,74 |
|
СЗД + ВФ ptv 0,5 cm |
20 |
905,86 |
845,4 |
696,4 |
1409,0 |
208,97 |
52,24 |
|
АВС-ЛУ ptv 0,5 cm |
20 |
844,96 |
770,95 |
648,4 |
1309,6 |
186,26 |
46,56 |
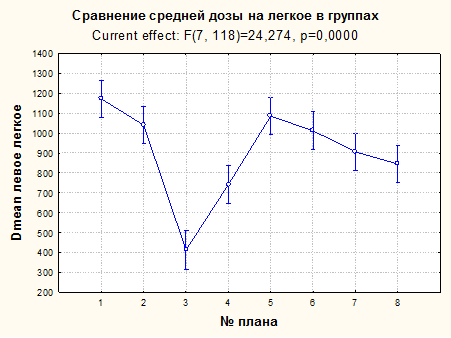
Рис. 3. Сравнение средней дозы на легкое в группах
Средний объем легкого в позиции на спине на свободном дыхании составил 1236,6 см3, на животе - 1233,6 см3, на задержке дыхания в положении на спине - 2251,8 см3 (рис. 4).
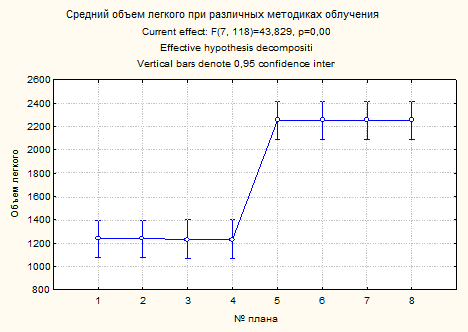
Рис. 4. Средний объем левого легкого при различных методиках облучения
При сравнении планов ССД, СЗД и ЖСД, когда в зону облучения входили только МЖ и аксиллярные ЛУ, наименьшие значения Dmean легкое зафиксированы в положении на животе (p=0,00002**) (рис. 5, табл. 2).
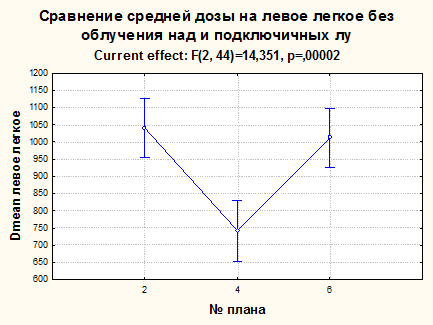
Рис. 5. Сравнение средней дозы на левое легкое без облучения над- и подключичных лимфоузлов
Анализ доз на легкое в планах ССД, СЗД и ЖСД, когда в зону облучения входили над- и подключичные ЛУ (сравнивали ССД и СЗД методики), не показал значимых различий (р=0,296) (рис. 6, табл. 3).
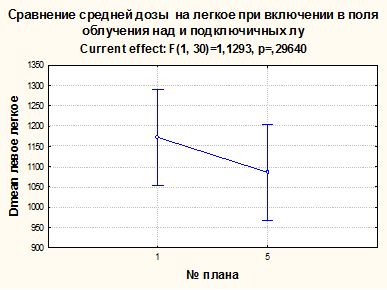
Рис. 6. Сравнение средней дозы на левое легкое при включении в поля облучения над- и подключичных лимфоузлов
Аналогичная закономерность наблюдалась при оценке значений V25 (α/β 3,1) и V28 (α/β 9). Наибольшие дозы, приходящиеся на V25легкое (α/β 3,1) и V28легкое (α/β 9) левого легкого, получены в положении на ССД, наименьшие в положении на СЖД в случае, если не облучаются над- и подключичные ЛУ (р<0,05) (табл. 2).
Таблица 2
Сравнение Dmean легкое и V28легкое левого легкого без облучения над- и подключичных лимфоузлов при ССД, ЖСД, СЗД
|
Показатель |
ССД |
ЖСД |
СЗД |
P value |
|
Dmean легкое, Гр |
10,42 |
7,42 |
10,11 |
Р=0,00002** |
|
V28легкое (α/β=9 пульмонит) |
19,60 |
9,19 |
19,01 |
Р=0,00000** |
|
V25легкое (α/β=3 пневмофиброз) |
20,72 |
10,19 |
20,17 |
Р=0,00000** |
Анализ доз на левое легкое в планах ССД, СЗД и ЖСД, когда в зону облучения входили над- и подключичные ЛУ (сравнивали ССД и СЗД методики), не выявил достоверных различий (р>0,05), (табл. 3). Осуществление облучения над- и подключичных ЛУ в положении на животе технически не представляется возможным.
Таблица 3
Сравнение Dmean легкое и V28легкое левого легкого с включением в поля облучения над- и подключичных лимфоузлов при ССД, СЗД
|
Показатель |
ССД |
СЗД |
P value |
|
Dmean легкое, Гр |
11,72 |
10,85 |
Р=0,2964 |
|
V28легкое (α/β=9 пульмонит) |
21,64 |
20,17 |
Р=0,461 |
|
V25легкое (α/β=3 пневмофиброз) |
23,07 |
21,49 |
Р=0,438 |
Сравнение всех выбранных нами показателей: Dmean легкое, V28легкое (α/β 9) и V25легкое (α/β 3,1) левого легкого показало наличие следующих закономерностей: при включении в зону облучения МЖ и только аксиллярных ЛУ методика в позиции на животе на свободном дыхании является наиболее оптимальной с точки зрения снижения лучевой нагрузки на легкое; анализ значений Dmean легкое, V28легкое (α/β 9) и V25легкое (α/β 3,1) при использовании ССД и СЗД методик, с включением в поля облучения над- и подключичных ЛУ, не выявил каких-либо преимуществ между методиками по всем показателям.
Обсуждение
Раннее выявление заболевания, молодой возраст пациентов РМЖ, определенные успехи в фармакологическом лечении привели к увеличению продолжительности жизни. Освоение и внедрение в практическое здравоохранение новых современных методик в снижении лучевых нагрузок на ОР в настоящее время является актуальной задачей. Целью нашего исследования являлось изучение влияния различных методик проведения ЛТ при РМЖ на параметры дозо-объемного распределения критических структур. Мы выявили статистически значимые снижения доз на ипсилатеральное легкое при использовании укладки на животе. Однако эти преимущества могут быть использованы только при облучении молочной железы на ранних стадиях, когда не проводится облучение над- и подключичных лимфоузлов. Соответственно, это очень ограниченный контингент больных. В случае включения над и подключичных лимфоузлов методики на свободном дыхании и с задержкой дыхания в положении на спине имели приблизительно одинаковые дозные нагрузки на легкое. Кроме того, в нашей работе, опубликованной ранее, мы оценили лучевую нагрузку на сердце и получили наихудшие результаты в положении лежа на животе [1]. Т.о., укладка пациента на животе, скорее всего, подходит для пациентов с поражением правой МЖ, так как в поля облучения не будет попадать сердце, а выигрыш в снижении нагрузки на легкое очевиден.
К недостаткам методики проведения ЛТ в положении на животе можно отнести более длительную предлучевую подготовку пациента, проблемы, возникающие при подведении полей через контралатеральную молочную железу, подведение многочисленных сегментов во избежание больших максимумов ионизации (что в свою очередь приводит к значительному увеличению продолжительности сеанса ЛТ и, соответственно, снижению пропускной способности линейного ускорителя), техническую невозможность облучения над- и подключичных ЛУ, а также трудности воспроизводимости укладки от сеанса к сеансу, о которых упоминают многие авторы.
Выводы
Позиция на животе может улучшить дозо-объемное распределение в отношении ипсилатерального легкого и, соответственно, уменьшить риск развития ранних реакций и поздних осложнений со стороны легких.
Идеальными кандидатами для проведения ЛТ при РМЖ в положении на животе являются пациенты с поражением правой молочной железы, при отсутствии показаний к облучению над- и подключичных лимфоузлов.
Библиографическая ссылка
Маслюкова Е.А., Корытова Л.И., Бондаренко А.В., Корытов О.В. РЕЗУЛЬТАТЫ СРАВНЕНИЯ ЛУЧЕВОЙ НАГРУЗКИ НА ИПСИЛАТЕРАЛЬНОЕ ЛЕГКОЕ ПРИ РАЗНЫХ ВАРИАНТАХ КОНФОРМНОГО ОБЛУЧЕНИЯ РАКА МОЛОЧНОЙ ЖЕЛЕЗЫ // Современные проблемы науки и образования. 2017. № 1. ;URL: https://science-education.ru/en/article/view?id=26096 (дата обращения: 07.05.2026).



