Scientific journal
Modern problems of science and education
ISSN 2070-7428
"Перечень" ВАК
ИФ РИНЦ = 0,936
BIS-MONITORING USE FOR THE ANESTHESIA AND SEDATION LEVEL CONTROL DURING XENON ANESTHETIC SUPPORT IN OPHTHALMOSURGERY
Ранее нами были опубликованы результаты сравнительных исследований информативности BIS-мониторинга при севорановой и ксеноновой общей комбинированной анестезии при проведении офтальмологических операций [8]. Было выявлено, что на начальных этапах общей анестезии, проводимой ксеноном, уровень BIS-индекса не всегда соответствует клинической картине анестезии. Тем не менее, учитывая специфику офтальмохирургических вмешательств, выполняемых без миорелаксантов, необходимость контроля глубины анестезии сохранялась.
В ряде исследований показано, что BIS-алгоритм, эмпирически основанный на ЭЭГ при использовании «ГАМК-ергических» гипнотиков (пропофол), не всегда корректен в отношении общих анестетиков с NMDA-антагонистичными свойствами: кетамина, N2O, α2-адренергических агонистов [15, 20, 21]. В других литературных источниках указывается на значимое соответствие BIS и клинической картины анестезии ксеноном [11, 2,10]. Степановой О.В. (2008) отмечена стабильность BIS на этапе поддержания моноанестезии ксеноном. Höсker J.et al. (2009) подтвердили соответствие BIS уровней при анестезии ксеноном и пропофолом у возрастных пациентов, однако не исключили возможность расхождений в оценке глубины анестезии в своих наблюдениях. Другие авторы отмечают относительную информативность BIS-индекса на этапе поддержания анестезии ксеноном и явное отставание от клинических проявлений анестезии на этапах индукции и пробуждения [12]. Вяткин А.А. (2014) для оценки глубины анестезии ксеноном рекомендует использовать не BIS-показатели, а мониторинг слуховых вызванных потенциалов.
Ксенон, являясь антагонистом NMDA-рецепторов, подавляет гиперактивацию нейронов под действием глутамата и других возбуждающих аминокислот, предотвращая эксайтотоксичность [14]. В результате ксенон может проявлять не только анестетические свойства, но и обладать выраженным анксиолитическим, нейропротекторным и ноотропным действием. Благодаря способности стабилизировать кровообращение головного мозга, купировать болевой синдром и снимать психоэмоциональное напряжение, ксенон нашел применение в комплексной терапии травматических, ишемических и дисциркуляторных поражений головного мозга, при коррекции острых и хронических стрессовых расстройств [3]. Ингаляции ксенона, как анальгетического, седативного средства и анестетика, в клинике Краснодарского филиала ФГАУ «МНТК “Микрохирургия глаза” им. акад. С.Н. Федорова» Минздрава России нашли применение при проведении операций лазерной коррекции с использованием фемтосекундного лазера. Наиболее частое использование фемтосекундного лазера в офтальмохирургии связано с формированием роговичного клапана при проведении операции FemtoLasik. Роговица в целом и фемто-клапан в частности обладают рядом анатомо-топографических и оптических преимуществ по сравнению с роговицей и клапаном, срезанным механическим микрокератомом [6, 19]. Однако несоблюдение правил аппланации индивидуального интерфейса на роговицу пациента, неправильная центрация роговицы, низкая компрессия при проведении процедуры фемтодиссекции или изменение положения головы пациента в вертикальной плоскости могут повлечь за собой потерю вакуума и отсоединение интерфейса от роговицы. Потеря вакуумной фиксации при операции FemtoLasik ведет к формированию неравномерного по форме и толщине лоскута роговицы, что негативно влияет на рефракционные параметры роговицы и результат операции. Одной из причин возникновения подобных осложнений могут быть выраженные тревожность и беспокойство пациентов [16,18,19,9,6]. Таким образом, на сегодняшний день весьма актуальной задачей является дальнейшая разработка комплекса лечебно-диагностических мероприятий, позволяющих исключить риск возникновения операционных осложнений, связанных с потерей вакуума. К ним можно отнести выявление эмоционально лабильных пациентов и привлечение к их предварительной подготовке к проведению операции врача-анестезиолога.
У данной категории пациентов психоэмоциональное напряжение сопровождается гемодинамическими и вегетативными проявлениями, в связи с чем необходима аналгоседация. Особенность ее проведения – сохранение возможности кооперации пациента с хирургом на различных этапах проведения такого рода вмешательств. Такие условия создавались при проведении предоперационного сеанса ингаляции кислородно-ксеноновой смеси. Поскольку необходимо было обеспечивать безопасный уровень седации, не только исключающий депрессивное влияние анестетика на дыхание и кровообращение, но и позволяющий осуществлять взаимодействие пациента и хирурга, актуальным был мониторинг глубины наркоза.
Цель работы: исследовать показатели BIS-индекса при проведении общей комбинированной ксеноновой анестезии и во время сеансов ингаляции кислородно- ксеноновой смеси в режиме аналгоседации.
Материал и методы. Для оценки эффективности BIS-мониторинга при общей анестезии во время офтальмохирургических вмешательствах (кератопластика, коррекция косоглазия или птоза, склеропластика) были исследованы параметры гемодинамики (среднее артериальное давление – САД и ЧСС), вентиляции (SatO2 и etCO2) и BIS-индекс в 1-й группе пациентов (19 человек), где в качестве основного анестетика использовался ксенон (Xe). Возраст пациентов – от 15 до 35 лет. Анестезия проводилась по следующему алгоритму: премедикация – феназепам на ночь и лоратадин утром перед операцией, в операционной – атропина сульфат 0,01 мг/кг, реланиум 5 мг в/в; индукция анестезии проводилась титрованием дозы пропофола до 1–1,5 мг/кг и фентанилом – 3–5 мкг/кг. После вводной анестезии устанавливалась ларингеальная маска соответствующего размера. В большинстве случаев сохранялось спонтанное дыхание, при угнетении дыхания и нарастании гиперкапнии подключалась ИВЛ. Отсутствие необходимости в миорелаксантах и высокая эффективность местной (ретробульбарной или субтеноновой) анестезии в офтальмологии – определяют необходимость достаточно глубокой вводной анестезии (чтобы гарантированно исключить реакцию на введение ларингеальной маски) и возможность проведения основной анестезии на границе уровня глубокой седации и хирургического уровня [1]. Аналгезия обеспечивается фентанилом, местной блокадой, НПВС или центральным аналгетиком нефопамом. Ксеноновая анестезия осуществлялась аппаратом «Ксена-010» в условиях полного герметичного реверсивного дыхательного контура по стандартной методике (денитрогенизация, насыщение ксеноном, поддержание анестезии с концентрацией анестетика 50–55 %). На этапе основной анестезии пациентам болюсно вводился фентанил по 50 мкг каждые 15–20 мин. Инфузионная поддержка проводилась физиологическим раствором. Мониторинг включал неинвазивный контроль АД, пульсоксиметрию, ЭКГ, определение газового состава вдыхаемой и выдыхаемой воздушной смеси, капнографию. BIS-мониторинг осуществлялся аппаратом Covidien. Этапы исследования: 1-й этап – до начала анестезии (исходные показатели), 2-й этап – после индукции, 3-й – через 20 мин после начала анестезии, 4-й – через 40 мин анестезии.
Во вторую исследуемую группу вошли 12 человек в возрасте от 20 до 33 лет, которым планировалась проведение лазерной коррекции по технологии FemtoLASIK по поводу миопии средней и высокой степени и в качестве предоперационной подготовки проводилась ингаляция кислородно-ксеноновой смеси в режиме аналгоседации. Обычно при таких операциях достаточно topical-анестезии – местных анестетиков в виде глазных капель. Однако в некоторых случаях пациенты настолько эмоционально переживали предстоящее хирургическое вмешательство, что возникали показания к проведению анестезиологического пособия. Мы предложили таким пациентам вариант аналгоседации ксеноном с сохраненным сознанием. При этом экспозиция ксенона осуществлялась в субнаркотических концентрациях – 35–40 % (до 1/3 МАC) перед операцией. Сеансы проводились наркозным аппаратом «КСЕНА-01», работающим по закрытому контуру с мониторингом показателей гемодинамики (АД, ЧСС), дыхания (SatО2), газового состава смеси, BIS-мониторинг осуществлялся аппаратом Covidien (BIS-индекс и показателя миоплегии). Исследуемые показатели фиксировались до начала сеанса, на 10-й, 20-й, 30-й и 40-й минутах сеанса.
Статистический анализ был проведен с использованием программы MS Exсel.
Результаты исследования
При проведении общей анестезии во время офтальмохирургических вмешательствах на этапе индукции у пациентов отмечалось снижение САД (гипотензивный эффект пропофола) на 10 %. BIS-потенциал снижался с исходных показателей до 24 ЕД. В дальнейшем течение ксеноновой анестезии отличалось стабильностью гемодинамики, что соответствует литературным данным [4, 7].
Показатели гемодинамики, оксигенации и мониторинга глубины анестезии в группе 1 во время общей комбинированной анестезии ксеноном
|
Исследуемые показатели |
Исходные |
Индукция |
Через 20 мин |
Через 40 мин |
Достоверность различий |
|
АД сист. мм рт. ст. |
133,0±9,3 |
120,6±5,7* |
119,0±8,0* |
120,5±10 |
* – p<0,05 при сравнении с 1-м этапом.; **– p<0,05 при сравнении со 2-м этапом. |
|
АД диаст.мм рт. ст. |
66,0±6,0 |
63,3±12,4 |
63,6±14,4 |
78,5±9,5 |
|
|
САД, мм рт. ст. |
95,0±4,1 |
89,0±7,9* |
88,0±11,1* |
98,0±13,6** |
|
|
ЧСС в мин. |
82,6±3,1 |
100,0±7,3* |
93,0±4,6* |
92,0±3,0*,** |
|
|
BIS, ЕД |
96,0±12,2 |
24,1±5,9* |
54,9±10,7*,** |
39,8±9,7* |
|
|
O2 in, % |
99±0,4 |
80,2±9,3* |
38,5±4,6*,** |
37,2±5,9*,** |
|
|
SatО2 |
98,5±0,5 |
99±0,5 |
99±1,0 |
97±1,0 |
|
|
CO2ex |
- |
4,65±0,8 |
5,5±1,2 |
5,9±1,5 |
На следующих этапах BIS-индекс повышался и в основном находился в коридоре от 40 до 60 ЕД. Однако на 3-м этапе в 40 % наблюдений отмечалось превышение порога 60 ЕД, при том, что показатели гемодинамики, данные ETAG-мониторинга и клинические данные свидетельствовали об адекватности анестезии и соответствии ее хирургическому уровню. К 4-му этапу BIS снизился с 54 до 39 ЕД, что соответствовало хирургическому уровню анестезии (см. табл.). Таким образом, в течение 20–25 мин после вводного наркоза и начала операции, в 40 % случаев при анестезии Xe наблюдалось несоответствие клинической картины и уровня BIS-мониторинга. После окончания операции подача Xe отключалась, регистрировалось повышение величины BIS-индекса более 80 ЕД, при восстановлении самостоятельного дыхания удалялась ларингеальная маска, пациенты открывали глаза, выполняли команды. Время восстановления сознания составило 4,0±1,2 мин.
В группе пациентов, которым проводилась аналгоседация кислородно-ксеноновой смесью перед эксимерлазерными вмешательствами, показатели гемодинамики и вентиляции были стабильны. Дополнительная премедикация обычно не требовалась или включала дормикумом в минимальных дозировках (1-2 мг в/в). По стандартной методике проводилась масочная анестезия ксеноном [6]. Продолжительность этапа денитрогенизации составляла 7,5±2,3 мин, затем подключался ксенон. Целевая концентрация ксенона – 35–40 % – достигалась в течение 10–12 мин, стадия глубокой седации наступала через 17–23 минуты после подключения ксенона.
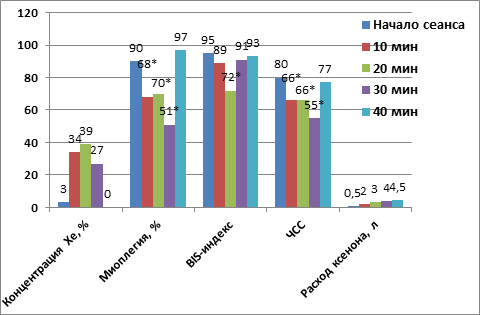
Динамика показателей гемодинамики, глубины седации и миоплегии во время сеансов аналгоседации ксеноном в группе 2
Увеличение содержания Xe в дыхательной смеси до 34–39 % сопровождалось снижением BIS-индекса до 89 и 72ЕД и миоплегии до 68–70 % (см. рис.). У 1/3 пациентов через 10–15 мин экспозиции ксенона появлялись легкие признаки эйфории – они пытались заговорить, улыбнуться. К 20-й минуте пациенты успокаивались, засыпали, снижалось исходно повышенное АД, ЧСС снижалась до 55,4±5,3 в мин. Экспозиция 40 % ксенона составляла 20 минут. После окончания сеанса сознание восстанавливалось через 2–3 минуты с полной ориентацией в пространстве и времени. Проводилась topical-анестезия, пациент был спокоен и готов к проведению операции, при необходимости мог выполнять все указания хирурга. Во время оперативных вмешательств пациенты, оставаясь в полном сознании, вели себя адекватно и спокойно. Жалоб на болевые ощущения не было ни у кого из пациентов. Расход ксенона составил от 3,7 до 4,5 л за сеанс.
Выводы
BIS-индекс позволяет осуществить более объективный контроль проведения анестезии, значительно повышает качество ее выполнения и уровень безопасности. При общей ксеноновой анестезии необходимо учитывать: почти у половины пациентов в течение первых 10–15 мин показатели BIS-индекса не соответствуют клинической картине хирургической стадии наркоза (выше уровня 60ЕД). Ингаляции кислородно-ксеноновой смеси в режиме аналгоседации обеспечивают адекватную ноцицептивную и антистрессовую защиту и позволяют гарантированно безопасно провести лазерные офтальмологические вмешательства у эмоционально лабильных пациентов.
Библиографическая ссылка
Мясникова В.В., Сахнов С.Н., Клокова О.А., Цымбалов О.В. ПРИМЕНЕНИЕ BIS-МОНИТОРИНГА ДЛЯ КОНТРОЛЯ ГЛУБИНЫ АНЕСТЕЗИИ И СЕДАЦИИ ПРИ ПРОВЕДЕНИИ АНЕСТЕЗИОЛОГИЧЕСКИХ ПОСОБИЙ С ИСПОЛЬЗОВАНИЕМ КСЕНОНА В ОФТАЛЬМОХИРУРГИИ // Современные проблемы науки и образования. 2016. № 6. ;URL: https://science-education.ru/en/article/view?id=25884 (дата обращения: 05.05.2026).
DOI: https://doi.org/10.17513/spno.25884



