Scientific journal
Modern problems of science and education
ISSN 2070-7428
"Перечень" ВАК
ИФ РИНЦ = 0,936
ASSESSMENT OF WAKE-SLEEP ORGANISATION IN PATIENTS WITH BRAIN TUMOR
Опухоли центральной нервной системы занимают первое место по среднегодовым темпам прироста заболеваемости в России, что обуславливает целесообразность разработки методов ранней диагностики новообразований и выявления наиболее значимых прогностических факторов, определяющих тактику лечения и реабилитации больных с данной патологией [2; 7].
Известно, что более чем в 80 % наблюдений у пациентов с опухолями головного мозга (ОГМ) проявляются различные когнитивные девиации, которые могут быть обусловлены самим заболеванием или являться побочным эффектом лечения, следствием неврологических заболеваний, депрессии, тревоги, нарушения сна [3; 4]. Из всех перечисленных симптомов нарушение сна является одним из самых тяжелых и часто встречаемых среди пациентов данной категории. Наиболее распространенные из них – это инсомния, нарушения дыхания во время сна и гиперсомния [3].
Традиционно физиологическая оценка изменений биоэлектрической активности мозга при ОГМ используется в клинике для локализации очага и определения степени общемозговых изменений. В серии работ Н.П. Бехтеревой (1960) [1] показано, что в области локализации новообразования в коре головного мозга возникают функциональные изменения мозговой ткани с формированием очага возбуждения либо торможения, что отражается в выраженности физиологических и патологических компонентов в биоэлектрической активности мозга. Соответственно физиологическая оценка изменений электроэнцефалограммы (ЭЭГ) в цикле сон-бодрствование у больных с опухолевым поражением головного мозга представляет несомненный интерес для понимания механизмов, касающихся локализации функций в коре, взаимодействия больших полушарий с подкорковыми и стволовыми структурами. Полученные данные могут способствовать принятию конкретных мер, которые внесут вклад в профилактику и лечение нарушений сна у больных ОГМ.
В соответствии с этим целью работы определено исследование когнитивных функций и организации ночного сна у пациентов c первичной опухолью головного мозга до оперативного вмешательства и после удаления.
Методика исследования
Были обследованы 6 пациентов обоего пола в возрасте от 15 до 64 лет с первичными глиальными опухолями супратенториальной локализации. Пациенты находились на лечении в отделении нейроонкологии ФГБУ РНИОИ г. Ростова-на-Дону в 2016 г. Глиомы астроцитарного ряда GRI-II выявлены у пяти пациентов, у одного пациента обнаружена анапластическая астроцитома GRI-III. Опухоли с локализацией в лобной доле головного мозга наблюдались у четырех пациентов, височной доли – у двух. Объем опухоли и зоны перифокального отека оценивали по данным МРТ с использованием формулы:
V= π/6 * A *B *C,
где А, В, С – максимальные диаметры размеров опухоли и зоны распространения отека в трех перпендикулярных проекциях, π =3.14.
У всех пациентов до операции (тотальная резекция опухоли) и на седьмые сутки после нее оценивали выраженность когнитивных нарушений и проводили полисомнографическое исследование ночного сна. Исследования были проведены с соблюдением этических стандартов Декларации Хельсинки (1964), с получением у пациентов предварительного письменного согласия.
Тестирование пациентов проводилось в отдельном помещении подготовленным специалистом в присутствии лечащего врача. Были использованы тест «Батарея лобной дисфункции» (англ. Frontal assessment battery, FAB [5]), краткая шкала оценки психического статуса (англ. Mini-Mental State Examination, MMSE [6]), тест рисования часов [9].
Регистрацию ночного сна осуществляли с 21 часа вечера до 7 часов утра следующего дня на электроэнцефалографе-регистраторе «Энцефалан ЭЭГР-19/26» (Медиком МТД, Таганрог) в соответствии с международными стандартами [10]. Регистрировали ЭЭГ в монополярных отведениях F3,F4,С3,С4,О1,О2 (референтные электроды A1+A2), билатеральную электроокулограмму (правый, левый глаз), электромиограмму подъязычной мышцы, частоту дыхания в абдоминальном и торакальном отведениях, электрокардиограмму и пульсоксиметрию. Анализ полисомнограмм с выделением фаз и стадий сна осуществлялся тремя экспертами в соответствии с международными стандартами [10].
Рассчитывали общую продолжительность сна, первой, второй, третьей, парадоксальной его стадий и общее время бодрствования во время сна. Латентный период развития сна рассчитывали как время после выключения света до появления феноменов второй стадии сна. Процентную представленность второй стадии, дельта-сна и парадоксальной стадии сна определяли по отношению к общей продолжительности сна. Амплитудную асимметрию ЭЭГ рассчитывали автоматически с использованием программных средств Энцефалан для состояний: расслабленного бодрствования с закрытыми глазами, второй стадии, дельта-сна и парадоксальной стадии ночного сна.
Данные обрабатывали, используя пакет программ Statistica 8, использовали методы описательной статистики (все данные представлены как среднее значение и его стандартное отклонение, M±SD) и корреляционный анализ Пирсона.
Результаты исследования
В таблице 1 представлены данные пациентов и результаты бланкового тестирования до хирургического вмешательства и на седьмые сутки после операции. Оценка выраженности когнитивных нарушений до операции показала, что у двух пациентов они определялись как умеренные, у двух – выраженные и у двух – отсутствие нарушений.
Таблица 1
Результаты тестирования пациентов до операции и на седьмые сутки после операции
|
Пациент |
1 |
2 |
3 |
4 |
5 |
6 |
M±SD |
|
|
Объем опухоли, см3 |
32.1 |
46.8 |
47.5 |
17.8 |
61.6 |
3.2 |
34.8±21.5 |
|
|
До операции |
Краткая шкала оценки психического статуса, балл |
27 |
23 |
10 |
30 |
12 |
30 |
22.0±8.9 |
|
Тест «Батарея лобной дисфункции», балл |
12 |
9 |
7 |
17 |
12 |
18 |
12.5±4.3 |
|
|
Тест рисования часов, балл |
10 |
4 |
5 |
10 |
7 |
10 |
7.2±2.7 |
|
|
7 сутки после операции |
Краткая шкала оценки психического статуса, балл |
29 |
25 |
12 |
30 |
12 |
30 |
23.0±8.7 |
|
Тест «Батарея лобной дисфункции», балл |
18 |
12 |
9 |
16 |
11 |
18 |
14.0±3.8 |
|
|
Тест рисования часов, балл |
10 |
4 |
9 |
10 |
7 |
10 |
8.3±2.4 |
|
Согласно данным корреляционного анализа Пирсона степень нарушений когнитивных функций у пациентов в предоперационном периоде (r = - 0.84; p = 0.04) в 71 % случаев и на седьмые сутки после операции (r = - 0.82; p = 0.04) в 67 % зависела от объема опухоли (рис. 1). Как представлено в таблице 1, у пациентов 1, 2, 3, 5 с большим объемом опухоли мозга до операции выявлены значимые нарушения когнитивных функций, которые в послеоперационном периоде сохранялись, но с меньшей степенью выраженности. У пациентов с небольшим объемом новообразований мозга (пациенты 4, 6) нарушений когнитивных функций не было выявлено.
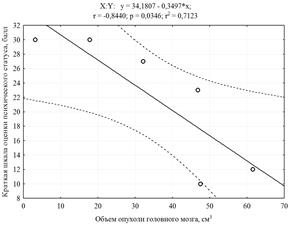
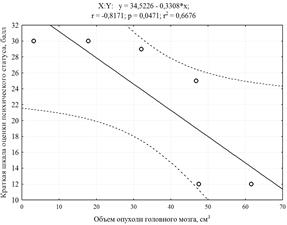
Рис. 1. Графическое представление отрицательной корреляционной связи между
объемом опухоли и балльными значениями «Краткой шкалы оценки психического статуса» пациента в предоперационном периоде (график слева) и на седьмые сутки после операции (график справа)
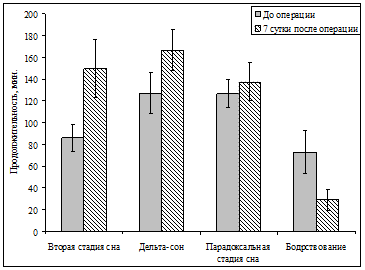
Анализ структуры ночного сна пациентов с большим объемом ОГМ (пациенты 1, 2, 3 и 5) позволили выявить сокращение латентного периода начала сна (не превышал 5 минут) и сокращение представленности его неглубоких стадий сна: вторая стадия сна у этих пациентов составила 21.5 % от общей продолжительности сна (у здоровых людей она составляет 40–50 % [8]). Установлено увеличение представленности дельта-сна до 31,6 % (в норме 20–27 %), парадоксальной стадии сна до 28,5 % (в норме 17–25 %) и времени бодрствования во время сна до 16.8 % (в норме 5 %). Сравнительный анализ продолжительности стадий сна до операции и на седьмые сутки после нее представлен на рисунке 2. Показано, что после операции выявлено значительное увеличение продолжительности второй стадии и дельта-сна (относительно общей продолжительности сна составили 30.2 % и 33.5 %, соответственно), сокращение времени бодрствования во время сна.
 _
_
Рис. 2. Продолжительность стадий сна у больных с ОГМ в дооперационном периоде и на седьмые сутки после операции. На рисунке представлены средние значения и их стандартные отклонения
Анализ ЭЭГ сна показал доминирование дельта-активности частотой 0.5–0.8 Гц с разным амплитудным градиентом на разных стадиях сна (от 46 мкВ во второй и парадоксальной стадиях – до 350 мкВ в дельта-сне) как до удаления опухоли, так и на седьмые сутки после операции. В дооперационном периоде на всех стадиях сна была отмечена амплитудная асимметрия в диапазонах дельта- и тета-активности с доминированием по амплитуде в полушарии контралатеральном локализации опухоли, а на седьмые сутки после операции – наоборот, в полушарии локализации опухоли.
Анализ ЭЭГ бодрствования до сна с закрытыми глазами показал доминирование альфа-ритма в затылочных областях. В области локализации опухоли регистрировали полиморфную дельта-активность частотой 2.0-4.0 Гц. Была отмечена выраженная амплитудная асимметрия в диапазонах дельта-, тета- и альфа-активности, отражавшаяся в повышении на 30–59 % амплитуды соответствующих ритмических составляющих в полушарии, пораженном опухолью. Асимметрия сохранялась и на седьмые сутки после удаления опухоли.
По данным литературы [1] при доброкачественных опухолях, например, при астроцитомах, медленные волны нешироко отмечаются по коре больших полушарий, выраженность медленных диффузных волн может варьировать по амплитуде и распространенности, однако степень их представленности ниже, чем при злокачественных опухолях. Регистрируются относительно сохранные нормальные регионарные различия корковых биопотенциалов: сохраняются доминирование альфа-ритма в задних отделах полушарий и наличие бета-ритма в лобных и прецентральных областях. В области очага выражены полиморфные дельта-волны частотой 2-4 Гц, амплитудой 40–100 мкВ, амплитуда альфа-ритма в этой зоне снижена по сравнению с другими областями. В областях мозга, непораженных опухолью, дельта-волны обычно меньшей амплитуды и перемежаются с сохранным альфа- и бета-ритмом. Опухоли больших полушарий характеризуются выраженностью межполушарной асимметрии (70–80 %), наличием очага патологической активности, в которой преобладают дельта-волны, особенно на стороне опухоли, на фоне сравнительно негрубых общемозговых изменений [1].
Выявленные нами особенности ЭЭГ бодрствования и сна соответствуют литературным данным об изменениях биоэлектрической активности мозга, пораженного опухолью. Эти изменения являются достаточно устойчивыми в послеоперационном периоде и могут быть связаны с длительностью процесса восстановления либо с необратимостью мозговых изменений, обусловленных опухолевой патологией, что требует дальнейшего исследования. Выявленное смещение большей амплитудной асимметрии в полушарие локализации опухоли в послеоперационный период может свидетельствовать об общем снижении электрогенеза в области операции.
Таким образом, первичная опухоль головного мозга (астроцитома) играет существенную роль в патогенезе нарушений когнитивных функций, в пользу чего свидетельствуют частные случаи их восстановления после хирургического вмешательства. Когнитивные нарушения у этих пациентов сочетаются с отклонениями в биоэлектрической активности мозга в цикле сон-бодрствование, проявляющиеся доминированием в ЭЭГ дельта-ритма и его большей амплитудой в контралатеральной области локализации опухоли. В послеоперационный период в ЭЭГ бодрствования вышеописанные феномены сохраняются, тогда как в ЭЭГ сна большая амплитудная асимметрия смещается в полушарие локализации опухоли. Выявлены нарушения в организации структуры ночного сна с некоторым их восстановлением в послеоперационном периоде.
Библиографическая ссылка
Арапова Ю.Ю., Росторгуев Э.Е., Кузнецова Н.С., Протасова Т.П., Вербицкий Е.В., Шихлярова А.И. ОЦЕНКА ОРГАНИЗАЦИИ БОДРСТВОВАНИЯ И СНА У ПАЦИЕНТОВ С ПЕРВИЧНОЙ ОПУХОЛЬЮ ГОЛОВНОГО МОЗГА // Современные проблемы науки и образования. 2016. № 4. ;URL: https://science-education.ru/en/article/view?id=25006 (дата обращения: 17.05.2026).



