Scientific journal
Modern problems of science and education
ISSN 2070-7428
"Перечень" ВАК
ИФ РИНЦ = 0,936
INTERACTION EFFECTOR IMMUNOCYTES ORAL MUCOSA UNDER PROSTHETICS PROSTHETIC CONTAINING WHITE GOLD
Актуальность. Отсутствие данных о взаимодействии ортопедических конструкций с организмом человека и реакции на них макрофагальной системы не способствует созданию высокоэффективных способов профилактики и терапии развивающихся осложнений при использовании в ортопедии сплавов металлов [1; 3; 6; 12; 15]. В научной литературе практически отсутствуют данные о реакции эффекторных иммуноцитов на воздействие ортопедических конструкций из сплавов белого золота [9]. Разнообразие и сложность клинической картины заболеваний слизистой оболочки полости рта в ответ на воздействие ортопедических конструкций из сплавов даже благородных металлов диктует проведение научных исследований для решения вопросов о причинах морфологических и клинических проявлений токсичности металлов. По данным Лебеденко И.Ю. (2001), индивидуальная непереносимость зубных протезов, изготовленных из различных материалов, наблюдается в 15-43% случаев. В связи с отсутствием достаточно чувствительных объективных методов исследования, позволяющих доказать наличие коррозии металлов в агрессивной среде полости рта, такой диагноз основывали на клинической картине и измерении микротоков [14]. При наличии яркой клинической картины непереносимости зубных протезов практически отсутствуют характерные морфологические критерии повреждения элементов слизистой оболочки полости рта, что свидетельствует о дистантном воздействии конструкций, подвергающихся коррозии, и, соответственно, высокой актуальности проводимого исследования [2; 7]. Актуальность выполняемой работы также связана с отсутствием данных о выделении группы риска категорий больных, нуждающихся в протезировании ортопедическими конструкциями из сплавов золота. До настоящего времени эта проблема полностью не решена, что значительно осложняет практическую работу врача-стоматолога. Выяснение причин непереносимости зубных протезов по-прежнему представляет трудности, поскольку комплексного обследования больных этой категории обычно не проводят [10]. В настоящее время отсутствует многофакторный подход к диагностике, дифференциальной диагностике, лечению и профилактике заболеваний, вызванных материалами зубных протезов, что свидетельствует о высокой актуальности проводимых в этом направлении исследований. Несмотря на появление новых технологий и внедрение в практику протезирования зубов новых видов безметалловой керамики, протезирование золотыми коронками считается одним из лучших, так как керамические конструкции по износостойкости сильно уступают золотым протезам.
В связи с этим целью нашей работы является установление особенностей реакций иммунного гомеостаза слизистой оболочки полости рта на ортопедические конструкции из сплавов золота с лигатурами из различных драгоценных металлов.
Материал и методы исследования
Клинические исследования. Обследованы 68 пациентов мужского пола (для исключения влияния гормональных циркадных ритмов) в возрасте от 20 до 75 лет.
Группу контроля составили 8 мужчин в возрасте от 20 до 25 лет, без сопутствующей патологии, с локальной адентией в ранние сроки после травмы. При клиническом осмотре использовали индекс гигиены полости рта Силнес–Лое, индекс подвижности зубов Миллера, индекс кровоточивости десен Мюллемана с целью определения степени выраженности воспалительных явлений в пародонте. Регистрировали наличие очагов гиперемии, отечности протезного ложа и слизистой оболочки полости рта. Для оценки состояния тканей пародонта использовали пробу Шиллера–Писарева. Весь спектр клинических обследований слизистой оболочки полости рта проводился в динамике - в процессе установки ортопедических конструкций различного химического состава с последующим цитологическим мониторингом клеточных элементов в ротовой жидкости.
Все пациенты были условно разделены на группы, с учётом возрастной классификации периодизации Г. Крайга: ранняя взрослость – 20–39 лет, средняя взрослость – 40–59 лет, поздняя взрослость – 60 лет и более; по классификации зубных рядов на основе локализации и характеру дефектов в соответствии с классификацией Е.И. Гаврилова; а также по характеру и степени атрофии беззубых челюстей в соответствии с классификациями Келлера и Шредера (рис. 1; табл. 1).
Таблица 1
Распределение материала по группам
|
Возраст по Крайгу |
20-39 |
40-59 |
60 и более лет |
|
|
контроль |
группа исследования |
|||
|
Количество пациентов |
8 |
12 |
31 |
25 |
|
Итого: |
8 |
68 |
||
|
Дефекты зубных рядов |
1,2+0,01 |
4,2+0,09 |
6,5+0,31 |
7,8+0,17 |
|
Степень атрофии челюстей |
1180 |
1200 |
1220 |
1260 и более |
Распределение пациентов по возрастным группам отображено на рис. 1.
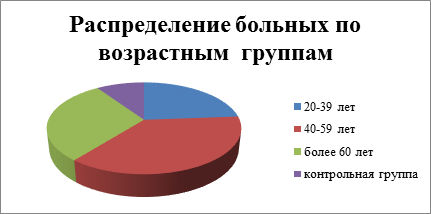
Рис. 1. Распределение пациентов по возрастным группам
Использовались ортопедические конструкции из сплавов на основе благородных металлов - Супер ТЗ (Голхадент), который содержит 75% золота и применяется для изготовления цельнолитых и штампованных коронок, а также сплав «Суперпал», который содержит 60% палладия и 10% золота, применяемый для изготовления литых протезов с полимерной и керамической облицовкой (табл. 2).
Таблица 2
Распределение материала по виду установленных ортопедических конструкций
|
Виды ортопедических конструкций |
||||
|
На основе сплавов золота |
68 |
|||
|
Супер ТЗ (Голхадент) |
3 |
11 |
14 |
10 |
|
сплав «Суперпал» |
5 |
7 |
15 |
11 |
|
Общее количество пациентов |
8 |
18 |
29 |
21 |
|
Установка на собственные зубы или импланты |
3/5 |
7/11 |
15/14 |
6/15 |
Критериями исключения являлись возраст меньше 18 и более 85 лет; расстройства психики, эндокринные и онкологические заболевания; системные заболевания в стадии декомпенсации, хронические заболевания слизистой оболочки полости рта.
Все пациенты обследованы согласно протоколу с заполнением медицинской карты стоматологического больного формы № 043/у.
Для морфологического исследования по клиническим показаниям иссекались фрагменты слизистой оболочки десны объемом 1 мм3. Забор материала производился как после хирургического удаления зубов, так и в динамике установки ортопедических конструкций на импланты. Всего изучено 96 биопсий.
Основным методом морфологического исследования явилось иммуногистохимическое фенотипирование на основе кластеров дифференцировки (Cluster of Differentiation – CD) клеток Лангерганса (СD68+), интерстициальных макрофагов (СD163+), T-лимфоцитов (СD4+/СD8+). Интенсивность пролиферативных процессов в эпителиальной пластинке оценивалась по митотическому индексу посредством маркера Ki-67: количество митозов на 100 клеток. Аргентофильные белки, ассоциированные с областью ядрышкового организатора, ответственны за активизацию и контроль транскрипции рибосомных генов в клетке, поэтому количественные параметры аргентофилии ядрышка отражают пролиферативную активность клеток. Отличительным свойством этих белков является их способность выявляться методом окрашивания гистологических препаратов 50% AgNO3.
Иммуноморфологическое исследование проводили в лаборатории патоморфологии университета г. Ниигата (Япония) и в Международном медицинском научно-образовательном центре (IMERC, Ниигата, Япония). Кроме этого, при анализе биопсий использовалась рутинная методика окраски гематоксилином и эозином.
Изучение гистологических срезов осуществлялось с помощью микроскопа Olympus BX52 с оригинальным программным обеспечением для морфометрии.
Статистическая обработка материала проведена с применением методов вариационной статистики.
Результаты исследования и их обсуждение. Многолетние наблюдения показали, что металлические конструкции из сплавов любых металлов подвергаются воздействию эффекторных клеток макрофагального звена, поступающего в зону протезного ложа из микроциркуляторного русла окружающей импланты и ортопедические конструкции соединительной ткани слизистой оболочки. Отмечено, что поверхности конструкций из мягких металлов фрагментируются быстрее, а твердые – медленнее, но подобный процесс все равно имеет место, о чем свидетельствуют частицы металла, найденные в тканях вокруг имплантированного никелид-титана [4; 5]. Данные научных исследований о воздействии сплавов золота на организм человека противоречивы и содержат сведения как о положительном их влиянии, так и отрицательном [8; 13]. Известно, что соединения золота стимулируют эндотелиальную систему и продукцию антител, а также обладают химиотерапевтической активностью в отношении гемолитического стрептококка [11]. В то же время препараты золота высокотоксичны, что ограничивает их терапевтическое применение, однако их назначают при ревматическом полиартрите. Учитывая, что золото входит в состав золотых сплавов и припоев для зубных протезов, а также их свойство проникать на значительные расстояния в твердые и мягкие ткани полости рта (ионы золота и меди — маргинально, цинк — в твердые ткани), в ортопедической стоматологии используют воздействие золота и серебра как одновременно и противовоспалительного средства.
На основании результатов морфологического исследования биоптатов слизистой оболочки протезного ложа пациентов контрольной группы и пациентов с устанавливаемыми ортопедическими конструкциями из сплавов золота была составлена модель, характеризующая состояние локального иммунного гомеостаза до начала ортопедического лечения (табл. 3, рис. 2).
Таблица 3
Показатели иммунного гомеостаза слизистой оболочки протезного ложа в исследуемых группах пациентов до начала ортопедического лечения
|
Возраст, лет |
Кол-во клеток в поле зрения (M±m) |
Суммарная площадь ЯОР, мкм2 в поле зрения |
||||||
|
CD4+/8+ |
CD68 |
CD163 |
CD34 |
МИ по активности Ki67(на 100 клеток) |
Апоптоз кератиноцитов (на 100 клеток) |
|||
|
20–39 |
1,45±0,07 |
1,78±0,09 |
1,74±0,13 |
0 |
5,89±0,33 |
4, 79±0,26 |
5,68±0,17 |
|
|
40–59 |
1,45±0,15 |
1,93±0,12 |
2,67±0,17 |
5,89±0,27 |
5,61±0,49 |
6,55±0,38 |
4,01±0,28 |
|
|
60 и более |
1,22±0,14 |
1,25±0,23 |
2,02±0,12 |
10,47±1,12 |
4,56±0,21 |
5,68±0,34 |
2,52±0,26 |
|
|
Контроль 20-25 лет |
1,17±0,12 |
0,98±0,14 |
1,67±0,08 |
0 |
2,49±0,75 |
3, 89±0,25 |
5,79±0,41 |
|
* (p<0,01).
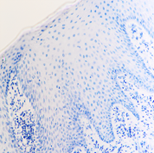 а
а 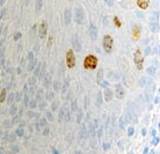 б
б 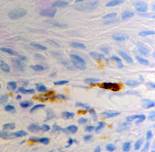 в
в
Рис. 2. Слизистая оболочка в зоне протезного ложа до установки ортопедических конструкций: а) окраска гематоксилином; б, в - локализация Ki67, CD68 соответственно
Данные таблиц были преобразованы в диаграммы, соотносящие количественные показатели к единице площади срезов СОПР (рис. 3).
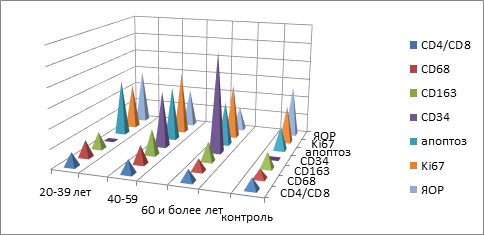
Рис. 3. Показатели иммунного гомеостаза (ИГ) слизистой оболочки рта в контрольной и исследуемых группах до начала ортопедического лечения
В результате хирургического удаления зубов и подготовки протезного ложа к установке ортопедических конструкций анализ образцов биоптатов, исследованных на содержание эффекторных иммунокомпетентных клеток, показал увеличение количества антигенпрезентирующих клеток CD68, фагоцитарного звена иммуноцитов CD163. Пролиферативная активность кератиноцитов статистически достоверно повышалась в период после хирургического лечения. После завершения реституции кератиноцитами раневой поверхности показатели пролиферативной активности снижались (р<0,01) (табл. 4, рис. 4).
Таблица 4
Показатели иммунного гомеостаза слизистой оболочки протезного ложа в исследуемых группах пациентов после ортопедического лечения
|
Возраст, лет |
Кол-во клеток в поле зрения (M±m) |
Суммарная площадь ЯОР, мкм2 в поле зрения |
||||||
|
CD4+/8+ |
CD68 |
CD163 |
CD34 (по локализации в эндотелии сосудов) |
МИ по активности Ki67 (на 100 клеток) |
Апоптоз кератиноцитов (на 100 клеток) |
|||
|
20–39 |
3,14±0,21 |
2,99±0,23 |
4,01±0,27 |
4,05±0,29 |
8,91±0,55 |
4,02±0,36 |
7,98±0,44 |
|
|
40–59 |
2,23±0,21 |
2,77±0,19 |
2,85±0,17 |
4,85±0,36 |
8,29±0,38 |
3,89±0,30 |
5,62±0,47 |
|
|
60 и более |
1,65±0,09 |
1,99±0,12 |
2,94±0,20 |
9,65±0,39 |
5,88±0,28 |
4,67±0,36 |
3,88±0,31 |
|
|
Контроль 20-25 лет |
2,43±0,25 |
2,05±0,08 |
2,54±0,19 |
1,38±0,07 |
3,39±0,26 |
4, 17±0,23 |
6,44±0,49 |
|
* (p<0,01).
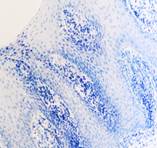 а
а 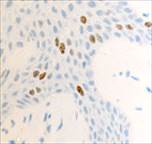 б
б 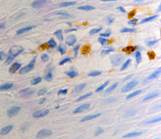 в
в
Рис. 4. Слизистая оболочка в зоне протезного ложа после установки ортопедических конструкций из сплавов белого золота: а) окраска гематоксилином; б, в - локализация Ki67, CD68 соответственно
Данные таблиц были преобразованы в диаграммы, соотносящие количественные показатели к единице площади срезов СОПР (рис. 5).
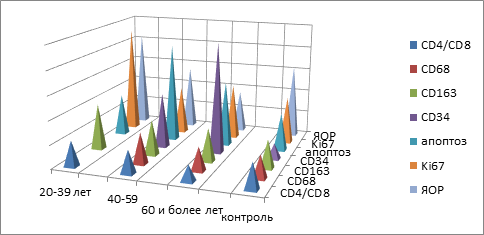
Рис. 5. Показатели иммунного гомеостаза (ИГ) слизистой оболочки рта в контрольной и исследуемых группах после ортопедического лечения с применением ортопедических конструкций из сплавов белого золота
Сравнительный анализ реакции эффекторных иммуноцитов на ортопедические конструкции из сплавов благородных металлов показал наименьшее изменение показателей иммунного гомеостаза при применении супер ТЗ (Голхадент), который содержит 75% золота и применяется для изготовления цельнолитых и штампованных коронок по отношению к сплаву «Суперпал», в котором содержится 60% палладия, 10% золота, применяющийся для изготовления литых протезов с полимерной и керамической облицовкой (p<0,05). Это является косвенным свидетельством более быстрого изнашивания конструкций из этого сплава не только за счёт стирания, но и включения механизмов отторжения инородных материалов.
Частицы металлических поверхностей, соприкасающихся со слизистой рта, поглощаются макрофагами, секретирующими химические вещества, вследствие инфильтрации которыми собственной пластинки слизистой развиваются отек и боль. Постоянное воспаление стимулирует разрушение костной ткани находящимися рядом с имплантатом клетками, а потеря кости увеличивает вероятность расшатывания импланта и необходимости повторной операции по его замене.
Тканевой ответ на протезирование, как комплекс физиологических и патологических реакций организма на внедрение инородного тела, обычно включает в себя воспаление, которое реализуется через фагоцитарные реакции, образование слившихся многоядерных макрофагов. В эксперименте доказана возможность лимфоцитов влиять на потенциал макрофагов к адгезии на поверхности имплантатов, но эти данные не подтвердились в клинических тестах [11]. Следует отметить, что макрофаги и их слившиеся многоядерные формы также могут экспрессировать множество клеточных релизов во время контакта с поверхностью инородных тел. Вместе с этим показана индукция секреции провоспалительных сигналов мононуклеарами периферической крови после контактирования с некоторыми материалами in vivo, но эти контакты не связаны с поликлональной стимуляцией CD4+ Т-клеток.
Коллагеназы и другие ферменты, разрушающие коллаген, вызывают истончение тканей, являющееся следствием деградации протеогликанов и коллагена посредством активных протеиназ, что ведёт к необходимости замены ортопедических конструкций в более короткие сроки.
Заключение. В настоящее время в России существует необходимость создания новых
материалов для стоматологии в связи с тем, что на рынке медицинских изделий предлагаются только те, которые по своим характеристикам часто не удовлетворяют требованиям, предъявляемым для медицинских ортопедических конструкций и имплантов, когда необходима не быстрая деградация, а длительное присутствие в организме без активации реакций отторжения. На основании вышеизложенного можно сделать заключение, что чем инертнее поверхность конструкций для тканей организма, тем в меньшей степени они будут активировать ответ макрофагов. Чем прочнее имплант фиксирован собственной капсулой, тем в меньшей степени он травмирует окружающие ткани во время смещения. Целесообразен дальнейший поиск максимально инертных материалов, достаточно устойчивых к механическому стиранию и к разрушению эффекторными иммуноцитами, к которым толерантны нормальные ткани организма [4].
Работа выполнена при поддержке научного фонда ДВФУ, в рамках государственного задания 2014/36 от 03.02.2014 г. и Международного гранта ДВФУ (соглашение № 13-09-0602-м от 6 ноября 2013 г.).
Библиографическая ссылка
Ким А.Р., Рева И.В., Одинцова И.А., Бочаров В.С., Толмачёв В.Е., Гульков А.Н., Рева Г.В. ВЗАИМОДЕЙСТВИЕ ЭФФЕКТОРНЫХ ИММУНОЦИТОВ СЛИЗИСТОЙ ОБОЛОЧКИ РТА В УСЛОВИЯХ ПРОТЕЗИРОВАНИЯ ОРТОПЕДИЧЕСКИМИ КОНСТРУКЦИЯМИ, СОДЕРЖАЩИМИ БЕЛОЕ ЗОЛОТО // Современные проблемы науки и образования. 2016. № 3. ;URL: https://science-education.ru/en/article/view?id=24840 (дата обращения: 17.05.2026).
DOI: https://doi.org/10.17513/spno.24840



