Scientific journal
Modern problems of science and education
ISSN 2070-7428
"Перечень" ВАК
ИФ РИНЦ = 0,936
PATHOPHYSIOLOGICAL ASSESSMENT OF DYNAMICS OF REPARATIVE PROCESSES OF BONE TISSUE WHEN EXPOSED TO PHYSICAL FACTORS
Многочисленными экспериментальными и клиническими исследованиями [2; 5; 10] доказана возможность оптимизации процессов репаративной регенерации костной ткани с помощью лазерного излучения в красном и инфракрасном (ИК) диапазоне. Установлено, что низкоинтенсивное лазерное излучение является фактором, регулирующим рост и структурную организацию костной ткани [3; 9]. Большая часть исследований, связанных с низкоинтенсивной лазерной стимуляцией остеорепарации, выполнена на длинных трубчатых костях [4; 8]. Последние научные исследования в данной области свидетельствуют об определенном интересе, проявляемом к возможностям, которые предоставляет использование импульсного излучения полупроводникового лазера инфракрасного спектрального диапазона высокого уровня мощности (ПЛИКВУМ) при лечении переломов нижней челюсти [7; 14]. Нижняя челюсть обладает органоспецифическими особенностями, отличающими ее от длинных трубчатых костей [1; 17]. Патофизиологические процессы перестройки губчатого и компактного костных компонентов нижней челюсти при травме и плановых оперативных вмешательствах интересны не только травматологам и челюстно-лицевым хирургам, но и стоматологам-имплантологам [6; 11]. В последнее десятилетие стоматологическая имплантология стала междисциплинарным направлением медицинской науки, собравшим проблемы не только хирургической и ортопедической стоматологии, но и биологии, физиологии, медицинского материаловедения и биотехнологий [12; 15]. Данное направление позволило значительно расширить показания к применению несъемных ортопедических конструкций, в том числе на нижней челюсти [13; 16]. Однако в современной литературе научных работ, отражающих особенности заживления переломов нижней челюсти или процессов регенерации костной ткани нижней челюсти после дентальной имплантации под действием ПЛИКВУМ, нами не обнаружено, что и стало предопределяющим фактором к разработке данного научного направления.
Цель исследования - морфологическое изучение динамики формирования регенерата в области перелома нижней челюсти под действием импульсного излучения полупроводникового лазера инфракрасного спектрального диапазона высокого уровня мощности.
Материалы и методы исследования. Эксперименты проводили на 26 половозрелых кроликах породы «Серый Великан» массой 2-2,5 кг. Животных содержали в обычных условиях вивария на привычном для них пищевом рационе. Под внутримышечным тиопенталовым наркозом и местной анестезией в асептических условиях моделировали типичный перелом нижней челюсти в области ее угла. Костные отломки репонировали и фиксировали проволочными швами. В зависимости от метода лечения всех животных разделили на 3 группы: 12 кроликов 1-й группы служили контролем, во 2-й и 3-й опытных группах также взято по 12 животных. Кроликам опытных групп на 2-е сутки после операции проводили лазеротерапию ИК-лазером «Интрадонт» с выходной мощностью 20 Вт, с длиной волны 0,9±0,01 мкм и длительностью импульса лазерного излучения 100±50 нс (2-я группа) и ИК-лазером «Интрадонт» с выходной мощностью 40 Вт, с длиной волны 1,9±0,02 мкм и длительностью импульса лазерного излучения 250±50 нс (3-я группа). Экспозиция во второй и третьей группах составляла 20 минут 3 раза в сутки с интервалом 8 часов ежедневно, до момента выведения кроликов из эксперимента. Контрольных и подопытных животных выводили из опыта введением в ушную вену воздуха через 3, 7, 10, 15, 21, 28 и 35 суток.
Оперированную половину нижней челюсти освобождали от мягких тканей и выпиливали блоки, которые фиксировали в 10%-ном растворе забуференного формалина. Декальцинацию производили в трилоне-Б. Блоки заливали в парафин и готовили серийные срезы, которые окрашивали гематоксилином и эозином, по Маллори и по Ван Гизону. Помимо изучения качественных характеристик регенерата, определяли количественные его показатели с помощью морфометрии. Для проведения количественного анализа использовали метод точечного счета. При увеличении микроскопа в 400 раз с помощью окулярной стереометрической сетки Автандилова Г.Г. на поперечном срезе биоптата определяли количество остеобластов, остеокластов и лимфоцитов. Использованы результаты оценок 40 случайных наложений окулярной сетки, имеющей 100 тест-точек. Учитывали только те клетки, которые соприкасались с тест-точками сетки. Полученный экспериментальный материал обработан методами вариационной статистики с использованием t-критерия Стьюдента с помощью пакета программ медицинской статистики Microsoft Excel.
Результаты исследования и их обсуждение. Как показал анализ экспериментальных исследований, в раннем посттравматическом периоде при качественной оценке регенерата у животных опытных и контрольной групп не выявлялось существенных различий. Так, спустя 3 суток после травмы превалировали деструктивно-некротические процессы. В зоне перелома нижней челюсти определялись фрагменты кости, обрывки мягких тканей, между которыми видны эритроциты, скопления лимфоцитов и нейтрофильных лейкоцитов. Мелкие кровеносные сосуды расширены, в них наблюдался стаз. По краю костных отломков встречались единичные остеокласты. Элементы периоста и эндоста находились в состоянии пролиферации. В периостальной и межотломковой зонах малодифференцированная соединительная ткань, которая представлена малодифференцированными клетками и молодыми коллагеновыми волокнами. Однако при количественном изучении клеточного состава у животных, подвергнутых воздействию ПЛИКВУМ, наблюдалось увеличенное содержание остеобластов.
Морфометрическая оценка активности репаративного остеогенеза (М±m)
|
Сутки |
Группы животных |
||||||||
|
1 |
2 |
3 |
1 |
2 |
3 |
1 |
2 |
3 |
|
|
лимфоциты |
остеобласты |
остеокласты |
|||||||
|
3 |
0,4±0,2 |
0,9±0,5 |
0,7±0,4 |
7,5±1,8 |
18,0±8,3* |
40,5±12,6* |
0,6±0,4 |
0,6±0,3 |
0,6±0,1 |
|
7 |
1,2±0,5 |
0,6±0,4 |
0,7±0,5 |
26,4±5,6 |
23,5±9,4 |
41,5±10,5 |
0,7±0,6 |
0,4±0,4 |
0,5±0,3 |
|
10 |
0,7±0,2 |
0,7±0,4 |
0,7±0,3 |
29,0±7,2** |
28,3±11,2* |
31,9±8,4 |
0,4±0,3 |
0,5±0,3 |
0,3±0,2 |
|
15 |
0,9±0,3 |
0,3±0,2 |
0,5±0,3 |
14,7±2,4 |
19,0±7,9* |
18,5±7,2 |
0,6±0,3 |
0,4±0,3 |
0,4±0,3 |
|
21 |
0,7±0,3 |
0,4±0,3 |
0,6±0,4 |
30,5±7,8** |
23,0±8,6 |
23,0±9,8* |
0,4±0,2 |
0,3±0,2 |
0,3±0,2 |
|
28 |
0,6±0,2 |
0,4±0,2 |
0,3±0,3 |
12,0±2,6** |
17,0±8,8 |
16,3±6,9 |
0,2±0,1 |
0,3±0,2 |
0,3±0,2 |
|
35 |
0,2±0,2 |
0,5±0,4 |
0,5±0,4 |
10,7±2,2* |
23,0±10,1 |
45,5±14,1* |
0,1±0,1 |
0,3±0,2 |
0,4±0,3 |
Примечание: * - достоверность различий по сравнению с группой контроля;
** - достоверность показателей по сравнению с исходными данными
Причем этот показатель у кроликов 2-й группы превышал контрольный в 2 раза, а у животных 3-й группы - более чем в 5 раз (различие статистически достоверно, р<0,05). Количество лимфоцитов и остеокластов у животных всех групп являлось приблизительно одинаковым. Через 7 дней отмечалась активизация пластических реакций, в результате чего происходило очищение костной раны и заполнение дефекта нижней челюсти формирующимся регенератом. Наибольшая пролиферативная активность в этот срок отмечалась у животных, подвергнутых воздействию ПЛИКВУМ.
На 10-е сутки наблюдения изменялись как качественные характеристики, так и количественные показатели регенерата у кроликов опытной и контрольных серий. У животных 1-й и 2-й групп в этот период преобладали пролиферативные явления. Количество остеобластов по сравнению с исходным заметно увеличивалось. Напротив, у животных 3-й группы число остеобластов имело тенденцию к уменьшению. На основании этого можно предположить, что в условиях стимуляции ПЛИКВУМ происходит более быстрая дифференцировка остеобластов в остеоциты. Образование первичной костной мозоли у кроликов 3-й группы происходило быстрее, нежели у животных 1-й и 2-й групп. На 15-е сутки у животных контрольной группы отмечалась частичная консолидация переломов. В костной мозоли, соединяющей отломки нижней челюсти, хорошо видны часто встречающиеся балочки, не связанные между собой и окруженные слоем остеобластов (рис. а).
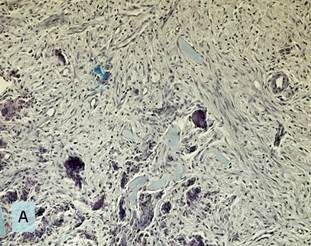
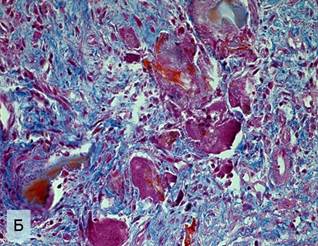
Микропрепараты. Морфологическая картина в зоне перелома нижней челюсти через 15 суток (а) и 21 (б) сутки после начала эксперимента.
а – формирующаяся костная мозоль, видны не связанные между собой костные балочки.
Окраска гематоксилином и эозином. Ок. 10, об. 20;
б – энхондральное окостенение. Окраска по Маллори. Ок. 10, об. 20
В балочках определялись равноудаленные линии роста кости. Межбалочные пространства заполнены малодифференцированной соединительной тканью, в которой наблюдались кровеносные сосуды различного диаметра. Кое-где в зоне перелома встречались участки новообразованной хрящевой ткани. Следует отметить, что, начиная с 15-х суток и до конца наблюдения, у животных контрольной группы отмечалось постепенное уменьшение бластных клеток в регенерате. У кроликов, подвергнутых воздействию ПЛИКВУМ, периоды снижения активности остеобластов чередовались с периодами усиленной их пролиферации (15-е и 21-е сутки).
Спустя 21 день у всех животных в костной ране преобладали продуктивные костеобразовательные процессы, в результате которых формировалась и перестраивалась первичная костная мозоль (рис. б). Под влиянием ПЛИКВУМ отчетливо активизировалось образование остеоидных балок. Так, у кроликов 3-й группы через 28 суток в регенерате, представленном широкими связанными между собой костными балочками, имелось большое количество активных бластных элементов.
Консолидация переломов нижней челюсти у животных контрольной группы наблюдалась в среднем на 4-7 дней позднее, чем у животных 2-й и 3-й групп. Обобщая результаты морфологических исследований, сопоставляя качественные и количественные характеристики регенерата у контрольных и подопытных животных, удалось выявить стимулирующее действие излучения полупроводникового лазера инфракрасного спектрального диапазона высокого уровня мощности на репаративную регенерацию костной ткани, которое отчетливо проявлялось в период пролиферации и дифференцировки остеогенных клеточных элементов.
Заключение. Таким образом, под влиянием излучения полупроводникового лазера инфракрасного спектрального диапазона высокого уровня мощности (3-я группа) улучшались условия течения репаративного остеогенеза и сокращались сроки заживления переломов нижней челюсти у экспериментальных животных. Воздействие низкоинтенсивного лазерного излучения (2-я группа) в раннем посттравматическом периоде приводило к усилению пролиферативной активности и более быстрой дифференцировке остеобластов в остеоциты. В условиях воздействия ПЛИКВУМ выявлены особенности течения репаративной регенерации костной ткани - периоды стихания активности остеобластов чередовались с периодами усиленной их пролиферации. Более выраженное стимулирующее действие отмечено в третьей группе, где использовалось излучение полупроводникового лазера инфракрасного спектрального диапазона высокого уровня мощности.
Библиографическая ссылка
Кошель И.В., Щетинин Е.В., Сирак С.В., Гатило Ю.Ю. ПАТОФИЗИОЛОГИЧЕСКАЯ ОЦЕНКА ДИНАМИКИ РЕПАРАТИВНЫХ ПРОЦЕССОВ КОСТНОЙ ТКАНИ ПРИ ВОЗДЕЙСТВИИ ФИЗИЧЕСКИХ ФАКТОРОВ // Современные проблемы науки и образования. 2016. № 3. ;URL: https://science-education.ru/en/article/view?id=24523 (дата обращения: 17.05.2026).



