Scientific journal
Modern problems of science and education
ISSN 2070-7428
"Перечень" ВАК
ИФ РИНЦ = 0,936
EXPERIMENTAL TREATMENT OF DEEP CARIES AND ACUTE FOCAL PULPITIS: PATHOPHYSIOLOGICAL AND HISTOLOGICAL ASPECTS
Изучение механизмов репарации пульпы зубов остается актуальной проблемой регенеративной медицины [2,4]. Несмотря на избыток предложений на стоматологическом рынке лечебных прокладочных материалов отечественных и зарубежных фирм, используемых при лечении глубокого кариеса и острого очагового пульпита, частота осложнений в первые 6 месяцев после лечения глубокого кариеса достигает 32 %, а после лечения острого очагового пульпита 84 % [1,3]. Это связано с неадекватной оценкой состояния твердых структур дентина, отсутствием знаний о механизмах репарации при выборе фармакологических средств для лечения, а также нарушениями технологии их применения [5,9]. Несмотря на особенности строения, специфичность локализации и функции пульпы, ряд авторов рассматривают процесс воспаления с позиций, соответствующих общим патофизиологическим и морфологическим закономерностям развития патологических процессов в других структурах организма человека. Характер воспаления, его течение, динамика развития обычно тесно связаны, обусловливаются разными уровнями реактивности организма и протекают преимущественно с проявлениями, в которых превалируют процессы экссудации, альтерации или пролиферации [6,7]. Рассматривая физиологические и патофизиологические свойства пульпы с общих позиций, характерных для всей соединительной ткани организма, следует упомянуть о некоторых ее особенностях, влияющих на течение возникающего патологического процесса. Пульпа в отличие от других тканей не покрыта эпителием и находится в замкнутом образовании из дентина, поэтому одновременно пульпе присуща специфическая функция, которая свойственна только ей – дентинообразование [8,11]. Такая функциональная анатомия обеспечивается комплексом защитно-приспособительных механизмов пульпы, что обусловливает особенности и характер течения воспалительных процессов. Повышение эффективности лечения патологии пульпы зубов невозможно без разработки, синтеза и создания специфических лечебных прокладочных материалов, обладающих изученными в эксперименте полипотентными свойствами [10,15]. Существующие композиции лекарственных прокладочных материалов в основном обладают однонаправленным действием и применяются либо для реминерализации дентина, либо для купирования начальных форм воспаления, и лишь незначительная часть из них способна многофакторно воздействовать как на структуру дентина, так и на компоненты пульпы [14]. Многие вопросы, несмотря на значительный интерес к изучению изменений в твердых тканях и пульпе на стадиях дезинтеграции при глубоком кариесе и остром очаговом пульпите, касающиеся механизмов развития патологии, и особенно адекватного выбора лекарственных средств и их эффективности в процессе лечения, остаются на сегодняшний день не выясненными [12, 13]. В этой связи представляется интересным и полезным экспериментально-морфологическое исследование влияния на структуры надпульпарного дентина и компоненты коронковой пульпы разработанной лекарственной пасты для лечения глубокого кариеса и острого очагового пульпита.
Цель исследования. Патофизиологическая оценка реакции пульпы зуба на использование разработанной пасты при экспериментальном пульпите.
Материал и методы исследования. Экспериментальное исследование выполнено в соответствии с Директивой 2010/63/EU Европейского парламента и совета европейского союза по охране животных, используемых в научных целях. Объектом для экспериментальных исследований служили 8 беспородных клинически здоровых собак в возрасте от 2 до 5 лет, весом от 4 до 8 кг, находящихся в обычных условиях вивария. Эксперимент выполнен под внутривенным наркозом (ксилазина гидрохлорид, Rometar®), по типу острого опыта. Формирование глубоких полостей проводили по общепринятым нормам твердосплавными борами на щечной поверхности со скоростью вращения 30000 об/мин с охлаждением физраствором. Затем вскрывали полость зуба и обнажали поверхность пульпы экскаваторами. Лечение смоделированных поражений глубоких слоев дентина и поверхностных слоев пульпы проводили с применением разработанной комбинированной лечебной пасты.
Материал у экспериментальных животных забирали через 7, 14 суток, 1, 3 и 6 месяцев. Зубы удаляли щипцами, иногда выпиливали блоки под наркозом вместе с фрагментами челюстей. Полученные образцы фиксировали в 10 % нейтральном забуференном формалине, а затем подвергали медленной деминерализации в 10 % растворе азотной кислоты. Проводку и заливку материала осуществляли с использованием гистологического процессора замкнутого типа Tissue-Tek VIP™ 5 Jr и станции парафиновой заливки Tissue-Tek® TEC™ 5 фирмы Sakura (Япония). Из полученных блоков делали гистологические срезы толщиной 5 – 7 мкм, которые окрашивали гематоксилином и эозином, альциановым синим, по Ван-Гизон, Акимченко, а также проводили серебрение по Mallori. Морфометрические исследования проводили с использованием программы Видео-Тест-Морфология 5.1 для Windows.
Растровую электронную микроскопию (РЭМ) проводили на аппарате JEOL серии JSM-6510 с разрешением в режиме высокого вакуума 3.0 нм (30 кВ), 8.0 нм (3 кВ), 15.0 нм (1 кВ). Полученный экспериментальный материал обработан методами вариационной статистики с использованием t-критерия Стьюдента с помощью пакета программ медицинской статистики Microsoft Excel.
Результаты и обсуждение. Лечение глубокого кариеса в эксперименте с помощью разработанной лекарственной композиции достаточно в короткие сроки приводило к существенным изменениям основных параметров построения надпульпарных слоев дентина. Однако обращает на себя внимание организация плотной консистенции лечебной прокладки. Микроскопически лечебная паста не везде плотно прилегает к дентину, образуя небольшие щелевые пространства. Уже к 7 суткам по ходу дентинных трубочек четко прослеживается погружение мелкозернистого вещества на глубину до 30–40 мкм. По площади объекта эта субстанция имеет различную плотность, что обусловлено двумя факторами: содержимым дентинных трубочек и перераспределением внутритканевого давления в них под действием лечебной прокладки. К 14 суткам эксперимента наблюдаемые явления усиливаются. Мелкозернистое вещество определяется на 60–70 мкм от поверхности дентина. По всей наблюдаемой площади объектов входы в дентинные трубочки облитерированы. Ближе к пульпе удается выявить сужение дентинных трубочек до 2,14±0,42 - 1,86±0,40 мкм.
Через 1 месяц в зоне контакта с лечебной пастой выражены признаки усиления рисунка перитубулярных и межтубулярных участков основного вещества дентина, за счет увеличения минеральной фазы. Ближе к пульпе подобных изменений в основном веществе дентина не обнаружено, вместе с тем в стенках дентинных трубочек адсорбировано большое количество мелкозернистого вещества. Через 1–3 месяца дентинные трубочки в большей своей массе плотно облитерированы мелкозернистым и аморфным веществом на глубину до 60–80 мкм. Изменения на поверхности околопульпарного дентина удается выявить через 1 месяц от начала эксперимента. На поверхности дентина формируются плотно прилегающие участки основного вещества в виде очагов. 3 месяцам большая часть околопульпарной поверхности дентина покрыта вновь сформированным слоем основного вещества, содержащего волокнистые структуры, мелкозернистую и аморфную субстанции. Толщина слоя составляет 18,36±1,20 - 34,12±0,84 мкм (рисунок 1).

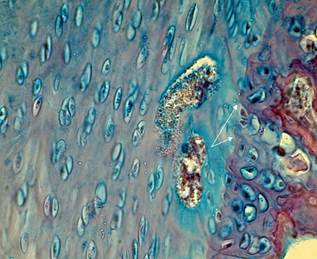
Рис. 1. Микропрепараты. Пограничная линия предентина с отростками одонтобластов. Окраска по Акимченко. Ув. х300. Справа – формирование слоя заместительного дентина с неравномерным распределением входов в дентинные канальцы. Окраска альциановым синим. Ув. х300
По архитектонике построения сформированный слой заместительного дентина существенно уступает строению в норме. Прежде всего, отличие выражено неравномерным распределением входов в дентинные трубочки и не систематически ориентированными волокнистыми структурами.
Через 6 месяцев заместительный слой дентина существенно расширяется и утолщается до 28,14+0,86-44,42±1,04 мкм. Увеличивается плотность расположения волокнистых структур. В зоне верхушки корня, рядом с апикальным отверстием в периодонтальной связке обнаружены фрагменты (тельца) цемента в виде крупных конгломератов. Одни из них шарообразной формы, другие вытянутые, в виде шипов. Вокруг каждого фрагмента была сформирована соединительнотканная капсула, которая имеет плотное сращение с фрагментом. Сами фрагменты содержат крупные тела цементоцитов (рисунок 2). Данная особенность характерна для локального гиперцементоза, а фрагменты – это цементикли, которые построены из цементобластов. Появление цементиклей, по-видимому, связано с чрезмерной нагрузкой на перицемент при жевании.
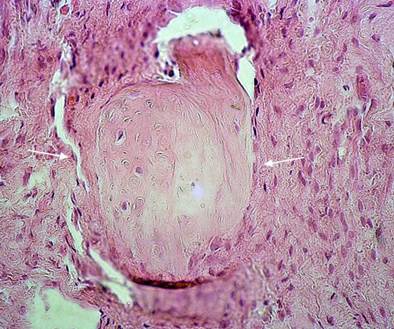
Рис.2. Микропрепарат. Пристеночный дентикль в пульпе зуба (отмечен стрелками). Окраска гематоксилином и эозином. Ок. 15, об. 40
Местами на поверхности основного вещества просматриваются участки мелкозернистой субстанции. Форма и размеры дентинных трубочек приближаются к нормальным, но плотность их расположения по поверхности уступает строению в норме.
При лечении острого очагового пульпита в ближайшие сроки эксперимента реакция пульпы характеризовалась признаками типичными для термомеханических факторов препарирования надпульпарных слоев дентина. К 14 суткам удавалось наблюдать усиление компенсаторных явлений, в отличие от других серий эксперимента. В первую очередь, четко прослеживалась нормализация в строении капилляров пульпы, особенно центрального и промежуточного слоев (рисунок 3).

Рис. 3. Микропрепарат. Нормализация строения капилляров пульпы центрального и промежуточного слоев. Окраска по Массону. Ок. 20, об. 100
В субодонтобластическом слое отек основного вещества мало выражен. Количество лейкоцитов снижено до 8,04+0,82 - 11,42±0,86 количества полей в поле зрения (10х12). Одновременно установлено увеличение количества малодифференцированных клеток, тяготеющих формировать слой до 36,74±1,86 - 44,56±1,84 (8х12). Увеличено количество фибробластов, прилегающих в виде тяжей к слою малодифференцированных клеток. Соотношение волокнистых структур к клеточным элементам и основному веществу составило пропорцию 32,12±0,44 - 36,82±0,76 %, что существенно лучше предыдущих серий эксперимента с применением других композиций.
К 1 месяцу эксперимента в слое одонтобластов определялась нормализация строения. Морфологических дефектов, микропор или щелевых образований вдоль формирующегося слоя дентина не установлено. Через 3–6 месяцев в строении периферического и центрального слоев пульпы изменений в строении, отличающих их от нормы, не обнаружено. В этой связи, можно утверждать, что в структурах пульпы и ее нервных элементах изменения носили функциональный характер, что выражалось в активации реактивных и восстановительных процессов с сохранением жизнеспособности пульпы. Гистологическая картина этих изменений проявилась в оптимизации воспалительного процесса с повышением уровня обменных реакций с выраженной активацией клеточных элементов пульпы и нормализацией их метаболизма. Таким образом, полученные экспериментальные результаты свидетельствуют об интенсификации дентиногенеза при применении разработанной лекарственной поликомпонентной композиции с ускоренным восстановлением свойств надпульпарного дентина и коронковой пульпы.
Заключение. Таким образом, установлено, что разработанная лекарственная паста для лечения глубокого кариеса и прямого покрытия пульпы при лечении острого очагового пульпита обладает полипотентными свойствами в отношении предупреждения осложнений воспаления и усиления защитных свойств пульпы. Проведенная оценка применения разработанной комбинированной лекарственной композиции показала быструю реструктуризацию надпульпарных слоев дентина. В сроки 7–14 суток – купирование воспалительной реакции, нормализацию основных компонентов пульпы и значительную активизацию ее дентиногенетической функции.
Библиографическая ссылка
Кобылкина Т.Л., Сирак А.Г. ЭКСПЕРИМЕНТАЛЬНОЕ ЛЕЧЕНИЕ ГЛУБОКОГО КАРИЕСА И ОСТРОГО ОЧАГОВОГО ПУЛЬПИТА: ПАТОФИЗИОЛОГИЧЕСКИЕ И ГИСТОЛОГИЧЕСКИЕ АСПЕКТЫ // Современные проблемы науки и образования. 2016. № 2. ;URL: https://science-education.ru/en/article/view?id=24333 (дата обращения: 17.05.2026).



