Scientific journal
Modern problems of science and education
ISSN 2070-7428
"Перечень" ВАК
ИФ РИНЦ = 0,936
PROGNOSTIC VALUE OF HEMOCOAGULATION TESTS IN PATIENTS WITH SEVERE BURNS
Ожоговая болезнь продолжает привлекать внимание патофизиологов и клиницистов, что обусловлено высокой частотой термических повреждений, тяжестью медицинских и социальных последствий. Число умерших пациентов на разных стадиях ожоговой болезни продолжает оставаться стабильно высоким, занимая одно из первых мест среди всех больных хирургического профиля [6].
Термическое воздействие на ткани с распространённым поражением поверхности тела вызывает у пострадавшего шок с последующим формированием комплекса компенсаторно-приспособительных процессов, которые зачастую приобретают патологический характер и создают условия для развития угрожающих жизни осложнений [4, 5]. Известно, что основными участниками экстренной и отсроченной регуляции постоянства внутренней среды организма при различных критических состояниях являются нервные, иммунные и гемостатические компоненты гомеостаза. Нарушение гемокоагуляционного баланса крови и развитие ДВС-синдрома вносят существенный вклад в развитие синдрома полиорганной недостаточности, который возникает у 30–50 % тяжелообожженных, до 80–90 % из которых погибают в различные периоды ожоговой болезни [1, 8].
Важнейшей задачей является оценка риска развития ДВС-синдрома у пациентов с термической травмой в каждом конкретном случае, возможность своевременно и адекватно его предупреждать, а при возникновении – купировать [2, 3, 7]. Однако до сих пор нет единого мнения об объективных критериях прогнозирования риска ДВС-синдрома у пациентов с тяжелыми термическими поражениями. Дальнейшее изучение и уточнение изменений в системе гемостаза, как важнейших факторов ДВС-синдрома и, как следствие, синдрома полиорганной недостаточности при ожоговой травме, является одним из актуальных и перспективных направлений в комбустиологии.
Целью исследования является анализ динамики показателей свертывающей и антикоагулянтно-фибринолитической активности плазмы крови в зависимости от исхода ожоговой болезни.
Объекты и методы исследования. В основу работы положен анализ обследования 37 мужчин с ожогами кожных покровов IIIБ-IV степени тяжести, в возрасте от 21 до 45 лет, находившихся на лечении в ГУЗ «Городская клиническая больница № 7» г. Саратова. Все пациенты разделены на две группы в зависимости от исхода ожоговой болезни. В I группу вошли 26 пациентов, выживших после термической травмы, средний возраст которых составил 37,3 года. Во II группу включили 11 пациентов, умерших на фоне ожоговой болезни, средний возраст – 40,8 лет. Во II группе 4 тяжелообожженных умерли в течение первой недели, 4 пострадавших – во вторую неделю, 3 пациента – на третьей неделе. Группу сравнения (К) составили 25 мужчин без ожоговых поражений, средний возраст – 36,5 лет.
Пострадавшие получали стандартное лечение в соответствии со степенью тяжести термической травмы. Всем пациентам проводилось определение протромбинового времени (ПВ), активированного частичного тромбопластинового времени (АЧТВ), тромбинового времени (ТВ), концентрации фибриногена, определение растворимых фибринмономерных комплексов (РФМК), активности антитромбина-III (АТ-III) и XIIа-зависимого фибринолиза (XIIа-ЗФ). Исследование проводилось на 1-е, 3-и, 7-е, 14-е и на 21-е сутки после ожога.
Результаты и их обсуждение. При поступлении в стационар у тяжелообожженных отмечались различные изменения в системе гемостаза в зависимости от исхода заболевания.
В группе выживших после термической травмы на 1-е, 3-и и 21-е сутки нахождения в стационаре не выявили достоверного изменения активности плазменных факторов свертывания крови по сравнению с группой сравнения. Только на 7-е и 14-е сутки после получения ожога отмечалось удлинение протромбиного времени, что свидетельствует о снижении активности факторов внешнего пути свертывания крови (p<0,05) (табл. 1).
Таблица 1
Показатели плазменного звена системы гемостаза у тяжелообожженных (I, II гр.) и лиц группы сравнения (К) (M+m)
|
Показатели |
Группы |
1-е сутки |
3-и сутки |
7-е сутки |
14-е сутки |
21-е сутки |
|
ПВ (сек) |
I |
95,2+2,55 |
93,5+2,42 |
76,6+1,27* |
81,6+1,55* |
88,7+1,42 |
|
II |
78,0+1,39*0 |
66,3+1,46*0 |
60,4+2,36* |
35,7+1,18*0 |
33,3+1,24*0 |
|
|
К |
92,7+0,93 |
|||||
|
АЧТВ (сек) |
I |
31,0+1,39 |
34,7+1,27 |
28,3+1,22 |
30,8+1,15 |
31,7+0,37 |
|
II |
41,5+1,72*0 |
56,3+1,42*0 |
47,9+1,37*0 |
51,8+1,75*0 |
77,7+1,61*0 |
|
|
К |
29,3+0,55 |
|||||
|
ТВ (сек) |
I |
17,2+0,65 |
16,6+0,42 |
17,6+0,22 |
16,5+0,72 |
17,4+0,93 |
|
II |
19,0+2,05*0 |
22,3+1,37*0 |
22,9+1,65*0 |
28,4+1,42*0 |
35,3+1,79*0 |
|
|
К |
16,8+0,86 |
|||||
Примечание: К – группа сравнения.
* – p<0,05 – достоверность по отношению к данным группы сравнения.
0 – p<0,05 – достоверность по отношению к данным I группы.
АЧТВ-тест, характеризующий активность факторов внутреннего пути свертывания крови, и ТВ-тест, отражающий конечные этапы свертывания крови, на протяжении всего исследования не имели достоверных отличий от значений в группе сравнения. Подобная динамика показателей коагулограммы пациентов, выживших после тяжелой ожоговой травмы, является адекватной реакцией системы гемостаза в ответ на проводимое лечение, включающее антикоагулянтные препараты.
В группе пациентов, умерших после получения термической травмы, показатели свертывающей системы характеризовались резким снижением активности плазменных факторовкак внешнего, так и внутреннего пути свертывания крови (табл. 1). Средняя величина ПВ в 1-е сутки после получения термической травмы по сравнению с показателями в группе сравнения снизилась на 14,7 %, АЧТВ – на 41,8 %, ТВ – на 13,1 %. При дальнейшем развитии ожоговой болезни выявилось нарастающее угнетение всех факторов свертывания, особенно выраженное непосредственно перед смертью. В последний день жизни тяжелообожженных среднее значение ПВ удлинилось до 24,4+1,06 сек, АЧТВ – до 65,2+2,37 сек, ТВ – до 31,2+1,53 сек, что значительно превышает данные показатели в группе сравнения (p<0,05). Степень нарастающего дефицита плазменных факторов свертывания крови у пациентов II группы отражает глубину гемостазиологических нарушений и тяжесть развивающегося ДВС-синдрома.
Показатели концентрации фибриногена и РФМК были различными у обожженных в группах I и II в различные периоды болезни и имели достоверное отличие в каждой группе от показателя лиц группы сравнения (p<0,05) (табл. 2).
Таблица 2
Концентрация фибриногена и РФМК у тяжелообожженных (I, II гр.) и лиц группы сравнения (К) (M+m)
|
Показа-тели |
Группы |
1-е сутки |
3-и сутки |
7-е сутки |
14-е сутки |
21-е сутки |
|
Фибри-ноген (г/л) |
I |
3,4+0,66 |
4,6+1,01* |
4,9+0,99* |
4,5+0,75* |
3,6+0,71 |
|
II |
5,4+1,22*0 |
4,7+1,36*0 |
4,2+1,14*0 |
2,9+1,66*0 |
2,4+0,45*0 |
|
|
К |
3,2+0,64 |
|||||
|
РФМК (мг/л х10-9) |
I |
95,5+8,77* |
186,4+12,84* |
200,3+13,52* |
175,2+11,69* |
111,8+11,34* |
|
II |
131+9,23*0 |
222+13,65*0 |
240+12,92*0 |
270+13,37*0 |
282+13,83*0 |
|
|
К |
0 |
|||||
Примечание: К – группа сравнения.
* – p<0,05 – достоверность по отношению к данным группы сравнения.
0 – p<0,05 – достоверность по отношению к данным I группы.
В плазме здоровых людей (К) гиперфибриногенемия и растворимые фибринмономерные комплексы отсутствовали, но определялись в разные сроки в плазме крови у пациентов в обеих группах, пострадавших от ожога. У пациентов I группы в 1-е сутки после получения травмы среднее значение концентрации фибриногена в плазме было стабильным и статистически значимо не отличалось от группы сравнения (M+m=3,4+0,66 г/л против 3,2+0,64 г/л). В дальнейшем содержание фибриногена сначала увеличивалось, достигая максимума к 7-м суткам, составляя в среднем 4,9+0,99 г/л, затем снижалось к 14-м суткам и возвращалось к исходному значению на 21-е сутки после получения термической травмы. Гиперфибриногенемия, незначительно возрастающая в течение первых двух недель после получения ожога, объясняется развитием умеренного воспалительного ответа на термическую травму. Отсутствие гиперфибриногенемии в более поздние стадии ожоговой болезни свидетельствует об адекватном характере защитно-приспособительных реакций организма и меньшем риске возникновений осложнений, угрожающих жизни.
Динамика содержания в плазме крови продуктов паракоагуляции на протяжении периода наблюдения также указывает на благоприятное течение ожоговой болезни у лиц I группы. В группе выздоровевших пациентов концентрация РФМК в первые сутки достигала в среднем 95,0 мг/л, затем постепенно нарастала на 7-e сутки до 200,0 мг/л и возвращалась к исходному уровню к 21-м суткам нахождения в стационаре. Среднее значение содержания РФМК у данных пациентов на протяжении всего времени нахождения в стационаре составило 134,3+12,83 мг/л.
У пациентов II группы уровень фибриногена в ранний период после травмы был статистически значимо повышен, составляя в среднем 5,4+1,22 г/л, но снижался в более поздние сроки и особенно выраженно (в 1,5–2 раза) непосредственно перед смертью (табл. 2). Подобная динамика фибриногена на фоне дефицита плазменных факторов свертывания крови свидетельствует о высоком риске развития диссеминированного внутрисосудистого свертывания крови. Кроме того, тяжелообожженные II группы в 1-е сутки после получения травмы имели уровень РФМК на 40 % выше, чем пострадавшие первой группы (р>0,05). В последующие сутки отмечали динамическое нарастание содержания продуктов паракоагуляции с максимальными значениями этого показателя непосредственно перед смертью. Средняя концентрация РФМК составила 248,0+13,56 мг/л. Нарастание концентрации фибринмономерных комплексов свидетельствует о расширении пула фибриногена и активации внутрисосудистого свертывания крови. Фибринмономерные комплексы блокируют ряд плазменных факторов, чем и объясняется у данных пациентов тенденция к снижению концентрации фибриногена и угнетение как внешнего, так и внутреннего путей свертывания крови.
Нами проведен анализ изменений показателей антикоагулянтной и фибринолитической активности плазмы крови у здоровых людей и ожоговых пациентов (рис. 1, 2).
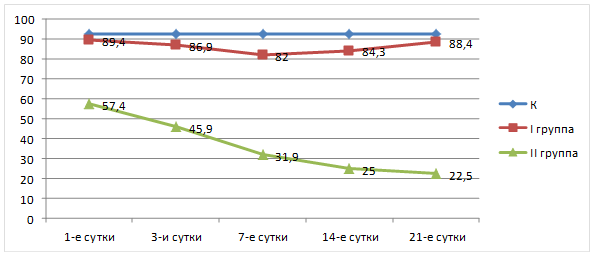
Рис. 1. Изменение активности антитромбина-III (%) у тяжелообожженных (I, II гр.) и лиц группы сравнения (К)
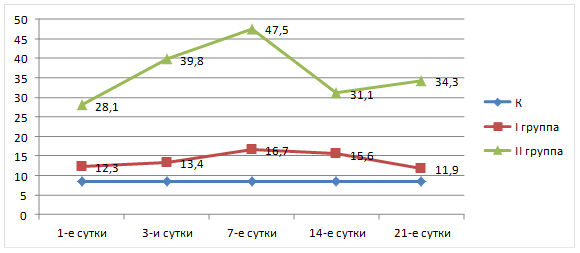
Рис. 2. Изменение времени XIIа-зависимого фибринолиза (мин) тяжелообожженных (I, II гр.) и лиц группы сравнения (К)
При исследовании антикоагулянтной и фибринолитической активности плазмы крови нами получены результаты с достоверным отличием показателей умерших пациентов от результатов людей в группах сравнения (К) и выживших после термической травмы (I группа). В плазме здоровых людей активность АТ-III составила в среднем 92,4+8,75 %, время XIIа-зависимого фибринолиза – 8,5+2,13 мин.
При сравнении результатов тяжелообожженных I группы с показателями группы сравнения угнетение фибринолитической способности и незначительное снижение активности АТ-III ниже 80 % (до 77,2 %) отметили только в 50 % наблюдений. У половины пациентов на 3-и сутки наблюдения выявили ускорение времени эуглобулинового фибринолиза более чем на 30 % и возвращение к исходным показателям на 14-е и 21-е сутки. Время фибринолиза статистически значимо увеличивалось только на 7-е сутки наблюдения (M+m=16,7+4,5 мин), возвращаясь к исходным значениям на 21-е сутки наблюдения. Активность АТ-III в этой группе сохранялась на исходном уровне на протяжении всего периода наблюдения и не имела достоверного отличия от группы сравнения (p<0,05).
Анализ показателей противосвертывающего механизма системы гемостаза у погибших пациентов выявил выраженный дефицит АТ-III и плазминогена, являющего пусковым фактором эуглобулинового фибринолиза (p<0,05). В 1-е сутки после термической травмы у всех пациентов активность основного эндогенного антикоагулянта снижалась на 35 %, а время XIIа-ЗФ увеличивалось более чем в три раза (M+m=28,1+3,8 мин), по сравнению с группой сравнения (К). При последующих исследованиях зафиксировано дальнейшее нарастание антитромбиновой и фибринолитической недостаточности, с максимальным их дефицитом перед смертью. В последний день жизни пациентов среднее значение АТ-III составило 21,6+3,28 %, время XIIа-ЗФ – 39,22+7,64 мин. Продолжающееся падение активности АТ-III у пациентов, вероятно, связано с развитием ДВС-синдрома, а увеличение времени лизиса эуглобулинового сгустка свидетельствует о нарушении согласованности работы различных механизмов системы гемостаза [2, 4, 8]. Как известно, одним из звеньев патогенеза ДВС-синдрома является образование микросгустков крови и блокада микроциркуляции в органах-мишенях (мозг, надпочечники, почки, печень, желудок и кишечник) с развитием дистрофических и деструктивных нарушений в них, которые, вероятно, и приводят к синдрому полиорганной недостаточности.
Заключение. Таким образом, сравнительное исследование системы гемостаза у тяжелообожженных пациентов позволило установить зависимость исхода ожоговой болезни от выраженности и динамики изменений показателей системы гемостаза. У пациентов с благоприятным исходом ожоговой болезни в период ожогового шока выявилось умеренное повышение концентрации фибриногена и продуктов паракоагуляции, с тенденцией к нарастанию изменений к 7–10 суткам после получения травмы при сохранении активности АТ-III на уровне не менее 70 % на всем протяжении заболевания. В группе пациентов с летальным исходом уже в ранний период ожоговой болезни выявлялась значительная гиперфибриногенемия, сменяющаяся выраженной тенденцией к снижению концентрации фибриногена, дефицит АТ-III и глубокое угнетение фибринолиза. Снижение активности АТ-III менее 70 % и трехкратное увеличение времени XIIа-зависимого фибринолиза на фоне дефицита плазменных факторов свертывания крови является, по нашему мнению, прогностическим предиктором развития жизненно опасных осложнений в системе гемостаза при ожоговой болезни.
Библиографическая ссылка
Иваненко И. Л., Гладилин Г. П., Шулаева Н. М., Островский Н. В., Никитина В. В., Веретенников С. И., Калинычева А. Е. ПРОГНОСТИЧЕСКОЕ ЗНАЧЕНИЕ ГЕМОКОАГУЛЯЦИОННЫХ ТЕСТОВ У ПАЦИЕНТОВ С ТЯЖЕЛЫМИ ОЖОГАМИ // Современные проблемы науки и образования. 2016. № 2. ;URL: https://science-education.ru/en/article/view?id=24154 (дата обращения: 22.05.2026).



