В последние годы антибиотикорезистентность микроорганизмов стала актуальной проблемой мирового значения. Всемирная Организация Здравоохранения (ВОЗ) работает в тесном сотрудничестве с Всемирной организацией по охране здоровья животных (МЭБ), Продовольственной и сельскохозяйственной организацией ООН (ФАО) над усовершенствованием методов борьбы с резистентностью к противомикробным препаратам, в том числе – над оптимальным использованием антибиотиков. ВОЗ разработала проект глобального плана действий по борьбе с устойчивостью микроорганизмов к противомикробным средствам [9].
В связи с этим всё более интенсивно изучают антимикробные белки и пептиды (АМР), которые рассматривают, как альтернативу традиционно используемым антибиотикам. Многие из АМР являются важнейшим звеном врождённого иммунитета макроорганизмов. Поэтому в процессе коэволюции бактериальных патогенов и их хозяев у ряда микробов выработалась способность противодействовать некоторым АМР. Один из перспективных подходов для преодоления такого противодействия - использование в качестве лекарственных средств не одного, а сразу нескольких АМР, что значительно уменьшает вероятность развития резистентности. В связи с этим расширяются исследования антимикробной активности природных комплексов, содержащих АМР. Одним из таких комплексов является секрет слюнных клеток медицинской пиявки Hirudo medicinalis (ССК МП), основной гуморальный агент, обеспечивающий высокую эффективность лечения пиявками – гирудотерапии (ГТ). ГТ оказывает многофакторное антикоагулирующее, тромболитическое, противоишемическое, антимикробное, иммуностимулирующее, восстанавливающее микроциркуляцию действие, и ряд других эффектов. Установлено, что в состав ССК МП входит более сотни белков (ферменты, ингибиторы протеиназ, модуляторы, АМР, а также ещё не описанные белки и пептиды) и более 150 низкомолекулярных соединений. Одним из важных и достаточно хорошо изученных компонентов ССК является АМР дестабилаза-лизоцим (Д-Л). Причём, в ССК обычно содержится несколько изоформ Д-Л, лизоцимы других типов, другие литические ферменты. Получены также данные о множестве новых белков в составе ССК [1, 5]
Проведённое нами ранее сравнение антимикробной активности растворов рекомбинантного Д-Л и ССК МП показало более высокую активность последнего, а также более широкий спектр его антимикробного действия [1, 7]. Такие работы имеют большую значимость и в связи с доказанной ролью многих микроорганизмов в развитии атеросклероза сосудов [10]. Исследования антимикробной активности ССК МП, проведённые на первом этапе in vitro, актуальны для получения конкретных данных о влиянии ССК на микроорганизмы, играющие ключевую роль при развитии ряда заболеваний, они необходимы для лечения этих заболеваний с привлечением ГТ. Кроме того, важно сравнительное изучение антимикробного эффекта растворов ССК и водного экстракта из орального лекарственного препарата «Пиявит», который разрешён к клиническому применению с 1994 г. Этот препарат на основе МП содержит все компоненты ССК, практически полностью сохраняющие свои активности при продолжительном хранении. В настоящее время регистрационный номер «Пиявита» P N000363/02 от 22.05.2008. Производится этот препарат ООО Научно-внедренческой фирмой «Гируд И.Н.», в г. Балаково Саратовской области [1].
В качестве тест-микроорганизмов при изучении антимикробной активности растворов ССК МП и водного экстракта «Пиявита» мы использовали условно-патогенных представителей грибов и бактерий - Candida guillermondii и Pseudomonas aeruginosa, а также бактерию Aeromonas hydrophila . Инвазивные штаммы синегнойной палочки вызывают инфекционные заболевания – псевдомонозы (аэромонозы), а также часто осложняют многие патологические процессы инфекционной и неинфекционной этиологии. Ряд представителей р. Aeromonas признаны факультативными патогенами для людей с ослабленным иммунитетом. Бактерия Aeromonas hydrophila subsp. hydrophila известна, как симбионт медицинской пиявки. Грамотрицательные бактерии Aeromonas spp. и Pseudomonas spp. имеют много сходных признаков, в том числе, у них выявлена широкая резистентность к антибиотикам, тяжёлым металлам, и др. Для некоторых грамотрицательных бактерий установлена резистентность и к AMP [6].
Представители р. Candida являются наиболее распространенными грибными патогенами, способными вызывать серьезные системные заболевания у людей с ослабленным иммунитетом, перенёсших операции, принимающих антибиотики широкого спектра действия. Около половины таких заболеваний вызывает Candida albicans, однако, растёт распространенность заболеваний, вызываемых и другими представителями этого рода. Например, среди возбудителей онихомикоза всё чаще встречается и C. guillermondii [8].
Поэтому изучение чувствительности P. aeruginosa и A. hydrophila, а также C. guillermondii к антибиотическому действию ССК МП и лекарственного препарата «Пиявит», содержащих комплексы AMP, является весьма актуальной задачей.
Цель исследования
Целью настоящей работы явилось изучение in vitro антибиотического влияния на микроорганизмы растворов ССК МП и водного экстракта из орального лекарственного препарата «Пиявит».
Задачи работы:
1) определить величину антибиотического действия растворов ССК МП и водного экстракта «Пиявита» на условно патогенные микроорганизмы с помощью метода диффузии в агар и контроля жизнеспособности клеток после воздействия на них изучаемых антимикробных агентов;
2) исследовать с помощью СЭМ и ТЭМ картину лизиса микробных клеток, чувствительных к влиянию растворов ССК МП и водного экстракта «Пиявита».
Материал и методы исследования
Отбирали нативный, свободный от примесей, ССК от МП H. medicinalis ранее описанным методом, для чего использовали по 20 особей МП, выращенных на биофабрике и купленных в аптеке. Для получения водного экстракта из препарата «Пиявит» суспензию (без капсул) этого препарата хорошо перемешивали, настаивали 3 часа в стерильной дистиллированной воде при комнатной температуре, затем центрифугировали при 11 тыс. об./мин. в течение 15 мин., использовали супернатант. Концентрацию белка в растворах определяли по известному методу Брэдфорд.
Работу проводили с культурами P.aeruginosa шт. 47, C. guillermondii шт. 327 из Музея культур кафедры микробиологии МГУ им. М.В. Ломоносова (MDMSU), а также A. hydrophila subsp. hydrophila шт. 8 из Музея культур Научно- исследовательского инновационного центра микробиологии и биотехнологии ФГБОУ ВО «Ульяновская ГСХА им. П.А. Столыпина».
Бактерий выращивали при 37о С в течение суток на агаризованной питательной среде следующего состава: K2HPO4 – 7,0; KH2PO4 – 2,0; цитрат натрия - 0,4; MgSO4 - 0,05; (NH4)2SO4 – 1,0; H2O дист.; pH 7,1. К среде добавляли 10 г/л триптозного бульона и 10 г/л глюкозы; а также 15 г/л высокоочищенного агара («Sigma, или «Difco», США). Дрожжи выращивали на агаризованной среде Чапека. На этих же средах определяли антимикробную активность изучаемых растворов с известной концентрацией белков методом диффузии в агар, учитывая размер зоны подавления роста тест-культуры от конца лунки. Минимальную ингибирующую концентрацию (МИК) растворов определяли путем учета антибиотических активностей ряда разведений. МИК выражали в мкг/мл раствора белка, внесенного в лунку. Жизнеспособность микроорганизмов определяли известным способом путём подсчёта колоний, выросших из сохранивших жизнеспособность клеток после влияния на них изучаемых растворов [4]. Статистическую обработку полученных результатов проводили с использованием программ Microsoft Excel; достоверность различий p<0,05.
Подготовку тест-микроорганизмов для электронной микроскопии проводили общепринятыми методами [4]. Для исследования в просвечивающем (трансмиссионном) электронном микроскопе (ТЭМ) клетки тест-микроорганизмов (контрольные и лизирующиеся под влиянием изучаемых растворов) фиксировали 2 ч. в 0,1 М фосфатном буферном растворе, рН 7,2 с 2,5%-ным глутаровым альдегидом. Затем образцы отмывали 2 раза в этом же буфере и помещали на 3 ч. в 1%-ный раствор OsO4. После этого препараты отмывали 3 раза в 50%-ном этаноле (пока раствор не становился прозрачным). Образцы оставляли на ночь при 4ºС в 2%-ном растворе уранилацетата в 70%-ном этаноле. Проводку в спиртах заканчивали: в 80%-ном – 2 раза по 30 мин.; в 96%-ном – 1 раз 1ч.; в абсолютном спирте (100%-ном) – 1 ч. Затем обезвоживание проводили в абсолютном ацетоне – 2 раза по 30 мин. Заливку и пропитку препаратов в эпоне проводили общепринятым способом. Срезы на формваровых пленках просматривали в ТЭМ Geol 1011, (Япония) при ускоряющем напряжении 80 kV после их контрастирования уранилацетатом и реактивом Рейнольса.
Для приготовления бактериальных препаратов методом негативного контрастирования каплю суспензии клеток P.aeruginosa после их инкубации с исследуемыми растворами (в которых определена концентрация белка), а также суспензию - контроль наносили на сеточки с формваровыми пленками. Через одну минуту избыток жидкости удаляли фильтровальной бумагой. Затем наносили на сеточки каплю 2%-ного раствора фосфовольфрамовой кислоты. Через 1 мин избыток жидкости удаляли.
Препараты клеток, приготовленные этими разными способами, просматривали в трансмиссионном микроскопе Geol JEM 1011 (Япония) при ускоряющем напряжении 80 кВ, с помощью Erlangshen ES 500 W Model 782, gatan, с программой Gatan Digital Micrograph.
Для изучения в сканирующем электронном микроскопе (СЭМ) фиксацию контрольных и опытных клеточных суспензий проводили 2,5%-ным глутаровым альдегидом в течение 1 ч; после чего исследуемый материал обезвоживали в спиртах возрастающих концентраций (20%, 50%, 70% - по 30 минут, 96% - 1 час, абсолютный спирт – 1 час), а затем в абсолютном ацетоне 1 час, и высушивали в критической точке. Напыление образцов проводили платиной на приборе фирмы LKB (Швеция). Форму и поверхность исследуемого материала изучали с помощью микроскопов «JSM-6380» (Япония) и «CamScan» (Великобритания) при ускоряющем напряжении 20 кV.
Результаты исследования и их обсуждение
Ранее мы сообщили [6, 7], что бактерии A. hydrophila – симбионты кишечника H. medicinalis, оказались практически устойчивы к влиянию раствора ССК МП в используемых концентрациях (до 100 мкг/мл). Основной причиной такой устойчивости является, по-видимому, эволюционная приспособленность бактерий-симбионтов к обитанию в организме своего хозяина – МП. В настоящем исследовании мы определили влияние на этих бактерий растворов ССК и водного экстракта «Пиявита»: они проявили слабую (следы) антимикробную активность в концентрации 150 мкг/мл. Как известно, биологическая активность разных партий ССК и «Пиявита» может существенно отличаться [1, 6].
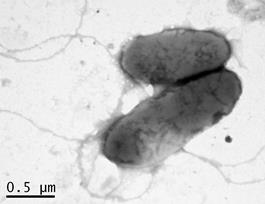
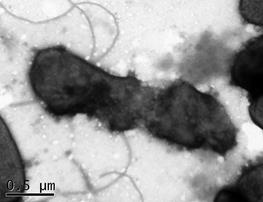
Клетки P. aeruginosa чувствительны к антибиотической активности ССК, как мы определили ранее [6]. Эти клетки лизируются и под влиянием раствора водного экстракта «Пиявита». На рис. 1 представлена картина лизиса бактерий P. aeruginosa под влиянием 35 мкг/мл (при 37о С, через 10 мин.) растворов ССК (рис. 1, б) и водного экстракта «Пиявита» (рис. 1, в). Видно, что, по сравнению с контролем (рис. 1, а), у бактерий нарушена целостность клеточной стенки и мембран. Эти клетки уже через 10 мин. лизируются под влиянием раствора ССК (рис. 1, б), хотя под влиянием раствора водного экстракта «Пиявита» за это время только незначительная часть клеток лизировалась, а у большинства клеток появились признаки изменения морфологии, увеличилось число мембранных везикул (рис. 1, в). Картина практически полного лизиса бактериальных клеток представлена на рис. 1, г.
а) б)


в) г)
Рис. 1. Вид в ТЭМ контрастированных клеток P. аeruginosa, лизирующихся под влиянием растворов ССК МП и водного экстракта «Пиявита» (50 мкг/мл, 37о С, через 10 мин.): а) – контроль; б) – лизирующаяся под влиянием ССК клетка с нарушенной целостностью клеточной стенки и мембран; в) клетка с изменённой поверхностью, увеличенным числом мембранных везикул в результате влияния раствора водного экстракта «Пиявита»; г) остатки лизировавшихся под влиянием ССК клеток.
Определение в двух разных опытах жизнеспособности клеток бактерий после действия на них изучаемых растворов одинаковой концентрации (50 мкг/мл, при 37о С) привело к результатам, представленным в табл. 1.
Таблица 1
Выживаемость клеток Pseudomonas aeruginosa после действия на них растворов ССК МП и водного экстракта «Пиявита»
|
Время действия изучаемых растворов на клетки, мин. |
% выросших колоний P. аeruginosa (по сравнению с контролем) после действия на бактериальные клетки растворов (в концентрации 50 мкг/мл): |
|
|
ССК МП |
Водного экстракта «Пиявита» |
|
|
10 |
31,5 ± 1,32 |
83,1 ± 3,87 |
|
60 |
0,8 ± 0,07 |
50,7 ± 0,31 |
|
120 |
0 |
31,5 ± 0,24 |
Из полученных данных видно, что под действием изучаемых растворов практически все клетки P. аeruginosa теряют жизнеспособность и лизируются через 1 час в инкубационной среде с ССК. Однако, за это время теряет жизнеспособность только половина клеток в инкубационной среде с водным экстрактом «Пиявита». Треть клеток бактерий сохраняют жизнеспособность и через 2 часа влияния последнего, через 3 часа инкубации количество жизнеспособных клеток уменьшается, благодаря действию раствора «Пиявита», примерно ещё вдвое (до 15 %).
Таким образом, раствор водного экстракта «Пиявита» оказывает антимикробный эффект на клетки возбудителей аэромонозов в опыте in vitro, хотя и менее интенсивно (за больший промежуток времени), чем раствор ССК МП. Следует подчеркнуть, что прямое количественное сравнение антимикробного действия изучаемых растворов мы не проводили, так как известно об отличиях биологической активности разных партий ССК, а, следовательно – и содержащего ССК препарата «Пиявит».
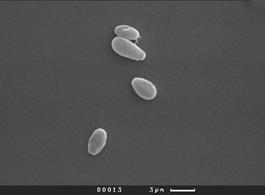
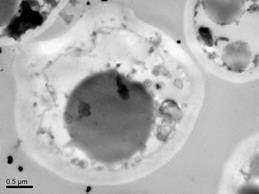
Эукариотические клетки дрожжей C. guillermondii также чувствительны к антимикробному влиянию растворов ССК МП и водного экстракта «Пиявита». Вид этих лизирующихся клеток в СЭМ и в ТЭМ представлен на рис. 2.

а) б)

в) г)

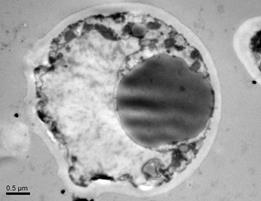
д) е)
Рис. 2. Вид в СЭМ (а, в, д) и в ТЭМ (б, г, е) клеток Candida guillermondii, лизирующихся под влиянием растворов ССК МП и водного экстракта «Пиявита» (50 мкг/мл, 37о С, через 60 мин.): а, б) - контроль; в) – cкопление, образование конгломератов, изменение формы и лизис дрожжевых клеток, остатков псевдомицелия с нарушенной поверхностью и проницаемостью мембран под влиянием раствора ССК; вид в СЭМ; г) вид в ТЭМ поперечного среза лизирующейся под влиянием раствора ССК клетки C. guillermondii: разрыхление и начало расслоения в отдельных местах клеточной стенки, отхождение от неё цитоплазматической мембраны, значительное просветление цитоплазмы за счёт потери внутренних компонентов клетки из-за нарушения проницаемости цитоплазматической мембраны; наличие в цитоплазме кольцевых мембранных апоптических структур; д) СЭМ конгломератов из клеток с нарушенной морфологией и лизирующихся под действием водного экстракта «Пиявита»; е) вид в ТЭМ поперечного среза лизирующейся под влиянием раствора водного экстракта «Пиявита» клетки C. guillermondii: начало расслоения клеточной стенки, отхождение от неё цитоплазматической мембраны, просветление цитоплазмы, появление в цитоплазме кольцевых мембранных структур.
Заключение
Таким образом, электронномикроскопическое исследование дрожжевой формы грибных клеток C. guillermondii выявило основные стадии их лизиса под влиянием изучаемых растворов. Как и в случае картины лизиса бактерий, наблюдается, прежде всего, нарушение целостности клеточных стенок – их разрежение, затем разрушение структуры этих стенок, хотя известно о существенном отличии в строении клеточных стенок грибов и бактерий [3]. Наряду с этим, выявлены также признаки нарушения проницаемости клеточной мембраны, что проявляется в просветлении цитоплазмы - её разрежении, потере клетками их содержимого, разрушении клеточной стенки и цитоплазматической мембраны.
Подсчёт среднего из 20 фото (полей зрения) в СЭМ процента лизирующихся дрожжевых клеток с нарушенной морфологией подтвердил (достоверность p<0,05), что изучаемые растворы ССК и водного экстракта «Пиявита» оказывают антибиотическое действие, приводящее к лизису дрожжей C. guillermondii (табл. 2).
Таблица 2
Процентное содержание лизирующихся под влиянием растворов ССК МП и водного экстракта «Пиявита» (50 мкг/мл, 37о С, через 60 мин.) клеток популяции дрожжей C. guillermondii
|
Раствор антимикробного комплекса |
Процент лизирующихся клеток |
|
ССК МП |
79,5 + 8,0 |
|
Водный экстракт «Пиявита»° |
65,2 + 7,7 |
Как и при изучении влияния на бактерий, мы определяли антимикробное действие разных партий изучаемых растворов, поэтому не имели возможности корректно сравнить количественно активности последних. Однако, во всех опытах клетки тест-микроорганизмов более интенсивно лизировались под влиянием ССК.
В таблице 3 представлены данные определения антибиотических активностей изучаемых растворов методом диффузии в агар.
Таблица 3
Минимальные ингибирующие концентрации растворов ССК МП и водного экстракта препарата «Пиявит»
|
Тест-микроорганизм |
МИК раствора, мкг/мл: |
|
|
|
Раствор ССК МП |
Водный экстракт «Пиявита» |
|
P. aeruginosa |
5 |
20 |
|
C. guillermondii |
15 |
45 |
Таким образом, определение in vitro антибиотического влияния растворов ССК МП и водного экстракта препарата «Пиявит» на бактерий и микроскопические грибы, способных вызывать заболевания людей и животных, показало перспективность дальнейшего изучения этих природных антимикробных комплексов с целью их использования в качестве актуальных лечебных препаратов, не вызывающих резистентности микроорганизмов. Как известно, лечение с помощью многих лекарств проводят, вначале используя их введение в кровоток (подобно ССК МП при ГТ), а затем осуществляя поддерживающую терапию оральными препаратами (подобно «Пиявиту»). При различных хронических заболеваниях (в том числе – сердечно-сосудистых), у людей со слабым иммунитетом такое лечение может способствовать не только ослаблению атеросклероза сосудов, улучшению микроциркуляции, но и подавлению ряда инфекций, в том числе - вялотекущих.
Рецензенты:
Алешкин А.В., д.б.н., главный научный сотрудник лаборатории клинический микробиологии и биотехнологии бактериофагов ФБУН «Московский научно-исследовательский институт эпидемиологии и микробиологии им. Г.Н. Габричевского» Роспотребнадзора, г. Москва;
Нафеев А.А., д.м.н., заведующий отделом особо опасных инфекций, природно-очаговых инфекций и профилактики туберкулеза ФБУЗ «Центр гигиены и эпидемиологии в Ульяновской области», г. Ульяновск.



