Scientific journal
Modern problems of science and education
ISSN 2070-7428
"Перечень" ВАК
ИФ РИНЦ = 0,936
A RESPONSE OF THE BONE TISSUE, LUNG, LIVER, AND LYMPH NODES TO BONE CEMENT IMPLANTATION INTO THE FEMUR BONE IN RATS
Цель исследования: изучить изменения костной ткани, легких, печени и лимфатических узлов при имплантации костного цемента в бедренную кость в эксперименте.
Объектом исследования служили 50 крыс линии Вистар (самцы). На наружной поверхности бедра осуществлялся доступ к диафизу бедренной кости. Выполнялась перфорация одного кортикального слоя, внутрикостно вводился метилметакрилат в дозе 0,1 мл. Фрезевое отверстие пломбировалось костным цементом. Контрольной группе животных выполнялась только перфорация одного кортикального слоя диафиза бедренной кости. Животные выводились из эксперимента через 1 час, через 1, 3, 7, 30 суток. Образцы тканей для гистологического исследования проводились по стандартной методике, окрашивались гематоксилином и эозином. С помощью стандартной сетки из 25 точек (площадь 4,9 х 10 мкм2) и при увеличении микроскопа «AxiostarZeiss» х100, х200 определялась объемная плотность альтерации костной ткани (дистрофия, некроз), некроз эндотелия, плотность воспалительных инфильтратов в легком. Фрагментация и гемолиз эритроцитов в сосудах, тромбоз в костной ткани и легком оценивалась в баллах. Для определения функционального типа лимфатического узла, его иммунной реакции определялись корково-мозговой индекс, коэффициент отношения лимфатических узелков со светлыми центрами (Л2) и без них (Л1), относительная площадь тимус-зависимых и тимус-независимых зон.
Результаты исследования
Костная ткань. При введении метилметакрилата сумма деструктивных изменений костной ткани превышала показатели в контрольной группе при всех сроках эксперимента с наибольшей объемной плотностью некрозов через 3 и 7 суток (рис.1). Фрагментация и гемолиз эритроцитов, тромбоз сосудов наблюдались через 1 и 7 суток. Регенерация костной ткани отсутствовала до конца эксперимента.
Легкие. В контроле через 1 час после операции легкие неравномерно полнокровны, наблюдаются единичные точечные кровоизлияния под висцеральной плеврой, повсеместно венозный застой (макроскопические изменения).
На 1-3-и сутки эксперимента – легкие неравномерно полнокровны, увеличивается число точечных кровоизлияний на плевре, умеренный отек. К концу 7-х суток – легкие неравномерной плотности, с мелкими, местами сливающимися кровоизлияниями под висцеральной плеврой.
К 30-м суткам – легкие неравномерно полнокровны, наблюдается умеренный отек, кровоизлияния отсутствуют. При гистологическом исследовании: в легких через 1 час – гемолиз и деформация эритроцитов в сосудах микроциркуляторного русла, некроз эндотелиальных клеток и единичные мелкие тромбы и кровоизлияния.
На 1-е сутки нарастающий венозный застой, кровоизлияния, стаз и мелкие тромбы в сосудах, гемолиз эритроцитов и некроз эндотелия во всех полях зрения (рис. 2). На 3-е сутки сохраняются расстройства кровообращения. Гемолиз эритроцитов и некроз эндотелиоцитов определяются не во всех полях зрения, но в каждом третьем поле зрения микроскопа имеется перибронхиальная и периваскулярная лимфоидная инфильтрация.
К концу 7-х суток – умеренный венозный застой, отек, умеренный стаз эритроцитов в сосудах, определяются гиалиновые тромбы в единичных сосудах, но значительное расширение площади лимфоидных инфильтратов с формированием 1- 3 аттенуированных фолликулов.
На 30-е сутки снижается отек, нет деформированных эритроцитов, гемолиза и тромбов в мелких сосудах, исчезает периваскулярная, но остается перибронхиальная лимфоидно-макрофагальная инфильтрация с единичными лимфоидными фолликулами (рис.3).
Динамика изменений в лимфатическом узле легкого: через 1 час эксперимента уменьшение площади лимфатического узла на 10%. На 3-и сутки увеличивается площадь лимфатического узла на 30% с увеличением отношения ЛУ2/ЛУ1 на 15%, свидетельствующих об активной антигенной стимуляции. К концу эксперимента показатели наибольшие: отношение ЛУ2/ЛУ1 – 5,11±0.02, что свидетельствует о присоединении иммунного компонента воспаления в легком и его хронизации.
Динамика гистологических изменений в печени: в контрольной группе отмечается острое венозное полнокровие в центре долек, умеренно выраженный отек, гидропическая дистрофия единичных клеток на периферии долек печени. Процент альтерации гепатоцитов в дольке составляет 2,3±0,77.
В эксперименте: через 1 час после операции: балочное строение печени сохранено, имеется стаз в центральных венах и умеренный отек. Количество дистрофически измененных с бледными ядрами гепатоцитов в центре и на периферии дольки приблизительно равно и не превышает 6,15 ± 1,43%.
К концу 1-х суток в центральных венах и межбалочных капиллярах сохраняется стаз, незначительно нарастает альтерация – до некроза единичных гепатоцитов.
Процент поврежденных клеток в центре и на периферии дольки увеличивается до 11,5%.
Через неделю эксперимента в печени нарастает белковая и жировая дистрофия гепатоцитов – появляются просветления, типа «песочных часов». Альтерация гепатоцитов на периферии дольки снижается до 16,24±1,05%, что свидетельствует об уменьшении токсического повреждения гепатоцитов.
На 30-е сутки в печени наблюдается стаз, гидропическая дистрофия вплоть до баллонной. В отдельных гепатоцитах в центре долек слабый стаз в портальных трактах. На месте погибших гепатоцитов определяются диссеминированные мелкие очаги из лимфоцитов, макрофагов. Процент альтерации в центральной и периферической части дольки не превышает соответственно 6±0,5% – 9±0,75% и становится ниже, чем в 1-е сутки.
Таким образом, на 3-и сутки эксперимента определяется токсическое повреждение гепатоцитов с максимальным нарастанием повреждения печени на 7-е сутки. К 30 суткам эксперимента по гистологическим и морфометрическим данным не определяется токсического повреждения печени, однако имеются очаги продуктивного гепатита.
Синхронно с регионарными лимфатическими узлами легких идет активная реакция регионарных лимфатических узлов печени, но начиная с 3-х суток эксперимента: ЛУ2 / ЛУ1 – повышается на 15%, на 7-е сутки – на 23%, на 30-е сутки – превышает контрольные показатели на 10%, что связано с сохраняющемся продуктивным воспалением на месте очагов токсического гепатита.
Обсуждение
Результаты исследований показали, что имеется сопряженная реакция легких, печени и иммунных органов – лимфатических узлов на токсическое повреждение мономером метилметакрилата. В легких через час после введения метилметакрилата первично повреждаются сосуды микроциркуляторного русла с максимальной выраженностью к концу первых суток, что может привести к массивным кровоизлияниям в легких, способствует тромбозу и объясняет интраоперационную летальность больных. Некроз эндотелиоцитов, гемолиз эритроцитов менее выражен на 3-и сутки, но появляются периваскулярные и перибронхиальные лимфоидные инфильтраты, которые особенно проявляются на 7-е сутки эксперимента, а появление лимфоидных узелков указывает на присоединившийся иммунный компонент воспаления. На 30-е сутки заканчивается токсическое повреждающее действие мономера метилметатриксата, на что указывает отсутствие периваскулярных инфильтратов, деформации и гемолиза эритроцитов в сосудах, но сохраняется, хотя и менее выраженный, иммунный компонент воспаления, что необходимо учитывать при профилактике легочных осложнений. Токсическое повреждение гепатоцитов определяется на 3-и сутки эксперимента, максимальное повреждение печени выявлено на 7-е сутки. К 30 суткам – по гистологическим и морфометрическим данным токсическое повреждение печени не выражено, однако имеются очаги продуктивного гепатита.
Морфология активной антигенной стимуляции в регионарных лимфатических узлах в конце эксперимента отражает присоединение иммунного компонента воспаления и представляет угрозу его хронизации в поврежденных органах.
В легких максимальные показатели объемной плотности некроза эндотелия отмечены через 1 и 7 суток. Деструкция эпителия, фрагментация эритроцитов и тромбоз сосудов были максимальными через 7 суток. Воспалительные инфильтраты с лимфоидными узелками сохранялись до конца эксперимента. Бедренный лимфатический узел перестраивался из фрагментированного в компактный тип с 3-х по 7-е сутки. Наибольшая антигенная стимуляция отмечена через 1 и 7 суток; резкое снижение относительной площади тимус-зависимой зоны – с 7 суток до окончания эксперимента. Синхронно изменялись и аналогичные показатели в лимфатическом узле корня легкого.
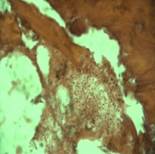
Рис. 1. Через 1 сутки костная ткань, соприкасающаяся с цементом, некротизирована и фрагментирована, костный мозг представлен некротическими тканями. Окраска гематоксилином и эозином. Х200
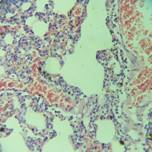
Рис. 2. В легких отек, стаз деформация эритроцитов в сосудах, деструкция эндотелия (12 час. эксперимента). Окраска гематоксилином и эозином. Х200
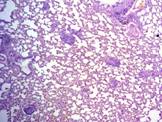
Рис. 3. 30-е сутки эксперимента. Перибронхиальные, периваскулярные воспалительные инфильтраты, формирование гранулем. Окраска гематоксилином и эозином. Х100
Заключение
Таким образом, токсическое повреждение сосудов исследуемых органов может быть источником тромбоэмболии, прогрессирующего тромбоза в легком через 1 и на 7 сутки. Повреждение печени выражено на 1-е сутки с усилением к концу первой недели. Нарушение транспортной и иммунной функций лимфатических узлов является фактором хронизации воспаления в органах. Мономер метилметакрилата резко замедляет регенерацию кости
Рецензенты:Бауэр И.В., д.м.н., зав. отделением травматологии и ортопедии Новосибирской государственной областной клинической больницы, г. Новосибирск;
Павлов В.В., д.м.н., главный научный сотрудник, руководитель отделения эндопротезирования тазобедренного сустава и осложнений ФГБУ «Новосибирский научно-исследовательский институт травматологии и ортопедии им. Я.Л.Цивьяна» Министерства здравоохранения Российской Федерации, г.Новосибирск.
Библиографическая ссылка
Прохоренко В.М., Зайдман А.М., Жуков Д.В., Прохоренко В.М., Устикова Н.В., Жукова В.А. РЕАКЦИЯ КОСТНОЙ ТКАНИ, ЛЕГКИХ, ПЕЧЕНИ И ЛИМФАТИЧЕСКИХ УЗЛОВ ПРИ ИМПЛАНТАЦИИ КОСТНОГО ЦЕМЕНТА В БЕДРЕННУЮ КОСТЬ КРЫС В ЭКСПЕРИМЕНТЕ // Современные проблемы науки и образования. 2015. № 6. ;URL: https://science-education.ru/en/article/view?id=23259 (дата обращения: 16.05.2026).



