Scientific journal
Modern problems of science and education
ISSN 2070-7428
"Перечень" ВАК
ИФ РИНЦ = 0,936
THE STRUCTURE AND MORPHOLOGICAL FEATURES OF THE CELLULAR ENVIRONMENT IN BREAST TISSUE IN WOMEN OF REPRODUCTIVE AGE
Многие вопросы патоморфологии доброкачественных заболеваний молочных желез остаются нерешенными, а в последние годы приобретают особенную актуальность. Это связано с неуклонным ростом онкологической патологии молочных желез, которая занимает лидирующее положение как в структуре онкологической заболеваемости, так и по показателям смертности среди женского населения [2,5,7]. Результаты многих клинико-эпидемиологических исследований показали, что доброкачественные гиперпластические процессы являются наиболее распространенной патологией, на фоне которой могут развиваться злокачественные опухоли [8,9]. По данным различных авторов частота встречаемости данной нозологической формы составляет 20-60%, а у женщин репродуктивного возраста достигает 95% среди всех онкологических заболеваний [9].
Возможность озлокачествления доброкачественных новообразований молочных желез является достаточно серьезной проблемой. У пациенток, страдающих различными видами мастопатии с явлениями пролиферации, рак встречается в 30-40 раз чаще. [6,11]. Кроме этого, нередко заболевание сопровождается выраженной клинической симптоматикой, снижающей качество жизни.
По определению ВОЗ (1984), фиброзно-кистозная болезнь представляет собой «комплекс процессов, характеризующихся широким спектром пролиферативных и регрессивных изменений тканей молочных желез с формированием ненормальных соотношений эпителиального и соединительнотканного компонентов и образованием в молочной железе изменений фиброзного, кистозного, пролиферативного характера, которые часто сосуществуют» [3]. К пониманию структурных особенностей, происходящих в ткани молочной железы, контактной с опухолью следует подходить с позиции рассмотрения структурно-функциональной перестройки двух взаимосвязанных тканевых компонентов — паренхимы и стромы [3,4,10]. Морфологические критерии, которые традиционно рассматриваются в качестве прогностических, не всегда в полной мере позволяют характеризовать биологический потенциал патологических изменений ткани. В связи с чем, ведется поиск новых, более информативных параметров. Так, в настоящее время большое внимание уделяется исследованию воспалительной инфильтрации в строме окружающей опухолевый узел. Морфологические преобразования имеют тенденцию к увеличению пролиферативной активности, причем характерной особенностью, описываемой рядом авторов, является некоторое отставание пролиферации в дольковом эпителии по сравнению с протоковым [11]. Изменения стромы в процессе клеточной прогрессии (переход доброкачественной в злокачественную) включают уменьшение общего количества основного вещества, увеличение числа коллагеновых, эластических волокон и появление лимфоцитарных инфильтратов [10]. Неотъемлемой частью морфогенеза патологических изменений молочных желез является изменение гистоархитектоники микроциркуляторного русла. Обращает на себя внимание увеличение числа кровеносных сосудов, прямо пропорционально выраженности пролиферативных изменений [12].
Широкая распространённость доброкачественных гиперпластических процессов в молочной железе, недостаточность данных о нарушении стромально-клеточных взаимоотношений диктует необходимость детального изучения патоморфологических основ диспластических процессов молочных желез.
Целью исследования явилось выявление морфологических особенностей тканей молочной железы контактной с патологическим очагом у женщин репродуктивного возраста с диагнозом фиброаденома.
Материалы и методы. Исследовали биопсийный операционный материал от 20 женщин с доброкачественной патологией молочных желез. Заключительный патогистологический диагноз у всех женщин звучал как «фиброаденома молочной железы». Критериями включения в исследование являлись:
- возраст женщин от 25 до 45 лет,
- наличие очагового образования молочной железы, в сочетании с фиброзно-кистозной мастопатией, подтвержденных данными клинического, рентгеномаммографического, ультразвукового и цитологического обследования.
Критериями исключения из группы явились:
- менопауза,
- беременность и лактация.
Для светооптического исследования материал фиксировали в 10% водном растворе нейтрального формалина, жидкости Буэна. После стандартной гистологической проводки материал заливали в парафин-целлоидин. Приготовление серийных срезов толщиной 5-6 мкм осуществляли на ротационном микротоме МПС-2. Депарафинированные срезы окрашивали гематоксилином Майера и эозином. Морфометрические исследования осуществляли используя винтовой окуляр – микрометр МОВ – 1 -15у42 и окулярные вставки. Со срезов получали микрофотографии при помощи микрофотонасадки МФН-12. При морфометрическом исследовании использовали стереометрическую сетку Автандилова, содержащую 100 тест-точек [3, 5]. Проводили подсчет точек, совпадающих с изучаемыми гистологическими структурами на срезе ткани, и по 30 полям зрения микроскопа определяли долю железистой ткани, стромы и сосудов (в процентах). Базисом, на основе которого проводилась гистологическая оценка препаратов являлись рекомендации второго издания Международной гистологической классификации опухолей и опухолеподобных процессов молочной железы» (ВОЗ, Женева, 1981, русский вариант 1984) [HistiligicalTypingofBreastTumuors WHO, 2-d ed. – Geneva, 1981].
Результаты и их обсуждение. При исследовании гистологических препаратов было выявлено, что в тканях, окружающих фиброаденому пролиферативные процессы преобладают над непролиферативными. В большинстве препаратов пролиферация эпителия начиналась в терминальных протоках внутри долек, что характерно для дольковой гиперплазии. Долька была представлена альвеолярными фолликулами, выстланными двуслойным эпителием (рис.1). Внутридольковые протоки выстланы многослойным эпителием (рис. 2). Обращали на себя внимание мелкие кистозные полости, заполненные оксифильной гомогенной массой (рис. 3). Явления пролиферации также были представлены элементами протоковой гиперплазии, которая характеризовалась наличием солидных пролифератов. В них клетки лежали сплошным слоем, отмечался некоторый полиморфизм ядер. Миоэпителиоциты распространялись в центральные отделы пласта, где в виде мелких темноокрашенных элементов перемешивались с более крупными эпителиальными клетками. Разросшийся железистый и миоэпителиальные компоненты частично заполняли просвет протока, образуя сосочковые выросты, так называемые, солидные пласты, изредка железистоподобные структуры. Часть стенки протока сохраняла нормальное морфологическое строение в виде двуслойной выстилки (рис. 4). В некоторых местах альвеолы были растянуты, с формированием микрокист. Изучение клеточной структуры показало, что эпителиальные клетки расположены в несколько слоев. Вероятнее всего, верхний слой состоял из высокодифференцированных и вступивших на путь специфической дифференцировки клеток. Выраженные изменения наблюдали в базальной мембране. Местами она была разрыхлена, имела многослойную структуру. Фибриллярный компонент был представлен в основном коллагеновыми волокнами, без четкой ориентации. В соединительной ткани встречались сосуды с резко утолщенной внутренней оболочкой, явлениями гиперэластоза, окруженные скоплениями лимфоцитов (рис. 5). Стереометрические показатели срезов гистопрепаратов характерные для дольковой и протоковой гиперплазии представлены в таблице. Выявлены достоверные отличия по доле площади, занимаемой дольками и протоками у пациенток с проявлениями дольковой и протоковой гиперплазий соответственно. Нарастание относительной доли межклеточного вещества при наличии дольковой гиперплазии могло быть обусловлено отеком, набуханием коллагеновых и эластических волокон. При этом плотность сосудов в обеих группах не имела достоверных различий.
Выводы. Таким образом проведенное исследование морфологии молочной железы позволило получить новые данные об изменениях структуры ткани, контактной с опухолью у женщин репродуктивного возраста. Так у 80% пациенток преобладали явления дольковой гиперплазии, у 20% протоковой. Помимо этого, встречалось сочетание этих процессов, что может быть обусловлено различной чувствительностью клеток к эндогенным факторам (гормональным, факторам роста), так и физическими причинами.
Установлено, что у женщин данной возрастной категории изменения структурной организации проявлялись преимущественно в эпителиальном компоненте. Они характеризовались гиперплазией эпителиальных клеток, сопровождающейся облитерацией протоков. Формация стромального компонента в свою очередь проявлялась межуточным отеком.
В тканях с преобладанием явлений протоковой гиперплазии происходило достоверное увеличение групповых и одиночных протоков. В группе женщин с наличием в ткани дольковой гиперплазии выявлено увеличение площади долек, а также преобладание стромы. Учитывая данные литературы о роли гиперэстрогении в развитии мастопатии, можно полагать, что выявленные особенности морфометрических показателей у женщин с этой патологией обусловлены повышением уровня эстрогенов.
Структурно-функциональное изучение морфологических преобразований стромально-клеточной организации тканей молочной железы, в совокупности с изучением возрастных и индивидуальных особенностей проявления данной патологии позволит дифференцированно подходить к проблемам профилактики и лечения заболеваний молочных желез.
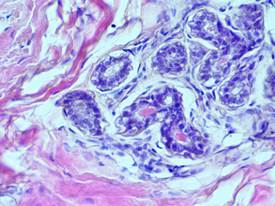
Рис.1. Фрагмент интактной ткани молочной железы на расстоянии 3 см от опухолевого узла; окр. гематоксилином и эозином (× 40). Дольковая гиперплазия. Плотно лежащие мелкие альвеолы, образованные двухрядным эпителием.
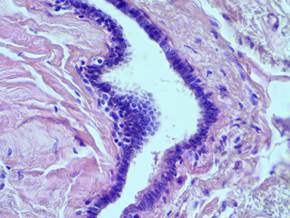
Рис.2. Фрагмент интактной ткани молочной железы на расстоянии 4 см от опухолевого узла; окр. гематоксилином и эозином (× 40). Многослойность эпителия внутридолькового протока.
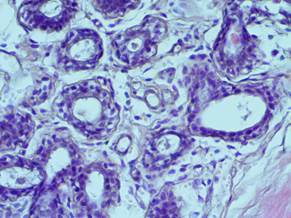
Рис.3. Фрагмент интактной ткани молочной железы на расстоянии 1 см от опухолевого узла; окр. гематоксилином и эозином (× 40). Кистозные полости и протоки, выстланные пролиферирующим эпителием.
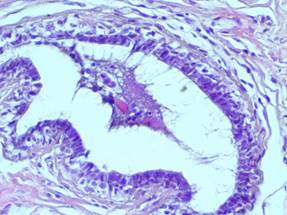
Рис.4. Фрагмент интактной ткани молочной железы на расстоянии 5 см от опухолевого узла; окр. гематоксилином и эозином (× 40). Протоковая гиперплазия. Разросшийся пролиферат заполняет просвет протока, образуя вырост, железистоподобную структуру.
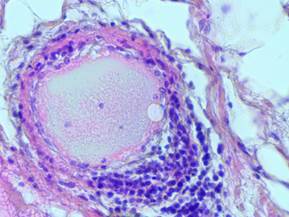
Рис.5. Фрагмент интактной ткани молочной железы на расстоянии 1 см от опухолевого узла; окр. гематоксилином и эозином (× 40). Пролиферативная форма фиброзно-кистозной мастопатии. Артериола, окруженная лимфоцитарным валом.
Стереометрические параметры форм пролиферативной мастопатии
|
Форма пролиферативной мастопатии |
Площадь одиночных протоков,% |
Площадь групповых протоков,% |
Площадь стромы,% |
Площадь долек, % |
Площадь сосудов, % |
|
Дольковая гиперплазия |
9,8±0,87* |
12,3±1,08* |
25,1±1,92* |
56,3±2,74* |
3,1±0,71 |
|
Протоковая гиперплазия |
38,7±1,56 |
55,4±1,62 |
12,4±1,03 |
14,6±1,23 |
2,4±0,62 |
Примечание: * различия достоверны (р≤0,01)
Рецензенты:
Абрамзон О.М., д.м.н., профессор кафедры общей хирургии ГБОУ ВПО «Оренбургский государственный медицинский университет» Минздрава России, г. Оренбург;
Валов С.Д., д.м.н., профессор кафедры гистологии, цитологии и эмбриологии ГБОУ ВПО «Оренбургский государственный университет» Минздрава России, г. Оренбург.
Библиографическая ссылка
Жирнова А.С., Шевлюк Н.Н., Курлаев П.П. ГИСТОАРХИТЕКТОНИКА И МОРФОФУНКЦИОНАЛЬНЫЕ ОСОБЕННОСТИ КЛЕТОЧНОГО МИКРООКРУЖЕНИЯ В ТКАНЯХ МОЛОЧНОЙ ЖЕЛЕЗЫ У ЖЕНЩИН РЕПРОДУКТИВНОГО ВОЗРАСТА // Современные проблемы науки и образования. 2015. № 5. ;URL: https://science-education.ru/en/article/view?id=21921 (дата обращения: 12.05.2026).



