Scientific journal
Modern problems of science and education
ISSN 2070-7428
"Перечень" ВАК
ИФ РИНЦ = 0,936
VASKULOENDOTELIALNY GROWTH FACTOR AS A MARKER OF ENDOTHELIAL DYSFUNCTION AND EARLY KIDNEY DAMAGE IN PATIENTS WITH METABOLIC SYNDROME
Распространенность метаболического синдрома (МС) в трудоспособной популяции составляет в среднем 25%. Синдром инсулинорезистентности является основой развития сахарного диабета 2-го типа и сердечно-сосудистых заболеваний (ССЗ) [1]. Кроме того, имеются данные, что МС негативно влияет на функцию почек, повышая риск возникновения хронической болезни почек (ХБП) в 1,6 раза [4].
Интегральным маркером кардиоренальных взаимоотношений является микроальбуминурия (МАУ), наличие которой указывает в том числе и на нарушенную функцию эндотелия [5]. Дисфункция эндотелия доказана при различных составляющих МС и может быть одним из его компонентов [2].
Одним из признанных биомаркеров дисфункции эндотелия является васкулоэндотелиальный фактор роста (ВЭФ), который активируется при формировании атеросклероза, гипертонической болезни, сахарного диабета 2-го типа [3]. В ряде работ было показано, что ВЭФ является ранним маркером повреждения почек у больных гипертонической болезнью (ГБ) [6].
Таким образом, вопрос ранней диагностики повреждения почек у больных МС весьма актуален, а использование маркера эндотелиальной дисфункции для этого процесса не изучено.
Цель исследования
Оценить возможность использования ВЭФ для ранней диагностики субклинического повреждения почек и эндотелиальной дисфункции у больных МС.
Материалы и методы
Группу обследования составили 40 пациентов с МС (критерии IDF, 2005) в возрасте от 25 до 55 лет, без органического повреждения почек в анамнезе и патологических изменений в общем анализе мочи, креатинина, без ультразвуковых признаков анатомических и структурных изменений почек. Пациенты ранее не получали гипотензивную терапию и статины.
В исследование не включали пациентов с вторичными формами АГ, больных с АГ III степени, сахарным диабетом (СД), воспалительными заболеваниями миокарда, системными заболеваниями соединительной ткани, онкологическими заболеваниями.
Группу сравнения составили 15 здоровых добровольцев (средний возраст 39,4±5,3 года; р<0,05).
Всем было проведено общеклиническое и лабораторное обследование. Уровни липидов, глюкозы плазмы крови, креатинина, мочевой кислоты, трансаминаз, билирубина определяли стандартными биохимическими методами. Индекс массы тела (ИМТ) рассчитывали по формуле Кетле: масса тела (кг)/рост (м²). Индекс инсулинорезистентности рассчитывался в малой модели гомеостаза (IR-HOMA). СКФ рассчитывали по формуле CKD-EPI мл/мин/1,73 м2. Степень снижения СКФ оценивали в соответствии с национальными рекомендациями 2012 г. [7].
Концентрацию изучаемых маркеров определяли в утренней порции мочи. Уровни ВЭФ в крови и моче, МАУ определяли методом иммуноферментного анализа (ИФА) с использованием фотометра «Stat-Fax» («Awareness Technology Inc.», США) и соответствующих наборов реагентов ЗАО «Вектор-Бест» (Новосибирск), «ELISA Micro-Albumin) производство Orgentec, Германия.
При статистической обработке данных использовали программу «Statistica 7.0 Rus». Оценивая данные с нормальным распределением, использовали (среднее, стандартную ошибку среднего), t-критерий Стьюдента. Данные с ненормальным распределением представлены в виде медианы и в виде интерквартильного интервала [25;75]. Для сравнения несвязанных выборок по количественным показателям использовали непараметрический критерий Манна—Уитни. Различия между выборками считали достоверными при значении для р<0,05. Связь признаков оценивали при помощи регрессивного анализа с определением коэффициента ранговой корреляции Спирмена, связь между значениями оценивали как сильную при R >|0,7|, средней силы при R от|0,3| до |0,7|, слабую при R< |0,3|.
Результаты
Сравниваемые группы не различались по возрасту (табл. 1). Отягощенная наследственность по сердечно-сосудистым заболеваниям (ССЗ) была выявлена у всех пациентов основной группы. Дислипидемия с гипертриглицеридемией присутствовала у 90%, низкий уровень ХСЛПВП — в 31%, а гипергликемия (без диагноза сахарного диабета) — у 68,5 % пациентов, что проявилось достоверным отличием от здоровых лиц. Средний стаж АГ оказался 4,1±2,5 года.
Таблица 1
Показатели больных метаболическим синдромом в сравнении с группой здоровых лиц (М ± SD).
|
Параметры (единицы) |
Группа МС (n=40) |
Здоровые (n=15) |
р |
|
Возраст (годы) |
42,3±8,3 |
39,4±5,3 |
0,7 |
|
ОТ (см) |
113,2±11 |
80,7±11 |
0,0001 |
|
ИМТ (кг/м²) |
38,0±10 |
27±1,3 |
0,00001 |
|
САД (мм рт. ст.) |
147,9±7,1 |
128,3±7,2 |
0,0001 |
|
ДАД (мм рт. ст.) |
98,8±5,0 |
78,5±5,3 |
0,0001 |
|
глюкоза (ммоль/л) |
5,8±0,8 |
4,21±0,5 |
0,0001 |
|
ХС (ммоль/л) |
5,9±0,9 |
4±0,7 |
0,004 |
|
ЛПНП (ммоль/л) |
3,62±0,7 |
2,43±0,4 |
0,03 |
|
ЛПВП (ммоль/л) |
1,31±0,3 |
1,4±0,1 |
0,3 |
|
ТГ (ммоль/л) |
2,33±1,1 |
0,57±0,11 |
0,001 |
|
креатинин (мкмоль/л) |
78,6±12,5 |
66,0±10,1 |
0,01 |
|
мочевая кислота (ммоль/л) |
391,4±45,4 |
241,5±86,1 |
0,009 |
|
СКФ мл/мин/1,73 кв.м. |
88,5±5,8 |
112,7±7,6 |
0,001 |
Примечание: АГ — артериальная гипертензия; ОТ — объем талии; ИМТ — индекс массы тела; САД — систолическое артериальное давление; ДАД — диастолическое артериальное давление; ХС — общий холестерин; ЛПНП – липопротеиды низкой плотности; ЛПВП — липопротеиды высокой плотности; ТГ — триглицериды; СКФ — скорость клубочковой фильтрации; SD (standard deviation) — стандартное отклонение; р – достоверность отличий в сравниваемых группах.
В группе МС было выявлено незначительное снижение СКФ (рис. 1).
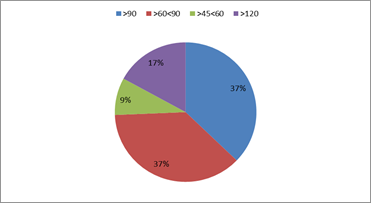
Рис. 1. Распределение пациентов по уровню СКФ мл/мин/1,73м²
Около половины больных МС с нормальным уровнем креатинина и протеинурии имели СКФ ниже оптимального. Значительное увеличение СКФ, равно как и ее снижение, было отмечено у больных с ожирением 3-й степени. Установлена отрицательная связь расчетной СКФ с уровнем ДАД (r=–0,4; р=0,04).
Была установлена прямая достоверная корреляция между суррогатным маркером инсулинорезистентности — величиной окружности талии (ОТ) и уровнем ДАД (r=0,43; р=0,03), мочевой кислоты (r=0,5; р=0,04), ТГ (r=0,36; р=0,03), ЛПОНП (r=0,5; р=0,04).
В группе больных МС была установлена достоверная корреляция уровня креатинина с общим холестерином (r=0,42; р=0,045), ЛПОНП (r=0,5; р=0,04) и мочевой кислоты (r=0,48; р=0,03).
Уровни маркеров эндотелиальной дисфункции и почечного повреждения – МАУ, ВЭФ — были значимо выше в группе МС (табл. 2).
Таблица 2
Концентрация ВЭФ и МАУ в группах
|
Показатель, единица измерения |
Значение медианы (25; 75% перцентиль); [Min- и Max- величины показателя] |
||
|
Группа МС (n = 38) |
контроль (n = 15) |
р |
|
|
Микроальбумин мг/мл |
25,8 (11,7; 34,0); [8,6; 56,5] |
9,4 (5,4;13,2); [1,4; 20,0] |
0,001 |
|
ВЭФ, пг/мл (моча) |
79,0 (28; 96,2); [5,0; 342] |
15,8 (9,1; 21,7); [02,1; 46,4] |
0,0001 |
|
ВЭФ, пг/мл (кровь) |
91 (76-270); [0-441] |
75 (0-96); [0-129] |
0,04 |
Примечание: МС — метаболический синдром; ВЭФ — васкулоэндотелиальный фактор роста
Уровни ВЭФ крови и мочи в группе МС были достоверно выше, чем в контрольной группе. Корреляции ВЭФ крови и мочи не было получено.
Была установлена прямая корреляция высокой степени между уровнем ВЭФ крови и общим холестерином (r=0,74; р=0,02), креатинином (r=0,67; р=0,001), IR-HOMA (r=0,36; р=0,04), ИМТ (r=0,4; р=0,04), уровнем ДАД (r=0,38; р=0,04), уровнем САД (r=0,6; р=0,02), МАУ (r=0,73; р=0,02) и отрицательная корреляция ВЭФ и СКФ (r=–0,7; р=0,02).
Также была установлена прямая связь между уровнем ВЭФ мочи и САД (r=0,49; р=0,04), МАУ (r=0,47; р=0,04), мочевой кислотой (r=0,49; р=0,04) и отрицательная с СКФ (r=–0,46; р=0,03).
Патологический уровень МАУ (>30 мг/мл) был установлен у 31,6% пациентов, 44,7% имели повышенный уровень МАУ (10–29 мг/мл).
Нами была установлена положительная корреляция величины МАУ с уровнем ДАД (r=0,7; р=0,02), уровнем креатинина (r=0,42; р=0,03), общего холестерина (r=0,41; Р=0,04) и отрицательная со значением СКФ (r=-0,5; р=0,03).
Обсуждение
На сегодняшний день СКФ рассматривают не только как показатель повреждения почек, но и как фактор риска неблагоприятных исходов у лиц с сердечно-сосудистыми заболеваниями и без них. В ряде работ было показано, что при снижении СКФ на 5 мл/мин/1,73 м2 риск сердечно-сосудистой смертности возрастает на 26%, а снижение СКФ с 90 до 60 мл/мин/1,73 м2 увеличивает ее в 4 раза. Причем связь снижения СКФ с исходами сердечно-сосудистых заболеваний не зависела от наличия АГ, СД [8]. В нашем исследовании незначительное снижение СКФ было выявлено у 37% пациентов, умеренное снижение СКФ — у 8,6%, меньший процент пациентов со сниженной СКФ в нашем исследовании можно объяснить более молодой группой (средний возраст 49 лет), небольшим стажем АГ (2–4 года).
Полученные изменения СКФ в отсутствие заболеваний почек в анамнезе и выявление четкой связи между показателями фильтрации, лабораторными проявлениями дисфункции эндотелия и уровня АД не только отражают начальные проявления нефропатии у больных МС, но и подтверждают повышенный риск сосудистых исходов.
Современные данные трактуют МАУ как показатель ранней почечной дисфункции, генерализованного поражения микрососудистого русла и доказанный маркер суммарного сердечно-сосудистого риска [2]. В среднем по данным литературы МАУ выявляется в 30–40% случаев АГ (до 72%), что, вероятно, связано с длительностью и тяжестью заболевания [2, 5]. Исследования АГ 1–2-й степени показали, что частота МАУ у данной категории больных составляет в среднем 12–22%, однако сочетание с ожирением увеличивает частоту МАУ до 30–40% [1, 2, 5]. В нашем исследовании МАУ была выявлена у 31,6% больных, и ее уровень сопряжен со снижением СКФ, что соответствует данным литературы.
Традиционное мнение о повышении уровня ВЭФ в ответ на гипоксию и активацию ангиогенеза подтверждается и данными нашего исследования [3]. У пациентов МС выявлено значительное повышение уровня ВЭФ крови и мочи по сравнению с контрольной группой. Увеличение содержания ВЭФ крови по мере роста ИМТ может быть связано со стимуляцией выделения цитокинов, в том числе и ВЭФ, под действием высокого уровня лептина, характеризующего степень ожирения [3].
Нами установлена прямая корреляционная связь между уровнем ВЭФ и индексом HOMA, отражающая зависимость инсулинорезистентности и эндотелиальной дисфункции. Существуют данные, подтверждающие значение ВЭФ как чувствительного предиктора развития сахарного диабета 2-го типа [9].
В нашем исследовании определяется значительное повышение уровня ВЭФ крови у молодых пациентов с малым стажем АГ. Также установлена корреляция уровня ВЭФ САД и ДАД, что подтверждает наличие дисфункции эндотелия даже у пациентов с небольшим стажем и невысокой степенью АГ [6, 10]. Следовательно, повышенный уровень ВЭФ крови в группе пациентов МС отражает наличие эндотелиальной дисфункции, связанной со степенью ожирения, инслинорезистентности и уровнем АД. Вероятно, мы можем рассматривать ВЭФ как интегральный показатель дисфункции эндотелия при множественных факторах риска сердечно-сосудистых заболеваний.
Ряд исследований показал, что связующим звеном между МАУ и сердечно-сосудистым риском может быть избыточная продукция ВЭФ, который не только повышает проницаемость сосудистой стенки, способствуя геморрагическим и атеросклеротическим процессам, но и увеличивает проницаемость клубочкового фильтра для альбумина [6, 10]. Было показано, что у больных мягкой формой АГ маркером раннего почечного повреждения может являться ВЭФ, причем была установлена прямая корреляция между величиной МАУ и уровнем ВЭФ в моче. Полученные данные отражают как наличие эндотелиальной дисфункции, так и активацию механизмов фиброгенеза, которые являются звеньями процессов ремоделирования микрососудистого русла почки при гипертонической нефропатии [6]. В нашем исследовании уровень ВЭФ мочи был достоверно выше в группе больных, нами также выявлена прямая корреляция МАУ и ВЭФ. Кроме того, была установлена отрицательная связь ВЭФ и СКФ, что также подтверждает то, что ВЭФ маркирует повреждение клубочка.
Выводы
1. Васкулоэндотелиальный фактор крови у пациентов с МС может быть интегральным маркером эндотелиальной дисфункции, связанным с основными компонентами синдрома инсулинорезистентности.
2. У пациентов с МС, не имеющих клинико-лабораторных признаков поражения почек, повышение МАУ и ВЭФ крови и мочи может свидетельствовать о субклинической почечной дисфункции.
Работа выполнена при поддержке ГРАНТа РНФ № 14-15-00809.
Рецензенты:
Завражных Л.А., д.м.н., главный врач ЗАО «Курорт Усть-Качка», г. Пермь;
Хлынова О.В., д.м.н., профессор кафедры госпитальной терапии ГБОУ ВПО ПГМУ им. ак. Е.А. Вагнера Минздрава России, г. Пермь.
Библиографическая ссылка
Смирнова Е.Н., Шулькина С.Г., Смирнова Е.Н., Шулькина С.Г., Щекотов В.В., Антипова А.А. ВАСКУЛОЭНДОТЕЛИАЛЬНЫЙ ФАКТОР РОСТА КАК МАРКЕР ЭНДОТЕЛИАЛЬНОЙ ДИСФУНКЦИИ И РАННЕГО ПОВРЕЖДЕНИЯ ПОЧЕК У БОЛЬНЫХ МЕТАБОЛИЧЕСКИМ СИНДРОМОМ // Современные проблемы науки и образования. 2015. № 5. ;URL: https://science-education.ru/en/article/view?id=21800 (дата обращения: 12.05.2026).



