Цель исследования – оценка эффективности применения технологии аутологичного модифицирования дентальных имплантатов на основе нетканого титанового материала со сквозной пористостью при использовании методов доказательной медицины.
Материалы и методы.В группу наблюдения было включено 20 пациентов с частичным отсутствием зубов на нижней челюсти. Всем пациентам после подписания добровольного информированного согласия в соответствии с ФЗ № 323 от 21 ноября 2011 года «Об основах охраны здоровья граждан в Российской Федерации» была произведена операция - дентальная имплантация с аутологичным модифицированием (патент РФ на изобретение №2544804). Каждому больному было установлено от 2 до 3 дентальных имплантатов в зависимости от индивидуальной клинической ситуации. Под местной анестезией производили выкраивание слизисто-надкостничного лоскута в области нижней челюсти. Производили скелетирование альвеолярной части нижней челюсти. При помощи набора фрез конструкции автора (патент РФ на полезную модель №139356) было произведено формирование костного ложа в области альвеолярной части челюсти в проекции отсутствующих зубов. Параллельность сформированного костного ложа определяли при помощи пинов и параллеометра. Подготавливали заготовку имплантата на основе титановой проволоки в соответствии с рисунком 1.

Рис.1. Заготовка имплантата
Полученную аутологичную костную стружку собирали в дозатор и ресуспендировали в физиологическом растворе. В условиях операционной методом холодного прессования производили модифицирование нетканого титанового материала со сквозной пористостью аутологичной костной стружкой методом холодного прессования в соответствии с рисунком 2.
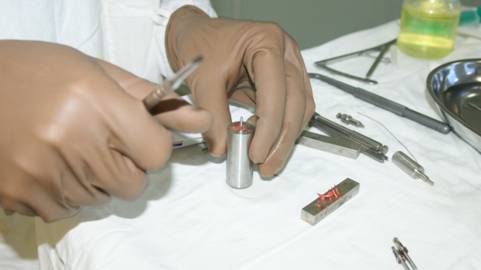
Рис.2. Модифицирование нетканого титанового материала со сквозной пористостью аутологичной костной стружкой
Для модификации материала использовался гидравлический пресс, титановая пресс-форма, выпрессовыватель. В ходе технологии холодного прессования получена внутрикостная втулка на основе нетканого титанового материала со сквозной пористостью, модифицированная аутологичной костной тканью в соответствии с рисунком 3.

Рис.3. Внутрикостная втулка на основе нетканого титанового материала со сквозной пористостью, модифицированная аутологичной костной тканью
Втулку устанавливали в костное ложе при помощи имплантовода до первичной стабильности. При помощи низкочастотного ультразвука производили активацию втулки внутри костного ложа. При помощи динамометрического ключа производили инсталляцию внутрикостного винта-распорки во втулку и костное ложе с усилием 35 н×см в соответствии с рисунком 4.
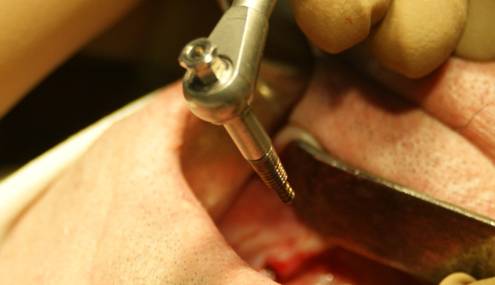
Рис.4. Инсталляция внутрикостного винта–распорки
Винт–распорку инсталлировали до уровня кортикальной пластины альвеолярной части. Производили установку формирователей десны. Рану ушивали узловыми швами, накладывали асептическую повязку. С момента операции проводили наблюдение в течение 3 месяцев, после чего проводили ортопедическое лечение. Оценку клинической эффективности оценивали на 14-е сутки, 2-й и 3-й месяцы. За неблагоприятный исход, свидетельствующий о недостаточной клинической эффективности, принимали клинические случаи дезинтеграции имплантата с нарушением его стабильности с резорбцией костной ткани. Частота исходов в группе лечения (ЧИЛ) высчитывалась как ЧИЛ=А/А+B, где А- наличие изучаемого эффекта, B-недостаточная эффективность.
Результаты исследования. На 14-е сутки наблюдения на ортомантомограммах отмечалось спокойное состояние костной ткани. Рисунок в зоне имплантации чёткий, с хорошо визуально различимой структурой. Разряжение костной ткани в области установленных имплантатов наблюдалось в пришеечной области у 1 пациента в области двух имплантатов, установленных на нижней челюсти. Данные изменения носили вид воронкообразного разряжения до 1 мм, имплантаты стабильны. При проведении рентгенологического исследования на второймесяц после операции изменений структуры костной ткани в области операции выявлено не было. Рисунок костной ткани чёткий, плотность тканей по периферии от установленных имплантатов не нарушена. Рентгенологическая картина у пациента с пришеечной резорбцией костной ткани показала стабилизацию процесса. На 3-ймесяц,при проведении оценки результатов на полученных ортопантомограммах у 20 пациентов, была отмечена стабильность рентгенологической картины у всех исследуемых пациентов. В области установленных имплантатов отсутствовали какие-либо изменения костной ткани. Структура костной ткани чёткая, хорошо визуально просматриваемая во всех отделах. Плотность костной ткани удовлетворительная, имплантаты стабильны. Частота исходов в группе лечения составила 1, что характеризует клиническую эффективность данного метода лечения.
Выводы. Применение разработанного метода аутологичного модифицирования нетканого титанового материала со сквозной пористостью позволило добиться оптимальных результатов в послеоперационном периоде. Положительные исходы в исследуемой группе составили 100%. Предложенный метод лечения имеет перспективу широкого внедрения в дентальную имплантологию.
Рецензенты:Бережной В.П., д.м.н., профессор кафедры терапевтической стоматологии ГБОУ ВПО «СамГМУ» Минздрава России, г. Самара;
Байриков И.М., д.м.н., профессор, заведующий кафедрой челюстно-лицевой хирургии и стоматологии ГБОУ ВПО «СамГМУ» Минздрава России, г.Самара.



