Scientific journal
Modern problems of science and education
ISSN 2070-7428
"Перечень" ВАК
ИФ РИНЦ = 0,936
THE INFLUENCE OF GOLD NANOPARTICLES ON MITOCHONDRIAL POTENTIAL AND THE CONCENTRATION OF REACTIVE OXYGEN SPECIES IN TUMOR CELLS AT DIFFERENT PERIODS OF THE CELL CYCLE IN VITRO
Стремительно развивающиеся исследования свойств наноматериалов и наночастиц ставят задачу оценить их влияния на живые организмы, как на уровне всего организма, так и на отдельные клетки и клеточные структуры. Оценка клеточных эффектов является особенно важной вследствие наноразмерности действующих агентов, которые непосредственно воздействуют на клеточные структуры. В настоящее время цитотоксичность наночастиц определяют чаще всего с помощью МТТ-теста, позволяющего оценить специфическую гибель клеток. В то же время показатели функционального состояния митохондрий, отражающих адекватность энергопродукции для поддержания нормального метаболизма клеток, и активность генерации активных форм кислорода (АФК), как показатель выраженности патологических процессов в клетке, остаются не изученными.
Целью данной работы явилось изучение влияния ЗНЧ на некоторые метаболические изменения синхронизированных по периодам клеточного цикла клеток in vitro.
Материал и методы исследования. В экспериментах использовали клеточную линию карциномы толстого кишечника HCT-116. Клетки культивировали при 37 °С, во влажной атмосфере, содержащей 5 % СО2. Для культивирования использовали среду RPMI-1649, содержащую L-глутамин, 12 % фетальной коровьей сыворотки и 50 мкг/мл гентамицина. Синхронизацию клеток проводили с помощью двойного тимидинового блока по стандартной прописи [3]. В работе были использованы наночастицы диаметром 10 нм, синтезированные в лаборатории нанобиотехнологий ИБФРМ РАН (руководитель – д.ф.-м.н., проф. Н.Г. Хлебцов). Финальная концентрация золота равнялась 50 мкг/мл. В культуру клеток вносили 3,125 мкл 10 нм ЗНЧ с добавлением 0,5 мл среды. В связи с тем, что золото обладает собственной флуоресценцией [4], проникновение ЗНЧ в клетки фиксировали с помощью проточного цитометра Becton Dickinson FACS.
Митохондриальный мембранный потенциал (трансмембранный потенциал) является важным показателем метаболической активности клеток, кроме этого, он отражает способность митохондрий генерировать АФК. Митохондриальный потенциал клеток HCT-116 определяли с использованием флуоресцентного красителя этилового эфира тетрародоминперхлората (TMRE). TMRE добавляли в среду с клетками в конечной концентрации 200 мкМ за 20 мин до анализа и держали в СО2-инкубаторе при 37°С. После инкубации среду удаляли, добавляли равный объём фосфатного буферного раствора рН 7,4 и определяли интенсивность красной флуоресценции с использованием проточного цитометра Becton Dickinson FACS Canto (лазер 488 нм, LP зеркало – 556, BP фильтр – 585/42). Зонд TMRE избирательно накапливается в функционально полноценных митохондриях с высоким трансмембранным потенциалом, и интенсивность его флуоресценции характеризует их АТФ-синтезирующую способность и энергообеспеченность клеток.
Внутриклеточную концентрацию FAR после введения ЗНЧ определяли с использованием 2′,7′-дихлородигидрофлуоресцеин диацетата (DCFH-DA). DCFH-DA добавляли в среду с клетками в конечной концентрации 30 мкМ за 30 мин до анализа и держали в СО2-инкубаторе при 37 °С в темноте. Интенсивность флуоресценции дихлорофлуоресцеина измеряли с использованием проточного цитометра Becton Dickinson FACS Canto (лазер 488 нм, LP зеркало – 503, BP фильтр – 530/30). Флуоресценция зонда DCFH-DA возникает при взаимодействии его молекул с АФК, и ее интенсивность характеризует активность свободнорадикальных процессов.
Флуоресценцию зондов изучали в клетках HCT-116 контрольной группы и после 60-минутной инкубации с ЗНЧ. При определении значений флуоресценции учитывали фоновые показатели. Все эксперименты и определения параметров были выполнены, как минимум, с пятикратным повторением. Результаты выражались как среднее значение ± ошибка среднего (М ± m). Статистическую обработку цифрового материала осуществляли с помощью компьютерной программы «Statistica 6.0», используя непараметрический анализ.
Результаты исследования и их обсуждение
Согласно литературным данным, ЗНЧ проникают в клетки in vitro уже через 5 минут после внесения в культуру [2]. На это указывает и уровень флуоресценции клеток с ЗНЧ, который имеет положительное значение, в то время как в культуре клеток без ЗНЧ при всех равных условиях флуоресценция отсутствовала (табл. 1).
Таблица 1
Уровень
флуоресценции (условные единицы, у.е.) клеток HCT-116
в норме (контроль) и после введения в культуру 10-нм ЗНЧ через 60 минут
|
фаза клеточного цикла
эЭкспериментальная ггруппа |
G1 |
S |
G2 |
M |
|
контроль |
- 48,85±6,40 |
- 60,32±2,50 |
- 46,74±3,41 |
- 54,87±2,84 |
|
ЗНЧ (60 мин) |
57,99±4,87* |
47,68±4,72* |
49,08±4,07* |
77,09±5,11* |
* – статистически значимые отличия уровня флуоресценции от контрольных значений (p<0.001).
Флуоресценция TMRE раковых клеток HCT-116 на протяжении всего клеточного цикла снижается. Период интерфазы характеризуется постепенным недостоверным (p>0.05) уменьшением значений с 73,89±3,39 у.е. в G1 периоде до 60,94±4,34 у.е. в G2 периоде. Своего минимума флуоресценция TMRE достигает в митотический период, снижаясь в 1,6 раза. Известно, что митохондриальный потенциал в норме изменяется вследствие изменения метаболической активности клетки. Уменьшение флуоресценции TMRE свидетельствует о временном снижении АТФ-синтетической активности митохондрий в период митоза клеток.
Интерфаза раковых клеток HCT-116 характеризуется достоверным ростом флуоресценции зонда DCFH-DA, свидетельствующим об усилении продукции АФК, которые регулируют ряд физиологических процессов, таких как пролиферация клеток и их дифференцировка [6]. Известно, что концентрация АФК различается в зависимости от физиологического статуса клетки (например, стадии клеточного цикла). Достижение определенного уровня АФК в клетке включает каскад реакций, которые стимулируют пролиферацию [1]. В М-период концентрация АФК значительно уменьшается, о чем свидетельствует 5-кратное снижение флуоресценции зонда DCFH-DA в клетках. Уменьшение внутриклеточного содержания АФК происходит за счет нейтрализации образовавшихся метаболитов, а также посредством снижения образования новых АФК.
60-минутная инкубация клеток HCT-116 с ЗНЧ не сопровождается значительными метаболическими изменениями, о чем свидетельствует отсутствие достоверных различий в показателях флуоресценции зонда TMRE между клетками контрольной группы и клетками, подвергшихся воздействию ЗНЧ в M, G1 и S периоды клеточного цикла. В клетках обеих групп указанных периодов определяется интенсивная флуоресценция этого зонда (рис. 1), что указывает на наличие функционально активных митохондрий, обеспечивающих адекватное энергоснабжение этих клеток. Период G2 характеризуется достоверным уменьшением митохондриального потенциала у клеток, подвергшихся воздействию ЗНЧ, о чем свидетельствуют меньшие значения флуоресценции (p<0.05) клеток с ЗНЧ по сравнению с таковыми клеток контрольной группы. Уменьшение флуоресценции зонда TMRE на 20 % в период G2 по сравнению с клетками контрольной группы свидетельствует о снижении АТФ-продуцирующей функции митохондрий в данный период.
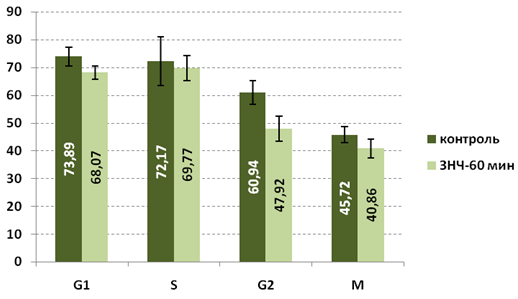
Рис. 1. Интенсивность флуоресценции (у.е.) TMRE клеток HCT-116 в норме (контроль) и после культивирования клеток ЗНЧ в течение 60 минут (ЗНЧ-60 мин)
Клеточный цикл HCT-116 при 60-минутном нахождении ЗНЧ в культуре характеризуется скачкообразными изменениями флуоресценции зонда DCFH-DA (рис. 2). Часовая экспозиция раковых клеток HCT-116 с ЗНЧ приводит к значительному падению продукции в этих клетках АФК, индикатором чего служат меньшие значения интенсивности флуоресценции DCFH-DA в G1, S и G2 периодах клеточного цикла в сравнении с клетками контрольной группы (p<0.05). Данный факт свидетельствует об уменьшении продукции АФК в течение указанных периодов в клетках с ЗНЧ, а также об активации процессов элиминации АФК внутриклеточными антиоксидантными ферментами (супероксиддисмутаза, пероксидредуктаза, глутатионтрансфераза и др.). Снижение концентрации АФК в G2-период происходит за счет уменьшения продукции митохондриальных АФК, о чем свидетельствует снижение функциональной актианости митохондрий в этот период (рис. 1).
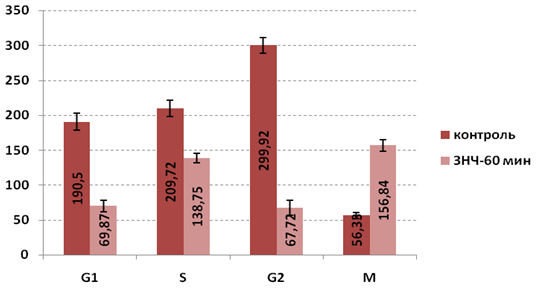
Рис. 2. Флуоресценция TMRE клеток HCT-116 в норме (А) и после культивирования клеток ЗНЧ в течение 30 минут (Б) и 60 минут (В). Конфокальная микроскопия с окраской DCFH-DA
Обращает внимание тот факт, что М-период клеток, подвергшихся часовому воздействию ЗНЧ, характеризуется почти трехкратным усилением флуоресценции зонда DCFH-DA по сравнению с клетками контрольной группы, что указывает на увеличение концентрации АФК в клетках с ЗНЧ. Однако флуоресценция клеток, подвергшихся воздействию ЗНЧ, не достигает максимальных значений флуоресценции клеток контрольной группы в другие периоды клеточного цикла.Рост концентрации АФК в М-период в клетках с ЗНЧ, вероятно, обусловлен восстановлением NADPH-оксидаз на плазматической мембране клеток [5] и в меньшей степени образованием т.н. митохондриальных АФК. На это указывает снижение флуоресценции зонда TMRE в М-период, свидетельствующее об уменьшении функциональной активности митохондрий. Известно, что АФК, генерируемые с помощью NADPH, в большей степени выполняют защитную функцию и продуцируются специализированными клетками, такими как нейтрофилы и макрофаги [8]. Вероятно, увеличение концентрации АФК в М-периоде обусловлено накоплением ЗНЧ в клетках (табл. 1). Повышение концентрации митохондриальных АФК в М-периоде клеток с ЗНЧ, вероятно, будет способствовать развитию оксидативного стресса и необратимому повреждению клеток, индуцируя апоптоз раковых клеток [7].
Выводы
Таким образом, присутствие ЗНЧ в культуре раковых клеток HCT-116 в течение 60 минут не обусловливает развитие оксидативного стресса клеток и не приводит к функциональным нарушениям митохондрий, о чем свидетельствует отсутствие резких и значимых уменьшений мембранного потенциала митохондрий в клетках с ЗНЧ и меньшая концентрация АФК в G1, S и G2. Рост концентрации АФК в М-период в клетках с ЗНЧ, вероятно, обусловлен накоплением частиц в цитоплазме и будет индуцировать гибель клеток.
Рецензенты:
Слесарева Е.В., д.м.н., доцент, заведующий кафедрой морфологии Института медицины, экологии и физической культуры ФГБОУ ВПО «Ульяновский государственный университет», г. Ульяновск;
Золотухин В.В., д.б.н., профессор кафедры зоологии ФГБОУ ВПО «Ульяновский государственный педагогический университет им. И.Н. Ульянова», г. Ульяновск.
Библиографическая ссылка
Михеева Н.А., Семенова М.А., Терентюк Г.С., Хайруллин Р.М., Михеев В.А., Столбовская О.В., Гальчин А.В. ВЛИЯНИЕ НАНОЧАСТИЦ ЗОЛОТА НА МИТОХОНДРИАЛЬНЫЙ ПОТЕНЦИАЛ И КОНЦЕНТРАЦИЮ АКТИВНЫХ ФОРМ КИСЛОРОДА ОПУХОЛЕВЫХ КЛЕТОК В РАЗЛИЧНЫЕ ПЕРИОДЫ КЛЕТОЧНОГО ЦИКЛА IN VITRO // Современные проблемы науки и образования. 2015. № 4. ;URL: https://science-education.ru/en/article/view?id=20483 (дата обращения: 12.05.2026).



