Scientific journal
Modern problems of science and education
ISSN 2070-7428
"Перечень" ВАК
ИФ РИНЦ = 0,936
PARACLINICAL METHODS OF RESEARCH OF STERNAL BONE CONSOLIDATION AFTER COLD PLASMA AND STANDARD STERNOTOMY
Частота подобных осложнений по разным данным составляет 0,4–8%. При этом в группе риска развития стернальной инфекции, которая составляет от 12 до 20% прооперированных пациентов, при развитии послеоперационного медиастинита летальность достигает 14–47% [1]. Нестабильность каркаса грудной клетки в послеоперационном периоде и последующее развитие остеомиелита и стерномедиастинита приводит к появлению либо усилению болевого синдрома, нарушению функции дыхания и влечет за собой удлинение сроков госпитализации и повышение стоимости лечения [9].
Нерешенность вышеизложенных проблем заставляет не только вести поиск новых, менее травматичных методик для рассечения грудины и гемостатических материалов с минимальным влиянием на репарацию костной ткани, но и требует разработки алгоритма для контроля процесса консолидации грудины с использованием комплекса параклинических методов исследования.
В современной практике для оценки степени консолидации грудины и диагностики возможных раневых осложнений наиболее часто используется компьютерная томография [7]. Однако существуют исследования, сообщающие о высокой информативности применения для этих целей остеосцинтиграфии[9], а также определения уровня маркеров метаболизма костной тканив сыворотке крови и моче [6].
Цельюданной работы является сравнительная оценка течения неосложненной репаративной регенерации грудины после холодноплазменнойстернотомии [3] и cтандартнойстернотомии, а также при раневых осложнениях грудной стенки.
Материал и методы
Материалом для анализа послужили данные обследования и лечения пациентов сишемической болезнью сердца, мужского и женского пола, оперированных через срединную стернотомию.В исследование включено 50 пациентов, средний возраст составил 62±6,5 лет. Всем пациентам было выполненокоронарное шунтирование. Обсуждаемые пациенты, согласно применявшейся методике хирургического доступа, были разделены на две группы.
Первая группа (основная) – включает 25 пациентов (21 мужчина и 4 женщины), которым рассечение грудины проводилось стернотомом с холодноплазменным наконечником. В применении дополнительных методов гемостаза необходимости не было. Вторую группу (контрольная) составили 25 человек (20 мужчин и 5 женщин), которым этап стернотомии проводился с использованием стандартной электромеханической пилы фирмы «AesculapAG&CO.KG»(Germany). Гемостаз рассеченной грудины у данных пациентов проводился по принятой методике с использованием электрокоагуляции для остановки кровотечения из надкостницы и медицинского воска – для остановки кровотечения из губчатого вещества грудины.
По основному заболеванию, сопутствующей патологии, видам хирургической коррекции заболеваний, а также дооперационным факторам риска развития стернальных осложнений [10] группы не различались. Различия в группах пациентов отмечались среди интароперационных факторов риска – таких как использование медицинского воска и электрокоагуляции для гемостаза грудины (p<0,05).
Пациентам обеих групп помимо общепринятого в кардиохирургии обследования,для контроля регенерации грудины на разных этапах лечения проводилось трехкратное определение маркеров костного метаболизма в сыворотке крови (концентрацииостеокальцина и активности костного изофермента щелочной фосфатазы – остазы)и моче (дезоксипиридинолин) методом иммуноферментного анализа, спиральная компьютерная томография и остеосцинтиграфия грудины. При этом исходные значения всех биохимических маркеров находились в пределах нормы – для остеокальцина 9,6–40,8 нг/мл., для остазы 15,0–41,3 Ед/л, для дезоксипиридинолина 2,3–5,4 нмоль/л.
Согласно клиническим данным, из 50 обследованных пациентов у 4-х отмечено осложненное течение постстернотомной раны – один случай развития свищевого хода в пределах подкожной жировой клетчатки без инфицирования (пациент основной группы), два случая инфекции мягких тканей и один случай стерномедиастинита, потребовавшие повторного хирургического вмешательства (пациенты контрольной группы). Данные пациенты при проведении ретроспективного анализа объединены в третью группу (группа осложнений).
Статистика. Проверку достоверности межгрупповых
различий показателей проверяли при помощи Т-критерия Манна – Уитни (с учетом
поправки Йейтса) для параметров, имеющих нормальное распределение, и Н-критерия
Крускала – Уоллиса при распределении, не соответствующем нормальному. Нормальность
распределения оценивали с использованием Shapiro-Wilk W-статистики при n![]() 50.Различия
считали статистически значимыми при уровне p<0,05 [2].
50.Различия
считали статистически значимыми при уровне p<0,05 [2].
Результаты и обсуждение
При оценке неспецифических воспалительных маркеров во всех группах отмечено повышение их уровня к 2-х недельному сроку, с последующим снижением до нормальных значений (3-я контрольная точка). Однако в группе осложнений уровень СОЭ к 6-ти месяцам значимо не изменился и оставался повышенным (рисунок 1).

Рис.1. Динамика неспецифических воспалительных маркеров в крови. Межгрупповые различия статистически не достоверны. Примечание: Лц – лейкоциты, СОЭ – скорость оседания эритроцитов, СРБ – С-реактивный белок. Исходный уровень (1), через 2 недели (2) и 4-6 месяцев после стернотомии (3), соответственно
Сравнительный анализ концентрации остеокальцина в сывороткекровипациентов в динамике показал прогрессивное увеличение его концентрации при неосложненном течении (рисунок 2). В группе пациентов с раневыми осложнениями отмечено снижение концентрацииостеокальцина в остром периоде (2 недели) на 36,7%, с последующим его приростом.
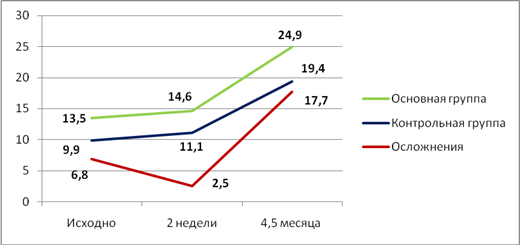
Рис.2. Концентрация остеокальцина в сыворотке крови в группах в различные сроки. Представлены медианные значения
При этом в основной группе концентрацияостеокальцина была наиболее высокой на всех этапах исследования, что может свидетельствовать о более выраженной остеобластической активности, обусловленной меньшей травматизацией костной ткани при проведении холодноплазменной стернотомии и меньшей интенсивностью асептического воспаления в области распила грудины.
Активностькостного изофермента щелочной фосфатазы (остазы) во всех группах через 2 недели после стернотомии была выше исходной – прирост в основной группе составил 77,5%, в контрольной 59,5%, а в группе осложнений 66,6%. К 3-й контрольной точке отмечено снижение активностиостазы, не достигшее однако исходных значений. Активность фермента в сыворотке пациентов в группах к 6-ти месяцам достоверно не различалась и составила 147,9% от исходной для основной группы, 143% для контрольной и 141,8% для группы осложнений.
Определение концентрациидезоксипиридинолина(ДПД) в моче пациентов также показало ее увеличение во всех группах к 2-х недельному сроку, при этом наиболее высокие показатели отмечены в группе осложнений на всех этапах исследования, и особенно в острый период. Самая низкая концентрация маркера отмечена в основной группе пациентов через 2 недели после стернотомии и в среднесрочном периоде, что может быть связано с меньшей травматизацией тканей грудины на этапе доступа (рисунок 3).
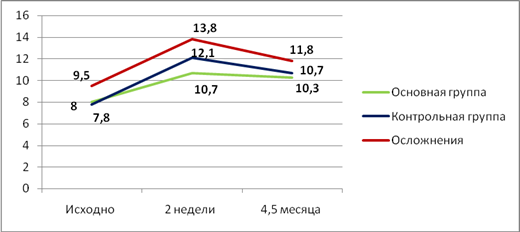
Рис.3. Изменение концентрации ДПД в моче. Представлены медианные значения. Примечание: Δ1(%) – концентрация ДПД через 2 недели после операции, выраженная в процентах относительно исходного значения. Δ3(%) – концентрация ДПД через 4–6 месяцев после операции, выраженная в процентах относительно исходного значения
Таким образом, при анализе маркеров костного метаболизма в динамике в сыворотке и моче отмечено, что в группе пациентов, имевших осложненное течение послеоперационной раны, в остром периоде (2-х недельный срок) интенсивность остеобластических процессов снижена (в сравнении с неосложненным течением), что подтверждается выраженным снижением концентрацииостеокальцина. В то же времяотмечается интенсивная резорбция костной ткани, о которой свидетельствует значительное повышение концентрации дезоксипиридинолина.
Данные биохимических исследований согласуются с результатами проведенной остеосцинитиграфии грудины, где отмечено повышенное накопление радиофармпрепарата (Технефор, 99mTc) у пациентов, имевших раневые осложнения (рисунок 5), отражающее более интенсивный кровоток в зоне распила, что может свидетельствовать о продолжающемся асептическом воспалении. В основной группе пациентов накопление препарата во всех отделах грудины было ниже, чем в остальных группах, что может свидетельствовать о снижении интенсивности воспаления у данных пациентов к 6-ти месяцам после перенесенной стернотомии.
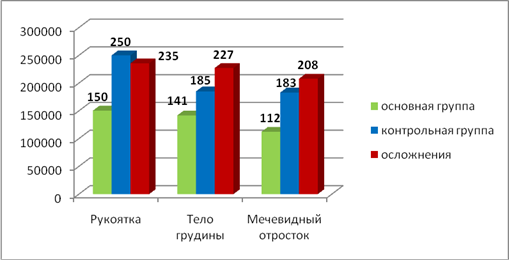
Рис. 5. Накопление радиофарпрепарата (Технефор, 99mTc) различными отделами грудины, число импульсов (тыс). Представлены медианные значения
Проведенная через 6 месяцев после стернотомииспиральная компьютерная томография (СКТ) грудины не выявила существенных межгрупповых различий – у всех пациентов отмечено формирование в зоне распила грудины разной выраженности и протяженности соединительнотканной мозоли, что согласуется с литературными сообщениями [5], где срок завершенной консолидации грудины принят за 12 месяцев. Полученные данные позволяют говорить о не высокой информативности данного метода в оценке неосложненной послеоперационной консолидации грудины.
Наибольшую информативность и хорошее соответствие с клиническими данными в исследовании показали биохимические маркеры регенерации костной ткани (остеокальцин и дезоксипиридинолин)сыворотки крови и мочи, которые также соотносились с результатами остеосцинтиграфии грудины.
Выводы
По данным комплексного параклинического обследования, стернотомия с холодноплазменным компонентом снижает травматическое воздействие на ткани грудины, а также продолжительность и интенсивность асептического воспаления в зоне хирургического доступа, что способствует снижению частоты раневых послеоперационных осложнений.
По данным проведенной СКТ грудины у пациентов, перенесших полную продольную срединную стернотомию, в сроки наблюдения до полугода не наступает полного восстановления костной ткани грудины. В месте распила вне зависимости от методики стернотомии формируется соединительнотканная мозоль, что необходимо учитывать в послеоперационной реабилитации.
Применение с диагностической целью остеосцинтиграфии грудины, наряду с анализом биохимических маркеров костной регенерации в сыворотке крови и моче,является оправданным, информативным, хорошо согласуется с клиническими данными и позволяет оценить состояние костной ткани, интенсивность кровообращения, воспалительных реакций и остеорепаративных процессов в зоне распила грудины, а также может быть полезным для выявления инфекционных осложнений в зоне интереса.
Рецензенты:Латыпов В.Р.,д.м.н., заведующий урологическим отделением клиники общей хирургии ГБОУ ВПО СибГМУ Минздрава России, г. Томск;
КомковаТ.Б., д.м.н.,профессор кафедры общей хирургии ГБОУ ВПО СибГМУ Минздрава России, г. Томск.
Библиографическая ссылка
Козлов Б.Н., Насрашвили Г.Г., Кузнецов М.С., Панфилов Д.С., Гусакова А.М., Саушкин В.В., Гуляев В.М., Николаев А.Г., Шипулин В.М. ПАРАКЛИНИЧЕСКИЕ МЕТОДЫ ИССЛЕДОВАНИЯ РЕПАРАТИВНОЙ РЕГЕНЕРАЦИИ ГРУДИНЫ ПОСЛЕ ХОЛОДНОПЛАЗМЕННОЙ И СТАНДАРТНОЙ СТЕРНОТОМИИ // Современные проблемы науки и образования. 2015. № 3. ;URL: https://science-education.ru/en/article/view?id=19043 (дата обращения: 17.05.2026).



