Scientific journal
Modern problems of science and education
ISSN 2070-7428
"Перечень" ВАК
ИФ РИНЦ = 0,936
MOLECULAR APPROACHES FOR IDENTIFICATION OF TRITICUM AESTIVUM L GENOTYPES BY ALLELIC VARIANTS OF WAXY-GENES AND HMW GLUTENIN SUBUNITS
Известно, что нефункциональные нуль-аллели локусов Wx-A1, Wx-B1 и Wx-D1 Waxy-генов пшеницы имеют прямое влияние на образование крахмала амилопектинового типа, где наиболее существенное снижение содержания амилозы оказывает хозяйственно-ценный нулевой аллель Wx-B1-локуса – Wx-B1b, идентификация которого диагностически значима [9]. А с учетом положительного влияния аллельных вариантов Glu-D1d (5+10) и Glu-A1b (Ax2*) HMW-GS на повышение мукомольно-хлебопекарных качеств, конкурентного преимущества Glu-A1b над Glu-A1a (Ax1), и отрицательного влияния аллелей Glu-D1a (2+12) и Glu-A1c (Axnull), приводящих к снижению хлебопекарных свойств пшеницы, одной из наиболее хозяйственно-ценных комбинаций HMW субъединиц глютенинов, ассоциированных с высокими качествами зерна, является желаемая для селекции комбинация Ax2*/5+10 [4].
Развитие высокоточных подходов к оценке аллельного полиморфизма Waxy-генов и HMW субъединиц глютенинов пшеницы на основе молекулярно-генетических методов диагностики – востребованная для маркер-вспомогательной селекции область исследования, достоверность генотипирования в которой является фактором, предопределяющим эффективность селекционной работы.
Основной целью настоящей работы являлось изыскание молекулярных подходов к идентификации генотипов Triticum aestivum L. по аллельным вариантам Waxy-генов и HMW субъединиц глютенинов для маркер-вспомогательной селекции сортов яровой пшеницы с высокими мукомольно-хлебопекарными и технологическими свойствами зерна.
Материалы и методы исследования
Молекулярно-генетическим исследованиям было подвергнуто 70 образцов яровой пшеницы селекции ТатНИИСХ на предмет идентификации генотипов по аллельным вариантам Waxy-генов и HMW субъединиц глютенинов методами ПЦР, ПЦР-ПДРФ и прямого секвенирования амплифицированной ДНК.
Экстракция геномной ДНК из зерновок яровой пшеницы молочно-восковой спелости осуществлена коммерческим набором «ДНК-сорб С» («ЦНИИ эпидемиологии», Россия).
Амплификация геномной ДНК выполнена на термоциклерах «Терцик» («ДНК-технология», Россия), «PTC-200» («MJ Research», Канада) и «MyCycler» с градиентом («Bio-Rad», США), с последующим проведением, в ряде случаев, этапа ПДРФ-анализа.
Перечень использованных праймеров и условия проведения ПЦР- и ПЦР-ПДРФ-анализа для идентификации аллелей генов Waxy и HMW-GS представлены в таблице 1.
Таблица 1
Перечень использованных праймеров и условия проведения ПЦР-
и ПЦР-ПДРФ-анализа для идентификации аллелей генов Waxy и HMW-GS
|
Наименования праймеров и их нуклеотидные последовательности |
Локус |
Режимы ПЦР-амплификации |
ПДРФ-анализ |
|
4F: 5/-AAGAGCAACTACCAGT-3/ 4R: 5/-TCGTACCCGTCGATGAAGTCGA-3/ |
Wx-A1 Wx-B1 Wx-D1 |
×1: 94 0С – 4 мин. ×40: 94 0С – 30 сек, 58 0С – 30 сек, 72 0С – 30 сек. ×1: 72 0С – 7 мин. |
AcsI 50 0C 3 часа |
|
4F-c: 5/-CCCCCAAGAGCAACTACCAGT-3/ 4R: 5/-TCGTACCCGTCGATGAAGTCGA-3/ |
Wx-A1 Wx-B1 Wx-D1 |
×1: 94 0С – 4 мин. ×40: 94 0С – 30 сек, 64 0С – 30 сек, 72 0С – 30 сек. ×1: 72 0С – 7 мин. |
AcsI 50 0C 3 часа |
|
Wx-A1L: 5/-CCCCAAAGCAAAGCAGGAAAC-3/ Wx-A1R: 5/-CGGCGTCGGGTCCATAGATC-3/ |
Wx-A1 |
×1: 94 0С – 4 мин. ×40: 94 0С – 45 сек, 55 0С – 30 сек, 72 0С – 1 мин. ×1: 72 0С – 7 мин. |
HindIII 37 0C 3 часа |
|
Wx-A2L: 5/-CGCAGGGGAAGACGTGGT-3/ Wx-A2R: 5/-CGTTGACGATGCCGGTGATC-3/ |
Wx-A1 |
×1: 94 0С – 4 мин. ×40: 94 0С – 30 сек, 65 0С – 30 сек, 72 0С – 30 сек. ×1: 72 0С – 7 мин. |
|
|
Wx-B1L: 5/-CGCAGGGGAAGACGTGGT-3/ Wx-B1R: 5/-CGTTGACGATGCCGGTGATG-3/ |
Wx-B1 |
×1: 94 0С – 4 мин. ×40: 94 0С – 45 сек, 65 0С – 40 сек, 72 0С – 50 сек. ×1: 72 0С – 7 мин. |
|
|
Wx-B1L: 5/-CGCAGGGGAAGACGTGGT-3/ Wx-B2R: 5/-CGTTGACGATGCCGGTGTTG-3/ |
Wx-B1 |
×1: 94 0С – 4 мин. ×40: 94 0С – 45 сек, 65 0С – 40 сек, 72 0С – 50 сек. ×1: 72 0С – 7 мин. |
|
|
Wx-D1L: 5/-GCCGACGTGAAGAAGGTGGTG-3/ Wx-D1R: 5/-CCCCTTGCGTCATTTGTTGTGT-3/ |
Wx-D1 |
×1: 94 0С – 4 мин. ×40: 94 0С – 45 сек, 55 0С – 30 сек, 72 0С – 1 мин. ×1: 72 0С – 7 мин. |
|
|
UMN19F: 5/-CGAGACAATATGAGCAGCAAG-3/ UMN19R: 5/-CTGCCATGGAGAAGTTGGA-3/ |
Glu-A1 (Ax1/Axnull, Ax2*) |
×1: 94 0С – 4 мин. ×40: 94 0С – 30 сек, 60 0С – 30 сек, 72 0С – 30 сек. ×1: 72 0С – 5 мин. |
HaeIII 37 0C 3 часа |
|
Axnull-F: 5/-ACGTTCCCCTACAGGTACTA-3/ Axnull-R: 5/-TATCACTGGCTAGCCGACAA-3/ |
Glu-A1 (Axnull) |
×1: 94 0С – 4 мин. ×40: 94 0С – 1 мин, 58 0С – 1 мин, 72 0С – 1 мин. ×1: 72 0С – 7 мин |
|
|
UMN25F: 5/-GGGACAATACGAGCAGCAAA-3/ UMN25R: 5/-CTTGTTCCGGTTGTTGCCA-3/ |
Glu-D1 (Dx2, Dx5) |
×1: 94 0С – 4 мин. ×40: 94 0С – 30 сек, 60 0С – 30 сек, 72 0С – 30 сек. ×1: 72 0С – 5 мин. |
HaeIII 37 0C 3 часа |
|
Dx5-1: 5/-GCCTAGCAACCTTCACAATC-3/ Dx5-2: 5/-GAAACCTGCTGCGGACAAG-3/ |
Glu-D1 (Dx2, Dx5) |
×1: 94 0С – 4 мин. ×40: 94 0С – 30 сек, 63 0С – 30 сек, 72 0С – 30 сек. ×1: 72 0С – 5 мин. |
|
|
UMN26F: 5/-CGCAAGACAATATGAGCAAACT-3/ UMN26R: 5/-TTGCCTTTGTCCTGTGTGC-3/ |
Glu-D1 (Dy10, Dy12) |
×1: 94 0С – 4 мин. ×40: 94 0С – 30 сек, 60 0С – 30 сек, 72 0С – 30 сек. ×1: 72 0С – 7 мин. |
HaeIII 37 0C 3 часа |
|
Dy10/12-F: 5/-GTTGGCCGGTCGGCTGCCATG-3/ Dy10/12-R: 5/-TGGAGAAGTTGGATAGTACC-3/ |
Glu-D1 (Dy10, Dy12) |
×1: 94 0С – 4 мин. ×40: 94 0С – 30 сек, 65 0С – 30 сек, 72 0С – 30 сек. ×1: 72 0С – 5 мин. |
|
Детекция результатов ПЦР- и ПЦР-ПДРФ-анализа выполнена методом горизонтального электрофореза в 2–3 % агарозном геле в буфере ТBE (рН 8,0), содержащем этидий бромид с последующей визуализацией результатов в ультрафиолетовом трансиллюминаторе (λ=310 нм).
Размеры фрагментов ДНК оценены по подвижности в сравнении со стандартными ДНК маркерами.
В работе использованы реактивы для молекулярно-биологических исследований производства ООО «СибЭнзим» (Россия) и ООО «Биотех-Индустрия» (Россия).
Секвенирование продуктов амплификации Wx-A1-локуса Waxy-гена линий яровой пшеницы Kk-71/06-3 (GenBank A/N: JX649155), Kk-11/06-10 (GenBank A/N: JX649156), Kk-11/06-11 (GenBank A/N: JX649157) и Kk-69/06-1 (GenBank A/N: JX649158) селекции ТатНИИСХ проведено на генетическом анализаторе «ABI PRISM 3100» (Applied. Biosystems, США) в НПК «Синтол» (Россия).
Выравнивание частичных нуклеотидных последовательностей аллельных вариантов генов Waxy и HMW-GS: CLUSTAL W (v. 1.83) и BLAST.
Результаты исследования и их обсуждение
Одним из подходов к идентификации аллельных вариантов Waxy-генов пшеницы является общепринятый способ проведения ПЦР с олигонуклеотидными праймерами 4F: 5/-AAGAGCAACTACCAGT-3/ и 4R: 5/-TCGTACCCGTCGATGAAGTCGA-3/, инициирующими амплификацию соответствующих аллельспецифичных продуктов Wx-A1-, Wx-B1- и Wx-D1-локусов [5, 7].
Существенным недостатком данного способа проведения ПЦР является невозможность идентификации нуль-аллеля Wx-B1b от активного аллеля Wx-B1e, а также трудность дискриминации Wx-A1a от Wx-A1g.
Для более эффективной аллельной дискриминации Waxy-генов, нами был разработан оригинальный способ ПЦР- и ПЦР-ПДРФ-генотипирования, отличающийся от прототипа тем, что на этапе ПЦР используют другой прямой праймер 4F-с: 5/-СССССAAGAGCAACTACCAGT-3/, и после этапа ПЦР проводят процедуру ПДРФ-анализа с эндонуклеазным расщеплением ампликонов рестриктазой AcsI.
В части аллельной дискриминации Wx-A1g от Wx-A1a, оригинальность разработанного нами способа генотипирования заключается в реконструкции прямого праймера 4F путем наращивания его 5/-концевого участка пятизвенным oligo (dC)5 блоком, для выравнивания температур плавлений реконструированного (4F-c) и обратного (4R) праймеров с целью подбора оптимальной температуры отжига, равной 64 0C. А принцип дискриминации данных аллелей основан на учете, как отсутствия ПЦР-продукта размером 262 bp в разработанном нами способе генотипирования с праймерами 4F-c и 4R (рис. 1a, треки 5-7), так и наличия амплифицированного фрагмента локуса Wx-A1g размером 257 bp в постановке ПЦР с праймерами 4F и 4R (рис. 1b, треки 5-7).
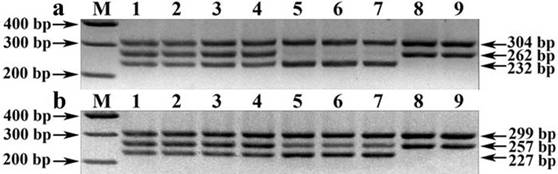
Рис. 1. Электрофореграмма технического результата предложенного способа проведения ПЦР и прототипа для комплексной идентификации
аллельных вариантов Waxy-генов пшеницы
Обозначения: a) Предложенный способ проведения ПЦР (праймеры 4F-c + 4R). b) Прототип (праймеры 4F + 4R). М) ДНК-маркеры 100 bp + 1,5 kb (СибЭнзим); 1-9) генотипы Triticum aestivum L с комбинациями Wx-аллелей: 1-4) Wx-A1a/B1a/D1a; 5-7) Wx-A1g/B1a/D1a; 8-9) Wx-A1a/B1b/D1a.
Таким образом, сочетанием общепринятого и предложенного нами способов генотипирования достигается точность ДНК-анализа в части эффективной аллельной дискриминации Wx-A1g, как от нуль-аллеля Wx-A1b, так и активного аллеля Wx-A1a Waxy-гена. А для эффективной дискриминации нулевого аллеля Wx-B1b от функционального аллеля Wx-B1e, нами были подобраны условия ПЦР-ПДРФ-анализа с праймерами 4F-c + 4R и эндонуклеазным расщеплением рестриктазой AcsI, приводящие к образованию аллельспецифичных профилей, в частности, с характерным для Wx-B1b-аллеля отсутствием ПДРФ-фрагмента размером 84 bp (рис. 2 a, треки 8-9), или наличием неразрезанного ПЦР-продукта локуса Wx-B1e-аллеля длиной 266 bp из-за отсутствия у него соответствующего сайта рестрикции (R↑AATTY).

Рис. 2. Электрофореграмма результата предложенного способа проведения ПЦР-ПДРФ для комплексной идентификации аллельных вариантов Waxy-генов пшеницы
Обозначения: a) Праймеры 4F-c + 4R. b) Праймеры 4F + 4R. М) ДНК-маркеры 50-100 bp (СибЭнзим). 1) ПЦР-профиль генотипа Triticum aestivum L с комбинацией аллелей Wx-A1a/B1a/D1a; 2-9) AcsI-ПЦР-ПДРФ-профили генотипов Triticum aestivum L с комбинациями Wx-аллелей: 2-4) Wx-A1a/B1a/D1a; 5-7) Wx-A1g/B1a/D1a; 8-9) Wx-A1a/B1b/D1a.
Следует отметить, что технический результат, выраженный в эффективной интерпретации образующихся ПЦР-продуктов (рис. 1) и ПЦР-ПДРФ-фрагментов (рис. 2), был полностью сопоставим с расчетными данными, которые в свою очередь были получены, исходя из анализа выравниваний нуклеотидных последовательностей аллельных вариантов Waxy-генов Triticum aestivum L., AcsI-рестрикционного картирования и расчета генерируемых ПЦР- и AcsI-ПЦР-ПДРФ-профилей (рис. 3).

Рис. 3. Выравнивание фланкируемых с праймерами 4F-c + 4R [4F + 4R] нуклеотидных последовательностей аллельных вариантов Waxy-генов Triticum aestivum L.,
AcsI-рестрикционное картирование и расчет AcsI-ПЦР-ПДРФ-профилей
Разработанный нами способ проведения ПЦР и ПЦР-ПДРФ для идентификации аллельных вариантов waxy-генов пшеницы является изобретением, на которое получен патент Российской Федерации (патент на изобретение RU 2 528 748 C1, опубликовано: 20.09.2014. Бюл. № 26).
Помимо комплексного подхода к идентификации аллельных вариантов одновременно по всем трем локусам Waxy-генов пшеницы, для обоснования достоверности заключения ДНК-тестов дополнительно были протестированы способы генотипирования по отдельно взятым локусам Waxy-генов пшеницы [7, 8] с праймерами: Wx-A1L + Wx-A1R и Wx-A2L + Wx-A2R (Wx-A1-локус), с использованием последних также в качестве сиквенсных при расшифровке частичных нуклеотидных последовательностей Wx-A1а- и Wx-A1g-аллелей; Wx-B1L + Wx-B1R и Wx-B1L + Wx-B2R (Wx-В1-локус), Wx-D1L + Wx-D1R (Wx-D1-локус).
Использованный же в работе праймер Wx-B2R является модифицированным нами аналогом Wx-B1R, отличающимся от прототипа «mismatch-нуклеотидом» в третьей позиции с 3/-конца олигонуклеотида, обеспечивающим корректную ПЦР-идентификацию аллельных вариантов Wx-B1-локуса Waxy-гена пшеницы.
Таким образом, при апробации вышеохарактеризованных общепринятых и разработанных нами способов генотипирования на образцах яровой пшеницы селекции ТатНИИСХ удалось провести их молекулярно-генетическую оценку на предмет идентификации генотипов по аллельным вариантам Waxy-генов, в результате которой было установлено, что из 70 происследованных образцов подавляющее большинство растений по классификации типов пшеницы с различным содержанием Waxy-генов относились к 1-му дикому типу (Wx-A1a/B1a/D1a = 65 растений, 92,8 %; Wx-A1g/B1a/D1a = 3 линии, 4,4 %), а 2 линии: Кк-8/06-6 и О-192/03-5 (2,8 %) принадлежали к 3-му типу пшеницы с совокупной комбинацией аллельных вариантов Wx-A1a/B1b/D1a (табл. 2).
Подытоживая результаты молекулярно-генетической оценки 70 образцов яровой пшеницы селекции ТатНИИСХ на предмет идентификации генотипов по аллельным вариантам Waxy-генов, можно вывести заключение, что наиболее перспективными генотипами, рассматриваемыми в качестве исходного материала для дальнейшей селекционной работы по созданию сортов с крахмалом амилопектинового типа являются две линии-носители нулевого Wx-B1b-аллеля (Кк-8/06-6 и О-192/03-5) с последующим введением в их геномы Wx-A1b- и (или) Wx-D1b-аллелей путем скрещивания с соответствующими донорами нуль-аллелей по локусам Waxy-генов пшеницы.
Таблица 2
Молекулярно-генетическая оценка Triticum aestivum L селекции ТатНИИСХ по генам Waxy и HMW-GS
|
№ п. п. |
Сорт/линия |
Waxy |
HMW-GS |
№ п. п. |
Сорт/линия |
Waxy |
HMW-GS |
||||||||||||||||||||
|
A1 |
B1 |
D1 |
A1 |
D1 |
A1 |
B1 |
D1 |
A1 |
D1 |
||||||||||||||||||
|
a |
b |
g |
a |
b |
e |
a |
b |
Ax1 |
Ax2* |
5+10 |
2+12 |
a |
b |
g |
a |
b |
e |
a |
b |
Ax1 |
Ax2* |
5+10 |
2+12 |
||||
|
1 |
Казанская Юбилейная |
+ |
– |
– |
+ |
– |
– |
+ |
– |
– |
+ |
– |
+ |
36 |
Казанская Юбилейная (неполег.) |
+ |
– |
– |
+ |
– |
– |
+ |
– |
– |
+ |
– |
+ |
|
2 |
К-109/02-5 |
+ |
– |
– |
+ |
– |
– |
+ |
– |
– |
+ |
– |
+ |
37 |
К-23/00-3 |
+ |
– |
– |
+ |
– |
– |
+ |
– |
– |
+ |
+ |
– |
|
3 |
Экада 97 |
+ |
– |
– |
+ |
– |
– |
+ |
– |
– |
+ |
– |
+ |
38 |
К-414/01-1 |
+ |
– |
– |
+ |
– |
– |
+ |
– |
+ |
– |
+ |
– |
|
4 |
К-100/03-2 |
+ |
– |
– |
+ |
– |
– |
+ |
– |
– |
+ |
+ |
– |
39 |
К-21/00 |
+ |
– |
– |
+ |
– |
– |
+ |
– |
– |
+ |
+ |
– |
|
5 |
К-18/03-8 |
+ |
– |
– |
+ |
– |
– |
+ |
– |
– |
+ |
+ |
– |
40 |
К-58/01-2 |
+ |
– |
– |
+ |
– |
– |
+ |
– |
– |
+ |
+ |
– |
|
6 |
К-68/04-5 |
+ |
– |
– |
+ |
– |
– |
+ |
– |
– |
+ |
+ |
– |
41 |
K-48/04-2 |
+ |
– |
– |
+ |
– |
– |
+ |
– |
– |
+ |
+ |
– |
|
7 |
К-130/04-10 |
+ |
– |
– |
+ |
– |
– |
+ |
– |
– |
+ |
+ |
– |
42 |
K-106/01-2 |
+ |
– |
– |
+ |
– |
– |
+ |
– |
– |
+ |
– |
+ |
|
8 |
Злата |
+ |
– |
– |
+ |
– |
– |
+ |
– |
– |
+ |
+ |
– |
43 |
K-101/04-3 |
+ |
– |
– |
+ |
– |
– |
+ |
– |
– |
+ |
+ |
– |
|
9 |
К-88/02-19 |
+ |
– |
– |
+ |
– |
– |
+ |
– |
– |
+ |
+ |
– |
44 |
K-112/04-2 |
+ |
– |
– |
+ |
– |
– |
+ |
– |
+ |
– |
+ |
– |
|
10 |
К-6/01-2 |
+ |
– |
– |
+ |
– |
– |
+ |
– |
– |
+ |
+ |
– |
45 |
K-134/04-19 |
+ |
– |
– |
+ |
– |
– |
+ |
– |
+ |
– |
+ |
– |
|
11 |
К-5/03-6 |
+ |
– |
– |
+ |
– |
– |
+ |
– |
– |
+ |
– |
+ |
46 |
К-51/00-3 |
+ |
– |
– |
+ |
– |
– |
+ |
– |
+ |
– |
+ |
– |
|
12 |
К-48/03 |
+ |
– |
– |
+ |
– |
– |
+ |
– |
+ |
– |
+ |
– |
47 |
K-133/05-5 |
+ |
– |
– |
+ |
– |
– |
+ |
– |
– |
+ |
+ |
– |
|
13 |
К-100/03-8 |
+ |
– |
– |
+ |
– |
– |
+ |
– |
– |
+ |
– |
+ |
48 |
K-57/05-6 |
+ |
– |
– |
+ |
– |
– |
+ |
– |
+ |
– |
+ |
– |
|
14 |
К-21/02-5 |
+ |
– |
– |
+ |
– |
– |
+ |
– |
– |
+ |
– |
+ |
49 |
К-117/04-4 |
+ |
– |
– |
+ |
– |
– |
+ |
– |
– |
+ |
+ |
– |
|
15 |
К-46/04-9 |
+ |
– |
– |
+ |
– |
– |
+ |
– |
– |
+ |
+ |
– |
50 |
К-12/04 |
+ |
– |
– |
+ |
– |
– |
+ |
– |
– |
+ |
– |
+ |
|
16 |
К-68/04-1 |
+ |
– |
– |
+ |
– |
– |
+ |
– |
– |
+ |
+ |
– |
51 |
К-99/05-2 |
+ |
– |
– |
+ |
– |
– |
+ |
– |
– |
+ |
– |
+ |
|
17 |
К-23/04-1 |
+ |
– |
– |
+ |
– |
– |
+ |
– |
– |
+ |
+ |
– |
52 |
Кк-8/06-1 |
+ |
– |
– |
+ |
– |
– |
+ |
– |
– |
+ |
– |
+ |
|
18 |
К-49/04 |
+ |
– |
– |
+ |
– |
– |
+ |
– |
+ |
– |
+ |
– |
53 |
Кк-71/06-3 |
+ |
– |
– |
+ |
– |
– |
+ |
– |
– |
+ |
+ |
– |
|
19 |
К-7/04-2 |
+ |
– |
– |
+ |
– |
– |
+ |
– |
– |
+ |
+ |
– |
54 |
Кк-8/06-6 |
+ |
– |
– |
– |
+ |
– |
+ |
– |
– |
+ |
– |
+ |
|
20 |
Экада 113 |
+ |
– |
– |
+ |
– |
– |
+ |
– |
– |
+ |
– |
+ |
55 |
Кк-75/06-3 |
+ |
– |
– |
+ |
– |
– |
+ |
– |
– |
+ |
+ |
– |
|
21 |
Экада 109 |
+ |
– |
– |
+ |
– |
– |
+ |
– |
– |
+ |
+ |
– |
56 |
Кк-11/06-11 |
– |
– |
+ |
+ |
– |
– |
+ |
– |
– |
+ |
+ |
– |
|
22 |
К-93/05-2 |
+ |
– |
– |
+ |
– |
– |
+ |
– |
+ |
– |
+ |
– |
57 |
Кк-11/06-10 |
– |
– |
+ |
+ |
– |
– |
+ |
– |
– |
+ |
+ |
– |
|
23 |
К-29/02-5 |
+ |
– |
– |
+ |
– |
– |
+ |
– |
+ |
– |
+ |
– |
58 |
Кк-69/06-4 |
+ |
– |
– |
+ |
– |
– |
+ |
– |
– |
+ |
– |
+ |
|
24 |
К-109/02-13 |
+ |
– |
– |
+ |
– |
– |
+ |
– |
– |
+ |
|
+ |
59 |
Кк-6/07-2 |
+ |
– |
– |
+ |
– |
– |
+ |
– |
– |
+ |
+ |
– |
|
25 |
К-20/02-2 |
+ |
– |
– |
+ |
– |
– |
+ |
– |
– |
+ |
+ |
– |
60 |
Кк-69/06-1 |
– |
– |
+ |
+ |
– |
– |
+ |
– |
– |
+ |
– |
+ |
|
26 |
К-73/03-4 |
+ |
– |
– |
+ |
– |
– |
+ |
– |
– |
+ |
+ |
– |
61 |
Кк-71/06-8 |
+ |
– |
– |
+ |
– |
– |
+ |
– |
– |
+ |
+ |
– |
|
27 |
К-68/04-4 |
+ |
– |
– |
+ |
– |
– |
+ |
– |
– |
+ |
+ |
– |
62 |
Кк-75/06-5 |
+ |
– |
– |
+ |
– |
– |
+ |
– |
– |
+ |
– |
+ |
|
28 |
К-100/03-9 |
+ |
– |
– |
+ |
– |
– |
+ |
– |
– |
+ |
– |
+ |
63 |
О-192/03-5 |
+ |
– |
– |
– |
+ |
– |
+ |
– |
– |
+ |
– |
+ |
|
29 |
К-7/04-1 |
+ |
– |
– |
+ |
– |
– |
+ |
– |
– |
+ |
– |
+ |
64 |
О-25/05-2 |
+ |
– |
– |
+ |
– |
– |
+ |
– |
|
+ |
– |
+ |
|
30 |
К-65/05-2 |
+ |
– |
– |
+ |
– |
– |
+ |
– |
+ |
– |
+ |
– |
65 |
О-206/05-2, |
+ |
– |
– |
+ |
– |
– |
+ |
– |
+ |
– |
+ |
– |
|
31 |
К-11/04-8 |
+ |
– |
– |
+ |
– |
– |
+ |
– |
– |
+ |
– |
+ |
66 |
О-186/04-1 |
+ |
– |
– |
+ |
– |
– |
+ |
– |
– |
+ |
+ |
– |
|
32 |
Экада 66 |
+ |
– |
– |
+ |
– |
– |
+ |
– |
– |
+ |
+ |
– |
67 |
О-464/02-2 |
+ |
– |
– |
+ |
– |
– |
+ |
– |
– |
+ |
– |
+ |
|
33 |
К-27/00-2 |
+ |
– |
– |
+ |
– |
– |
+ |
– |
– |
+ |
+ |
– |
68 |
О-513/00-21 |
+ |
– |
– |
+ |
– |
– |
+ |
– |
+ |
– |
– |
+ |
|
34 |
К-65/05-1 |
+ |
– |
– |
+ |
– |
– |
+ |
– |
+ |
– |
+ |
– |
69 |
Эр.255/00-3-1 |
+ |
– |
– |
+ |
– |
– |
+ |
– |
– |
+ |
– |
+ |
|
35 |
Симбирцит |
+ |
– |
– |
+ |
– |
– |
+ |
– |
– |
+ |
+ |
– |
70 |
О-28/05-2 |
+ |
– |
– |
+ |
– |
– |
+ |
– |
– |
+ |
– |
+ |
|
Примечание: |
+ |
– наличие соответствующего аллеля |
– |
– отсутствие соответствующего аллеля |
Следующим этапом исследования являлась апробация разработанного нами способа проведения ПЦР-ПДРФ для идентификации аллельных вариантов Glu-A1- и Glu-D1-локусов HMW субъединиц глютенинов пшеницы, ближайшим аналогом которого послужил способ генотипирования, предложенный Лиу с соавт. в 2008 г. [4].
Прототип заявленного способа генотипирования, предусматривающий идентификацию аллельных вариантов HMW субъединиц глютенинов пшеницы с тремя наборами праймеров: UMN19F + UMN19R (Ax1/Axnull- и Ax2*-аллели), UMN25F + UMN25R (Dx2- и Dx5-аллели) и UMN26F + UMN26R (Dy10- и Dy12-аллели), в основном был рассчитан авторами на детекцию полученных результатов ПЦР преимущественно методами капиллярного или вертикального гель-электрофореза в ПААГ [4].
Отличительным признаком предложенного нами способа генотипирования от вышесказанного прототипа являлось, как введение дополнительного этапа ПДРФ-анализа с эндонуклеазным расщеплением ампликонов рестриктазой HaeIII, так и последующая детекция результатов анализа методом горизонтального электрофореза в агарозном геле.
В результате же практических исследований, направленных на апробацию разработанного нами способа проведения ПЦР-ПДРФ, был получен технический результат, обеспечивавший эффективную идентификацию аллельных вариантов HMW субъединиц глютенинов пшеницы, благодаря корректной интерпретации генерируемых ПЦР-ПДРФ-фрагментов при их электрофорезной детекции в агарозном геле (рис. 4-6),
Следует отметить, что результаты генотипирования визуально были сопоставимы с расчетными данными, полученными, в свою очередь, исходя из анализа выравниваний соответствующих нуклеотидных последовательностей с HaeIII-рестрикционным картированием и расчета генерируемых ПЦР- и HaeIII-ПЦР-ПДРФ-профилей.
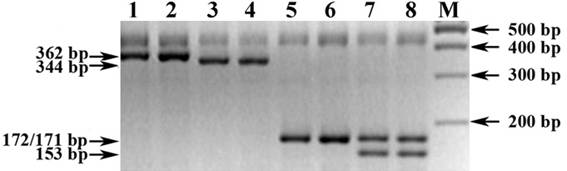
Рис. 4. Электрофореграмма результата ПЦР-анализа и предложенного способа проведения ПЦР-ПДРФ для идентификации аллельных вариантов Ax1/Axnull и Ax2* Glu-A1-локуса HMW-GS пшеницы (праймеры UMN19F + UMN19R)
Обозначения: 1-4) ПЦР-анализ (прототип): 1-2) Axl-/Axnull-аллели (362 bp); 3-4) Ax2*-аллель (344 bp). 5-8) HaeIII-ПЦР-ПДРФ-анализ (предложенный способ): 5-6) Ax1-/Axnull-аллели (172/171/19 bp); 7-8) Ax2*-аллель (172/153/19 bp). М) ДНК-маркеры 100 bp (СибЭнзим)
Так, в результате апробации разработанного нами способа проведения ПЦР-ПДРФ с первым набором праймеров UMN19F + UMN19R и эндонуклеазным расщеплением рестриктазой HaeIII, регистрировались ПЦР-ПДРФ-профили, характерные как для аллельных вариантов Ax1/Axnull (172/171/19 bp), так и для Ax2*-аллеля (172/153/19 bp) Glu-A1-локуса HMW субъединиц глютеиинов пшеницы (рис. 4, треки 5-8), запечатленные вместе с цельными ПЦР-продуктами (рис. 4, треки 1-4) на соответствующей электрофореграмме.
А в результате апробации предложенного способа проведения ПЦР-ПДРФ со вторым набором праймеров UMN25F + UMN25R и эндонуклеазным расщеплением HaeIII визуализировались ПЦР-ПДРФ-профили аллельных вариантов Dx2 (171/109/19 bp) и Dx5 (171/91/19 bp) Glu-D1-локуса HMW субъединиц глютеиинов пшеницы (рис. 5, треки 5-8), тоже запечатленные вместе с неразрезанными ПЦР-продуктами данных аллелей (рис. 5, треки 1-4) на соответствующей электрофореграмме.
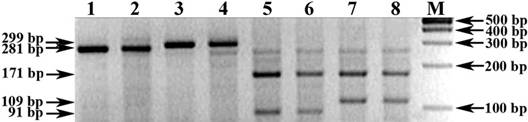
Рис. 5. Электрофореграмма результата ПЦР-анализа и предложенного способа проведения ПЦР-ПДРФ для идентификации аллельных вариантов Dx2 и Dx5 Glu-D1-локуса HMW-GS пшеницы (праймеры UMN25F + UMN25R)
Обозначения: 1-4) ПЦР-анализ (прототип): 1-2) Dx5-аллель (281 bp); 3-4).Dx2-аллель (299 bp). 5-8) HaeIII-ПЦР-ПДРФ-анализ (предложенный способ): 5-6) Dx5-аллель (171/91/19 bp); 7-8) Dx2-аллель (171/109/19 bp). М) ДНК-маркеры 100 bp (СибЭнзим)
В результате же постановки ПЦР-ПДРФ с третьим набором праймеров UMN26F + UMN26R и рестрикцией ферментом HaeIII, нами также были зарегистрированы аллельспецифичные профили (Dy10 = 223/174 bp; Dy12 = 241/174 bp) Glu-D1-локуса HMW-GS (рис. 6, треки 5-8), репрезентативно визуализированные вместе с соответствующими цельными ПЦР-продуктами (рис. 6, треки 1-4) на представленной ниже электрофореграмме.
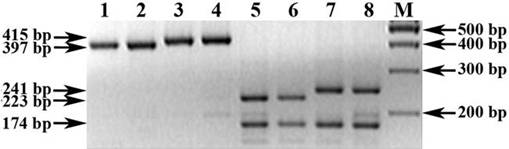
Рис. 6. Электрофореграмма результата ПЦР-анализа и предложенного способа проведения ПЦР-ПДРФ для идентификации аллельных вариантов Dy10 и Dy12 Glu-D1-локуса HMW-GS пшеницы (праймеры UMN26F + UMN26R)
Обозначения: 1-4) ПЦР-анализ (прототип): 1-2) Dy10-аллель (397 bp); 3-4) Dy12-аллель (415 bp). 5-8) HaeIII-ПЦР-ПДРФ-анализ (предложенный способ): 5-6) Dy10-аллель (223/174 bp); 7-8) Dy12-аллель (241/174 bp). М) ДНК-маркеры 100 bp (СибЭнзим).
Так, именно введением дополнительного этапа ПДРФ-анализа с HaeIII-эндонуклеазным расщеплением амплифицируемых ПЦР-продуктов, инциируемых тремя различными парами праймеров (UMN19F + UMN19R, UMN25F + UMN25R и UMN26F + UMN26R), удалось адаптировать детекцию результатов анализа методом горизонтального электрофореза в агарозном геле.
Низко-дискретные цельные ПЦР-продукты, практически также можно анализировать методом горизонтального электрофореза в агарозном геле, однако, ввиду высокого риска негативного влияния эффекта «улыбки» с геометрическим искажением электрофорезной картины, все же для этой цели предпочтительней использовать методы капиллярного или вертикального гель-электрофореза в ПААГ, как ранее и было предусмотрено авторами данных протоколов генотипирования [4].
Для обоснования достоверности заключения ДНК-тестов, также в ходе исследования были дополнительно протестированы и другие общепринятые способы ПЦР-идентификации: Axnull Glu-A1-локуса c праймерами Axnull-F + Axnull-R [3], Dx5 и Dx2 Glu-D1-локуса с праймерами Dx5-1 + Dx5-2 [1], Dy10 и Dy12 Glu-D1-локуса HMW-GS с праймерами Dy10/12-F + Dy10/12-R [6].
Молекулярно-генетической оценкой генотипов пшеницы по аллельным вариантам HMW субъединиц глютенинов выяснено, что по Glu-A1-локусу HMW-GS подавляющее большинство растений (57 образцов, 81,4 %) имели субъединицу Ax2*, кодируемую аллельным вариантом Glu-A1b (Ax2*-аллель), а остальные 13 генотипов (18,6 %) – субъединицу Ax1, кодируемую аллельным вариантом Glu-A1a (Ax1-аллель); по Glu-D1-локусу HMW-GS 44 растения (62,9 %) являлись носителями комбинации субъединиц Dx5 и Dy10 (5+10), кодируемой аллельным вариантом Glu-D1d (Dx5- и Dy10-аллели), а 26 образцов (37,1 %) характеризовались наличием комбинации субъединиц Dx2 и Dy12 (2+12), кодируемой аллельным вариантом GluD1a (Dx2- и Dy12-аллели) (табл. 2). При оценке же распределения происследованных генотипов Triticum aestivum L. по совокупной комбинации Glu-A1/D1-локусов HMW субъединиц глютенинов (Ax1/5+10 = 12 (17,1 %); Ax1/2+12 = 1 (1,4 %); Ax2*/5+10 = 32 (45,7 %); Ax2*/2+12 = 25 (35,7 %)) нами было установлено преобладание желаемой для селекции на мукомольно-хлебопекарные качества зерна комбинации субъединиц Ax2*/5+10.
Заключение
Таким образом, разработанные и апробированные нами способы генотипирования Triticum aestivum L. по аллельным вариантам Waxy-генов и HMW субъединиц глютенинов обеспечили эффективное проведение корректной молекулярно-генетической оценки 70 исследуемых образцов (62 линий и 8 сортов) яровой пшеницы селекции ТатНИИСХ.
Рецензенты:Гайнуллина М.К., д.с.-х.н., профессор, зав. кафедрой технологии производства и переработки сельскохозяйственной продукции Казанской государственной академии ветеринарной медицины имени Н. Э. Баумана, г. Казань;
Якупов Т.Р., д.в.н., доцент кафедры биологической и неорганической химии Казанской государственной академии ветеринарной медицины имени Н. Э. Баумана, г. Казань.
Библиографическая ссылка
Вафин Р.Р., Абдулина И.Р., Вафин Р.Р., Абдулина И.Р., Ржанова И.В., Ржанова И.В., Гараева А.Л., Тюлькин С.В., Асхадуллин Д.Ф., Асхадуллин Д.Ф., Василова Н.З., Зайнуллин Л.И., Алимова Ф.К., Шагалиева Г.И. МОЛЕКУЛЯРНЫЕ ПОДХОДЫ К ИДЕНТИФИКАЦИИ ГЕНОТИПОВ TRITICUM AESTIVUM L. ПО АЛЛЕЛЬНЫМ ВАРИАНТАМ WAXY-ГЕНОВ И HMW СУБЪЕДИНИЦ ГЛЮТЕНИНОВ // Современные проблемы науки и образования. 2015. № 2-1. ;URL: https://science-education.ru/en/article/view?id=18593 (дата обращения: 12.05.2026).



