Scientific journal
Modern problems of science and education
ISSN 2070-7428
"Перечень" ВАК
ИФ РИНЦ = 0,936
STUDY OF REPRODUCTIVE TOXICITY OF PROMISING NEW MEDICINAL PRODUCT «11-DEOXY MISOPROSTOL»
Проблема безопасности лекарственных средств становится все более актуальной во всем мире. Это связано, прежде всего, с внедрением в широкую медицинскую практику большого числа фармакологических препаратов с высокой биологической активностью, сенсибилизацией населения к биологическим и химическим веществам, нерациональным использованием лекарств, медицинскими ошибками и применением некачественных лекарственных препаратов [2, 9]. Одним из обязательных этапов доклинических исследований новых лекарственных средств является изучение их репротоксического действия. Под репродуктивной токсичностью фармакологических средств понимают эмбрио- и фетотоксическое действие в антенатальном и постнатальном периоде развития, а также влияние на генеративную функцию организма [6].
Исследуемое вещество, 11-дезоксимизопростол (11 - ДМП) - этиловый эфир (±)-11,15-дидезокси-16-метил-16-гидроксипростагландина E1 (рисунок 1), проявляющее утеротоническую активность.
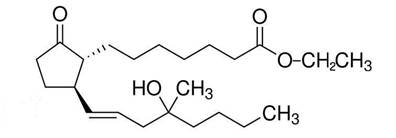
Рис. 1. Этиловый эфир (±)-11,15-дидезокси-16-метил-16-гидроксипростагландина E1(11-дезоксимизопростол)
Это соединение относится к ряду 11-дезоксипростагландинов и близко по химическому строению с мизопростолом. Будучи химически более стабильным и в 2 раза менее токсичным, оно превосходит мизопростол по утеротонической активности, что, наряду с синтетической доступностью и отсутствием побочных эффектов, делает его исключительно перспективным для внедрения в практику с целью замены мизопростола в гинекологических бинарных препаратах. Описаны синтез [4], противоязвенная и ряд других видов активности соединений 11-дезоксимизопростола [3,7,8]. Кроме того, имеются предварительные сведения о способности 11-ДМП подавлять развитие тяжелого окислительного стресса, который может являться одним из патогенетических звеньев нарушений различных видов обмена веществ [1, 7].
Согласно действующим в настоящее время рекомендациям по доклиническим исследованиям лекарственных средств [5,6], исследования по выявлению репродуктивной токсичности должны включать изучение влияния на репродуктивную (генеративную) функцию; изучение эмбрио- и фетотоксического действия, регистрируемого в антенатальном периоде развития; изучение эмбрио- и фетотоксического действия, регистрируемого в постнатальном периоде развития.
Цель исследования: изучение репродуктивной токсичности лекарственного средства «11-дезоксимизопростол» по его влиянию на генеративную функцию при внутрижелудочном введении.
Материалы и методы
Экспериментальная работа проведена на нелинейных белых самках и самцах крыс. (масса тела 20–22 г). Исследуемое вещество вводили животным в форме суспензии в 1%-ном крахмальном геле. Перед приготовлением суспензии 11-ДМП, таблетки (11-ДМП табл.) растирали в ступке до однородного порошка. Рабочие разведения 11-ДМП табл. готовили в день введения. Животные из групп негативного контроля получали 1% крахмальный гель (плацебо).
Эксперименты выполнены на нелинейных белых крысах массой 190-210 гр. Весь экспериментальный период животных содержали на стандартном рационе. Наблюдение и оценку состояния животных проводили ежедневно: осмотр регистрация среднего потребления воды и пищи, один раз в неделю животных взвешивали. Длительность карантина (акклиматизационного периода) для всех животных составляла четырнадцать (14) дней. В течение карантина проводили ежедневный осмотр каждого животного (поведение и общее состояние), дважды в день животных наблюдали в клетках (заболеваемость и смертность). Клетки с животными были помещены в отдельную комнату. Световой режим: 12 час - свет, 12 час - темнота. Температура воздуха поддерживалась в пределах 20-22 °C, относительная влажность - 60-70%. Температура и влажность воздуха регистрировались ежедневно. Был установлен режим проветривания, обеспечивающий около 15 объемов помещения в час, концентрацию CO2 не более 0.15 объемных %, аммиака - не более 0.001 мг/л. Животных распределяли по группам, используя при рандомизации в качестве основного критерия массу тела (отклонение значений массы тела в пределах группы не более 10%). Количество животных в каждой экспериментальной группе – 20.
Введение препарата производили внутрижелудочно в дозе 10 мг/кг. В каждой группе было по 20 самцов и 20 самок. Введение самцам проводили в течение 48 дней до спаривания с интактными самками. Самкам введение производилось в течение 15 дней до спаривания с интактными самцами.
Таким образом, в эксперименте использовано 6 опытных групп животных:
- Группа 1- 20 самцов, крахмал (контроль), 48 дней
- Группа 2-20 самцов, препарат (10 мг/кг), 48 дней
- Группа 3 - 20 самок, крахмал, 15 дней
- Группа 4 - 20 самок, препарат (10 мг/кг), 15 дней
- Группа 5 - 20 интактных самцов
- Группа 6 - 20 интактных самок
Через 24 часа после окончания введения самок подсаживали к соответствующей группе самцов сроком на 2 эстральных цикла (10 дней). Половину самок вскрывали на 17-21 дни беременности, подсчитывали количество желтых тел, мест имплантации, количество живых и погибших плодов.
Индекс фертильности рассчитывали по следующей формуле:
![]()
За единицу наблюдения при статистической обработке полученных результатов принимали одну самку или один помет. Вторую половину самок оставляли до родов и проводили наблюдение за течением родов и физическим развитием потомства в период вскармливания.
Результаты обрабатывались общепринятыми методами вариационной статистики и выражались в виде среднеарифметической (М) и её стандартной ошибки (m). Применялся критерий непараметрической статистики Манна-Уитни (U). Обработка полученных данных производилась с использованием пакета прикладных программ Statistica 6.
Результаты и обсуждение
В период введения 11-ДМП табл., снижения темпов прироста массы тела, изменений в поведении, гибели животных не отмечалось ни в одной из изучаемых групп самцов или самок. Индекс фертильности достоверно не различался во всех экспериментальных группах (таблица 1).
Таблица 1
Влияние 11-ДМП табл. (10 мг/кг) на плодовитость крыс
|
Показатели |
♂ |
♀ |
|||
|
Группы |
|||||
|
Контроль |
11-ДМП |
Контроль |
11-ДМП |
||
|
Кол-во самок, посаженных с самцами |
20 |
20 |
20 |
20 |
|
|
Кол-во оплодотворенных самок |
20 |
20 |
20 |
20 |
|
|
Кол-во беременных самок |
20 |
20 |
20 |
20 |
|
|
Индекс фертильности, % |
100,0 |
100,0 |
100,0 |
100,0 |
|
При вскрытии самок не было выявлено повышения уровней пред- и постимплантационной смертности в опытных группах по сравнению с соответствующими контрольными группами (таблицы 2 и 3).
Таблица 2
Влияние 11-ДМП табл. (10 мг/кг) на репродуктивную способность крыс самцов
|
Показатели |
Группы |
|
|
Контроль |
11-ДМП |
|
|
Кол-во забеременевших самок |
10 |
10 |
|
Кол-во желтых тел |
11,9 ± 0,8 |
11,7± 0,8 |
|
Кол-во мест имплантации |
11,2 ± 0,6 |
11,1 ± 0,7 |
|
Кол-во живых плодов |
10,9 ± 0,7 |
10,7 ± 0,5 |
Таблица 3
Влияние 11-ДМП табл. (10 мг/кг) на репродуктивную функцию крыс самок
|
Показатели |
Экспериментальные группы |
|
|
Контроль |
11-ДМП |
|
|
Кол-во беременных самок |
10 |
10 |
|
Кол-во желтых тел |
12,8 ± 0,4 |
11,7± 0,5 |
|
Кол-во мест имплантации |
12,1 ± 0,4 |
11,9 ± 0,6 |
|
Кол-во живых плодов |
11,9 ± 0,6 |
10,1 ± 0,5 |
У оставленных рожать самок процесс родов и забота о потомстве были без особенностей. Среднее количество плодов на одну самку, соотношение крысят по полу, уровень гибели новорожденных крысят не изменялись в пометах всех экспериментальных групп. Сроки отлипания ушной раковины, появления первичного волосяного покрова, прорезывания резцов, открывания глаз в пометах как опытных, так и контрольных групп достоверно не различались (таблицы 4 и 5).
Таблица 4
Показатели физического развития потомства крыс-самцов, получавших 11-ДМП табл. (10 мг/кг) в течение 48 дней до спаривания
|
Показатели |
Экспериментальные группы |
|
|
Контроль |
11-ДМП |
|
|
Кол-во пометов |
10 |
10 |
|
Кол-во крысят |
58 |
59 |
|
В т.ч, живых |
58 |
59 |
|
Гибель крысят в период вскармливания (количество) |
3 |
2 |
|
Кол-во самок |
34 |
36 |
|
Кол-во самцов |
24 |
23 |
|
Соотношение полов (самки/самцы) |
1,57 |
1,52 |
|
День отлипания ушной раковины |
4,1 ± 0,2 |
4,2 ± 0,3 |
|
День появления первичного волосяного покрова |
5,8 ± 0,3 |
5,7 ± 0,2 |
|
День прорезывания резцов |
10,8 ± 0,3 |
11,1 ± 0,3 |
|
День открытия глаз |
15,9 ± 0,4 |
16,0 ± 0,4 |
|
День опускания семенников |
28,1 ± 0,3 |
28,6 ± 0,3 |
|
День открытия влагалища |
34,2 ± 0,6 |
33,3 ± 0,5 |
|
масса тела крысят (г) на 4-ый день на 7-ой день на 14-ый день на 21-ый день |
8,28 ± 0,19 14,17 ± 0,30 18,11 ± 1,50 27,61 ± 2,44 |
7,99 ± 0,28 13,05 ± 1,24 21,21 ± 2,40 28,55 ± 2,38 |
|
гибель самок в период вскармливания |
0±0 |
0±0 |
Таблица 5
Показатели физического развития потомства крыс-самок, получавших 11-ДМП табл. (10 мг/кг), в течение 10 дней до спаривания
|
Показатели |
Экспериментальные группы |
|
|
Контроль |
11-ДМП |
|
|
Кол-во пометов |
10 |
10 |
|
Кол-во крысят |
54 |
55 |
|
В т.ч, живых |
52 |
52 |
|
Гибель крысят в период вскармливания |
2 |
1 |
|
Кол-во самок |
31 |
30 |
|
Кол-во самцов |
21 |
22 |
|
Соотношение полов (самцы/самки) |
1,48 |
1,36 |
|
День отлипания ушной раковины |
4,8 ± 0,3 |
4,6 ± 0,2 |
|
День появления первичного волосяного покрова |
5,8 ± 0,3 |
5,6 ± 0,3 |
|
День прорезывания резцов |
11,9 ± 0,4 |
12,1 ± 0,3 |
|
День открытия глаз |
14,2 ± 1,3 |
15,2 ± 1,4 |
|
День опускания семенников |
26,3 ± 0,8 |
25,9 ± 0,9 |
|
День открытия влагалища |
34,2 ± 1,4 |
33,9 ± 1,8 |
|
Масса тела крысят (г) на 4-ый день на 7-ой день на 14-ый день на 21-ый день |
7,90 ± 0,82 12,98 ± 1,13 21,33 ± 1,11 28,91 ± 2,12 |
7,81 ± 0,70 13,21 ± 1,23 22,12 ± 1,15 31,14 ± 2,16 |
|
гибель самок в период вскармливания |
0 |
0 |
Взвешивание крысят на 4-ый, 7-ой, 14-ый и 21-ый дни после родов показало, что масса тела крысят во всех экспериментальных группах достоверно не различалась (таблицы 4 и 5).
Заключение
При изучении репродуктивной токсичности 11-ДМП табл. показано, что препарат не вызывает изменений генеративной функции при внутрижелудочном введении в дозе 10 мг/кг. Не выявлено изменений плодовитости и репродуктивной способности крыс – самцов и самок. Отсутствовали изменения показателей физического развития потомства животных.
Рецензенты:
Зарудий Ф.С., д.м.н., профессор кафедры фармакологии №1 с курсом клинической фармакологии ГБОУ ВПО Башкирский государственный медицинский университет Минздрава РФ, г. Уфа;
Дианов В.М., д.фарм.н., профессор, профессор кафедры фармацевтической химии с курсами аналитической и токсикологической химии ГБОУ ВПО Башкирский государственный медицинский университет Минздрава РФ, г. Уфа.
Библиографическая ссылка
Катаева Р.М., Аглетдинов Э.Ф., Иванова Н.А., Галимова Р.А., Булыгин К.В., Катаев В.В. ИЗУЧЕНИЕ РЕПРОДУКТИВНОЙ ТОКСИЧНОСТИ ПЕРСПЕКТИВНОГО НОВОГО ЛЕКАРСТВЕННОГО СРЕДСТВА «11-ДЕЗОКСИМИЗОПРОСТОЛ» // Современные проблемы науки и образования. 2015. № 1-1. ;URL: https://science-education.ru/en/article/view?id=17128 (дата обращения: 16.05.2026).



