Scientific journal
Modern problems of science and education
ISSN 2070-7428
"Перечень" ВАК
ИФ РИНЦ = 0,936
THE DETERMINATION OF VERAPAMIL IN THE GEL BY THE METHOD OF PLANAR CHROMATOGRAPHY
Цель работы. Разработать методику идентификации и количественного определения верапамила в геле, в 100 г которого содержится 1 г данного вещества.
Материал и методы исследования. В качестве растворителя геля был выбран ацетон. При растворении в ацетоне образуется прозрачный бесцветный раствор. Для хроматографирования использовали пластинки марки «Sorbfil ПТСХ-АФ-В-УФ» для высокоэффективной тонкослойной хроматографии размером 10х15 см. Подвижной фазой служила система растворителей «ацетон - вода очищенная» (8:2) [2]. Хроматографирование проводили в стеклянной камере, насыщенной парами растворителя. Для приготовления стандартного образца (СО) 0,0125 г верапамила (ФС 42-0224-07) (точная навеска) помещали в мерную колбу вместимостью 25,0 мл, растворяли в ацетоне и доводили ацетоном раствор до метки. Концентрация СО верапамила составила 0,5 мкг/мкл.
Приготовление раствора геля: около 1,25 г (точная навеска) геля помещали в мерную колбу вместимостью 25,0 мл, растворяли в ацетоне и доводили ацетоном раствор до метки.
На линию старта хроматографической пластинки длиной 15 см наносили раствор СО с содержанием верапамила 0,5; 0,75; 1,0; 1,25; 1,5; 1,75 мкг в пятне. На этой же пластинке обозначали линии контрольных треков, на которые наносили ацетоновый раствор геля объемом 3,0 мкл. Пробы наносили при помощи микрошприца МШ-10. Пластинки помещали в камеру для хроматографирования объемом 2000 см3, насыщенную парами растворителя. После подъема растворителя на необходимый уровень пластинки вынимали, высушивали в вытяжном шкафу при комнатной температуре до удаления паров растворителя. Длина пробега растворителя около 8 см. Детектирующий реагент - реактив Бушарда. На жёлтом фоне реактива появляются пятна коричневого цвета с Rf 0,58±0,01.
Необходимо учитывать, что пятна очень неустойчивы и после высыхания пластинки обесцвечиваются. Поэтому сразу после проявления в мокром виде пластинки сканировали при помощи планшетного сканера «HP Scanjet 3670» (разрешение 100 dpi) и далее осуществляли ее цифровую обработку с помощью компьютерной программы «Видеоденситометр Sorbfil» (г. Краснодар).
Количественное определение проводили методом абсолютной калибровки (внешнего стандарта), по градуировочному графику зависимости «масса вещества - площадь пика» (линейная аппроксимация). Статистическая обработка результатов проводилась в соответствии с ОФС «Статистическая обработка результатов химического эксперимента и биологических испытаний» [1].
Результаты исследования и их обсуждение
Определение хроматографических характеристик.
Чувствительность детектирующего реагента устанавливали по величине предела обнаружения (ПО), который рассчитывали с учётом стандартного отклонения сигнала и углового коэффициента градуировочного графика. ПО составляет 0,4 мкг. Специфичность определяли по величине Rf пятна контрольного трека, которая должно соответствовать Rf пятен стандартного образца (0,58±0,01). На треках контрольного образца визуально обнаруживалось пятно коричневого цвета с Rf, соответствующей стандартным образцам (рис. 1, 2).
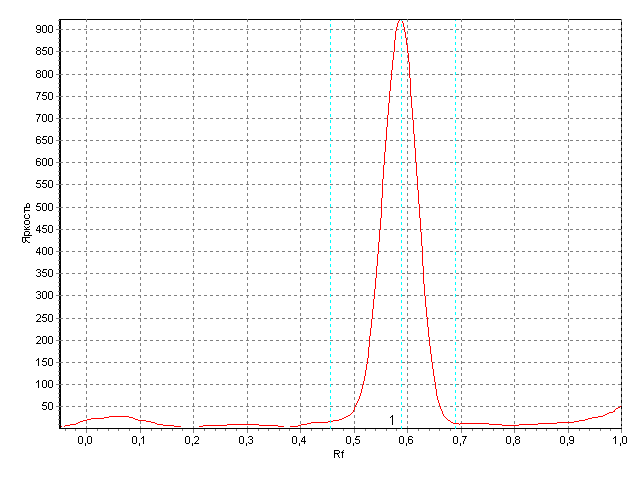
Рис. 1. Хроматограмма СО верапамила.
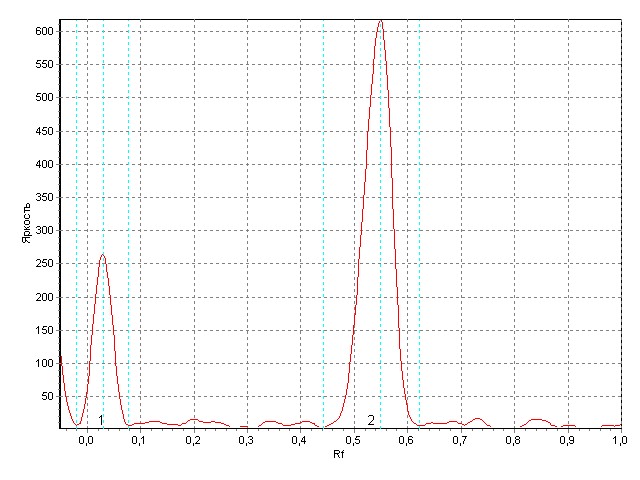
Рис. 2. Хроматограмма ацетонового раствора геля (2 - верапамил).
Эффективность пластинки около 800 теоретических тарелок.
Валидация методики количественного анализа проведена по следующим критериям: чувствительность количественного определения, линейность, правильность и сходимость результатов [5].
Линейность устанавливали по градуировочным графикам, полученным при компьютерной обработке хроматограмм в координатах площадь пика (S) - масса (m, мкг). Под площадью пика в видеоденситометрии понимается интегральная характеристика, включающая собственно площадь пятна, его объём в пространстве и интенсивность его окраски [3]. По данным градуировочных графиков рассчитывали статистические характеристики и коэффициент корреляции. Методом наименьших квадратов определяли значимость свободного члена линейной зависимости (а), углового коэффициента (b) и чувствительность количественного определения. Расчеты проводили с помощью программы Microsoft Excel. В диапазоне концентраций 0,5-2,0 мкг в пятне наблюдается прямолинейная зависимость. Градуировочный график описывается уравнением S=1,69.104 m, коэффициент корреляции r = 0,995 (рис. 3).
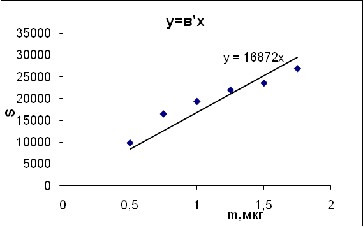
Рис. 3. Градуировочный график верапамила.
Предел количественного определения (quantitation limit), рассчитанный по величине стандартного отклонения сигнала и углового коэффициента градуировочного графика, составляет 1,2 мкг.
Правильность методики определяли методом «введено-найдено». По уравнению градуировочного графика рассчитывали содержание верапамила на 5 уровнях концентраций СО и определяли метрологические характеристики (табл. 1).
Таблица 1
Оценка правильности определения верапамила
|
Уровень |
Взято, мкг |
Найдено, мкг |
Открываемость, % |
Метрологические характеристики |
|
1 |
1,0 |
1,03 |
103 |
Хср = 101 SD = 1,67 ΔX=3,77 RSD = 5,22% Е% =3,73% |
|
1 |
1,0 |
1,12 |
112 |
|
|
2 |
1,5 |
1.52 |
101 |
|
|
2 |
1,5 |
1,41 |
94 |
|
|
3 |
2,0 |
1,90 |
95 |
|
|
3 |
2,0 |
2,04 |
102 |
|
|
4 |
2,5 |
2,50 |
100 |
|
|
4 |
2,5 |
2,38 |
98 |
|
|
5 |
3,0 |
3,18 |
106 |
|
|
5 |
3,0 |
2,97 |
99 |
Сходимость методики оценивали по результатам повторного определения содержания верапамила в геле. Результаты и метрологические характеристики представлены в таблице 2.
Таблица 2
Результаты определения верапамила в геле. Оценка сходимости
|
Содержание верапамила в геле, г/100 г |
Метрологические характеристики |
|
0,90 |
Хср = 0,925 DХ = 0,057 SD = 0,055 RSD% = 5,9% Е% = 6,2%
|
|
1,01 |
|
|
0,94 |
|
|
0,85 |
|
|
0,9 |
|
|
0,95 |
Выводы. В результате проведённых исследований разработана методика идентификации и количественного определения верапамила в геле методом планарной хроматографии на пластинках марки ПТСХ-П-В-УФ. Полученные данные свидетельствуют, что методика специфична, имеет достаточно высокую чувствительность и эффективность. Методика количественного определения отвечает необходимым требованиям по показателям чувствительность, линейность, правильность и сходимость.
Рецензенты:
Коновалов Д.А., д.ф.н., профессор кафедры фармакогнозии Пятигорского медико-фармацевтического института - филиала ГБОУ ВПО «Волг ГМУ», г. Пятигорск;
Компанцева Е.В., д.ф.н., профессор кафедры фармацевтической химии и токсикологии Пятигорского медико-фармацевтического института - филиала ГБОУ ВПО «Волг ГМУ», г. Пятигорск.
Библиографическая ссылка
Мезенова Т.Д., Ушакова Л.С., Леонова В.Н., Жидкова Ю.Ю., Пеньевская Н.А. ОПРЕДЕЛЕНИЕ ВЕРАПАМИЛА В ГЕЛЕ МЕТОДОМ ПЛАНАРНОЙ ХРОМАТОГРАФИИ // Современные проблемы науки и образования. 2014. № 5. ;URL: https://science-education.ru/en/article/view?id=15232 (дата обращения: 04.06.2026).



