Scientific journal
Modern problems of science and education
ISSN 2070-7428
"Перечень" ВАК
ИФ РИНЦ = 0,936
THE DEPENDENCE OF THE PRESSURE OF AMMONIA OVER THE JOINT WATER SOLUTION OF AMMONIA AND AMMONIUM CHLORIDE FROM THE COMPOSITION OF THE SOLUTION
Введение
Совместный водный раствор аммиака и хлорида аммония эффективно экстрагирует соединения переходных металлов, образующих растворимые аммиачные комплексы (медь, цинк и др.), из отвалов рудников и отходов цветной металлургии [2, 4]. Переработка в качестве вторичного сырья техногенных отходов имеет значение для экономики и актуальна с точки зрения уменьшения загрязнения окружающей среды солями тяжёлых металлов. Для выделения соединений металлов из экстракта аммиак отгоняют, что разрушает аммиачные комплексы и приводит к осаждению оксидов и гидроксидов извлекаемых металлов.
Для определения условий извлечения соединений переходных металлов аммонийно-аммиачным раствором и минимизации потерь аммиака при его отгонке необходимо знание зависимости парциального давления аммиака (PNH3) над этим раствором от его состава. Значения давления аммиака над аммиачной водой, не содержащей солей, табулированы [6], однако в литературе нет алгоритма расчёта PNH3 по составу, позволяющего вычислить PNH3 при концентрации аммиака, не включённой в справочные таблицы.
Фрагментарные данные для аммонийно-аммиачных растворов [7] позволяют считать, что при близких к насыщению концентрациях NH4СI равновесная моляльность аммиака в растворе растёт в изобарно-изотермических условиях с ростом концентрации NH4СI. Это соответствует редко наблюдаемому в системе: «Вода, растворённый газ, соль» всаливанию газа». Известно [2, 3] PNH3 над аммонийно-аммиачными растворами в ограниченном интервале концентраций NH4СI и NH3, но отсутствует методика расчёта PNH3 над раствором по данным о его составе без измерения давления аммиака над раствором заданной концентрации.
Влияние концентрации соли на растворимость газов в водном растворе электролита в изобарно-изотермических условиях адекватно описывает уравнение Сеченова [1]:
lgC = lgC0 – k C2 (1)
В уравнении (1) С − растворимость газа; индекс 1 относится к водно-солевому раствору, индекс 0 – к воде; k − коэффициент Сеченова; C2 − концентрация соли, обычно уменьшающей растворимость газа. Концентрации компонентов целесообразно выражать через их моляльность [1]. Коэффициент Сеченова для раствора NH3 и NH4Cl в воде неизвестен; в тоже время его значения индивидуальны для каждой системы «Вода, растворённый газ, соль» и не могут быть определены априорно.
Цель работы
Изучение зависимости парциального давления аммиака над совместным водным раствором аммиака и хлорида аммония от концентрации его компонентов и разработка методики расчета численных значений PNH3 по составу и температуре раствора, применимого в интервале концентраций аммиака и хлорида аммония до 15% масс.
Методика исследования
Равновесное давление аммиака над совместными растворами в воде аммиака и хлорида аммония определяли динамическим методом, аналогично ранее проведённым исследованиям [2, 3] при концентрациях: аммиака до 10, NH4Cl до 3,5 моль/1000 г воды. Растворы для исследования готовили, растворяя в аммиачной воде, содержащей 5, 10, 15 % масс. аммиака, точно известные навески хлорида аммония. Отклонения содержания аммиака в аммиачной воде от указанных концентраций в отдельных пробах не превосходили ±0,3%. Хлорид аммония вносили навесками по 2, 5, 10 г на 100 мл раствора. Указанные массы навесок хлорида аммония выдерживали с отклонениями не более ±0,1 г. Для расчета C0 − равновесного содержания аммиака в аммиачной воде по величине PNH3 статистически обработаны данные [6, 8] по давлению аммиака над аммиачной водой.
Зависимость C0 от PNH3 аппроксимирована уравнениями:
С0-1 = А1 + B1 PNH3-1 (2)
lgB1 = А2 + B2 T-1 (3)
В уравнениях (2) и (3) С0 выражено в моль/1000г воды, PNH3 − в кПа, температура в К. При известных по данным опыта значениям температуры, PNH3, концентраций хлорида аммония и аммиака вычисляли последовательным решением уравнений (3), (2) и (1) коэффициент k в уравнении Сеченова.
Результаты исследования
В таблице 1 частично представлено сопоставление литературных данных [6, 8] по равновесным концентрациям аммиака (СNH3(Э)) и расчетным значениям СNH3(Р), найденными решением уравнений (2) и (3) для указанных в литературе величин РNH3 над аммиачной водой. Значение ∆ равно относительному отклонению величин СNH3(Р) от опытных данных.
Таблица 1. Экспериментальные и расчетные значения содержания аммиака в аммиачной воде
|
Темпе-ратура, К |
РNH3, кПа |
Растворимость NH3, моль/1000 г Н2О |
∆, % |
Темпе-ратура, К |
РNH3, кПа |
Растворимость NH3, моль/1000 г Н2О |
∆, % |
||
|
экспери- мент |
расчет |
экспери- мент |
расчет |
||||||
|
273 |
1,520 |
2,914 |
2,889 |
–0,84 |
313 |
3,213 |
0,938 |
0,956 |
+1,98 |
|
3,306 |
5,924 |
5,811 |
–1,91 |
8,106 |
2,349 |
2,332 |
–0,72 |
||
|
8,530 |
11,790 |
12,080 |
+2,47 |
17,730 |
4,673 |
4,780 |
+2,38 |
||
|
10,990 |
14,350 |
14,590 |
+1,66 |
36,400 |
8,790 |
8,761 |
–0,33 |
||
|
15,330 |
17,470 |
17,870 |
+2,33 |
53,660 |
11,790 |
11,590 |
–1,74 |
||
|
25,530 |
23,560 |
23,160 |
–1,70 |
77,060 |
15,490 |
15,020 |
–3,06 |
||
|
293 |
1,600 |
1,176 |
1,150 |
–2,19 |
333 |
18,250 |
2,360 |
2,404 |
+1,74 |
|
3,320 |
2,349 |
2,318 |
–1,33 |
28,780 |
3,600 |
3,668 |
+1,90 |
||
|
7,493 |
4,920 |
4,889 |
–0,63 |
40,050 |
4,962 |
4,933 |
–0,58 |
||
|
15,200 |
8,790 |
8,850 |
+0,68 |
50,080 |
6,082 |
5,990 |
–1,36 |
||
|
22,130 |
11,790 |
11,750 |
–0,34 |
77,730 |
8,790 |
8,616 |
–1,98 |
||
|
30,260 |
14,700 |
14,550 |
–1,02 |
111,20 |
11,740 |
11,318 |
–3,59 |
||
Таблица 2 содержит коэффициенты А1, А2 и B2, определённые по методу наименьших квадратов. Данные таблицы 1 доказывают адекватность описания зависимости равновесной концентрации аммиака в растворе от его парциального давления с помощью уравнений (2) и (3). Средняя ошибка расчёта СNH3(Р) по отношению к опытным значениям составляет 1,7%.
Таблица 2. Численные значения коэффициентов регрессии в уравнениях (2) и (3)
|
Наименование коэффициента регрессии |
А1 |
А2 |
B2 |
|
Численная величина коэффициента регрессии |
0,024 |
6,15432 |
−1764,8 |
Из приводимых в таблице 3 результатов, выполненных в настоящей работе измерений PNH3 над совместными растворами аммиака и хлорида аммония в воде, видно, что с ростом моляльности NH4Cl при близких по величине концентрациях аммиака PNH3 возрастает. Таким образом, в изученной системе в области умеренных концентраций наблюдается эффект высаливания. Отметим, что коэффициент Сеченова, вычисленный по опытным данным, закономерно уменьшается с ростом содержания в растворе хлорида аммония.
Таблица 3 . Давление аммиака и значения коэффициента Сеченова для изученных водных растворов аммиака и хлорида аммония
|
№ опыта |
Моляльность NH4Cl |
PNH3, кПа |
Коэффициент Сеченова |
|||
|
NH3 |
NH4Cl |
экспе-римент |
расчёт |
экспе-римент |
расчёт |
|
|
1 |
3,148 |
0,202 |
5,179 |
5,204 |
0,232 |
0,2415 |
|
2 |
3,098 |
0,403 |
5,452 |
5,545 |
0,184 |
0,2006 |
|
3 |
3,064 |
1,006 |
6,093 |
6,211 |
0,122 |
0,1295 |
|
4 |
3,005 |
2,011 |
6,020 |
5,642 |
0,0629 |
0,05920 |
|
5 |
3,101 |
3,003 |
4,921 |
4,899 |
0,0110 |
0,0104 |
|
6 |
6, 580 |
0,426 |
13,21 |
13,35 |
0,188 |
0,1968 |
|
7 |
6,539 |
1,091 |
15,79 |
12,55 |
0,130 |
0,1220 |
|
8 |
6,508 |
2,189 |
14,40 |
14,14 |
0,0525 |
0,0494 |
|
9 |
6,505 |
3,208 |
10,61 |
10,598 |
0,0020 |
0,0018 |
|
10 |
10,40 |
0,222 |
21,705 |
22,10 |
0,211 |
0,2365 |
|
11 |
10,38 |
0,433 |
24,98 |
24,47 |
0,210 |
0,1957 |
|
12 |
10,21 |
1,190 |
28,99 |
28,3 3 |
0,1192 |
0,1139 |
|
13 |
10,16 |
2,35 |
24,25 |
24,66 |
0,0425 |
0,0410 |
|
14 |
10,09 |
3,473 |
16,22 |
16,41 |
−0,010 |
−0,0089 |
Из рисунка 1, иллюстрирующего зависимость коэффициента Сеченова от mNH4Cl , видно асимптотическое приближение величины этого коэффициента к нулю с ростом концентрации NH4Cl.
Зависимость k от m NH4Cl отвечает уравнению:
lg k = 0,4 − 0,27 (mNH4Cl)0,333 (4)
Данные таблицы 3 показывают удовлетворительную сходимость величин коэффициентов Сеченова, вычисленных по данным опытов и рассчитанных по уравнению (4). Еще меньше относительная разница между опытными и расчетными значениями давления аммиака над аммонийно-аммиачным раствором. Величина PNH3 в этом случае вычислена по расчетным значениям коэффициента Сеченова, приведенным в таблице 3 последовательным решением уравнений (1), (3) и (2).
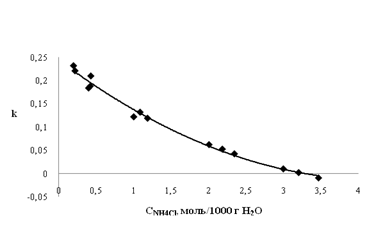
Рисунок 1. Зависимость коэффициента Сеченова от концентрации NH4Cl в растворе
Система уравнений (1) − (4) может быть решена как по отношению к равновесному содержанию аммиака в растворе по известной или заданной величине РNH3, так и по отношению к величине равновесного парциального давления аммиака над изученными растворами, если концентрации аммиака и NH4Cl моль/1000г воды известны. Среднее отклонение расчётных величин РNH3, вычисленных по уравнениям (1) − (4), от опытных данных равно ±1,7% при отсутствии расчётных ошибок, более чем вдвое превышающих среднюю величину.
Представленные уравнения обеспечивают точность расчёта парциального давления аммиака над совместными водными растворами аммиака и хлорида аммония достаточную для определения возможных потерь аммиака при его отгонке из раствора, использованного для извлечения цветных металлов из техногенных отходов.
Зависимость коэффициента Сеченова от моляльности NH4Cl связано с существенными отличиями системы: «Вода, хлорид аммония, аммиак» от других водно-солевых систем, в которых растворён газ. Во-первых, мольная доля аммиака в данной системе при изученных концентрациях достигает 0,145, в то время как в типичных системах, на основании изучения которых выведено уравнение Сеченова, мольная доля растворённого газа не превышает 10-4 – 10-3. В изучаемой системе структура воды заметно нарушена растворением аммиака, и влияние хлорида аммония на деструктуризацию воды не может не уменьшаться с ростом его концентрации. Во-вторых, известна способность аммиака к нестойкой связи с ионом аммония, проявляющаяся в уменьшении РNH3 над раствором нитрата аммония в жидком аммиаке по сравнению с давлением над жидким аммиаком [7]. Названные факторы ведут к уменьшению влияния NH4Cl на растворимость аммиака в воде по мере роста моляльности соли.
Анализ литературных данных по системе: «Вода, аммиак, хлорид аммония» [6] при давлении аммиака 101,325 кПа показывает, что моляльные концентрации аммиака и хлорида аммония в совместных аммонийно-аммиачных растворах существенно выше, чем в соответствующих бинарных системах. Так, моляльная концентрация NH4Cl в насыщенном водном растворе составляет при 293 К 11,07 моль/1000г воды, а в насыщенном аммонийно-аммиачном растворе достигает 20,05 моль/1000г воды, моляльная концентрация аммиака при той же температуре и РNH3 равном 101,325 кПа в аммиачной воде составляет 35 моль, а в насыщенных по NH4Cl, лежит в интервале 37−54,1 моль/1000г воды. Вычисленные нами по данным [6] коэффициенты Сеченова лежат в интервале минус 0,01 − 0,011. Таким образом, данные, полученные ранее для растворов, насыщенных по хлориду аммония, при РNH3, равном 101,325 кПа, подтверждают рост равновесной концентрации аммиака в расчёте на 1000 г воды в совместном растворе аммиака и хлорида аммония с ростом его моляльности по NH4Cl. Следует отметить, что расчёт по уравнению (4) даёт существенно большие по модулю значения коэффициента Сеченова. Можно предполагать, что расхождения по численной величине коэффициента Сеченова связаны с тем, что концентрации аммиака и NH4Cl в растворах, данные по которым приведены в литературе [7], лежат далеко за границей полной гидратации, в то время как нами исследованы растворы, представляющие практический интерес, в которых мольная доля воды существенно больше 50%.
Выводы
- Изучена зависимость парциального давления аммиака над совместным водным раствором аммиака и хлорида аммония при концентрациях неводных компонентов раствора до 15% масс.
- Установлено наличие при мольных концентрациях хлорида аммония до 3,3 моль/1000г воды эффекта высаливания аммиака хлоридом аммония, проявляющееся в увеличении парциального давления аммиака над совместным раствором аммиака и хлорида аммония по сравнению с изоконцентрационной по аммиаку аммиачной водой.
- Представлены расчётные уравнения, обеспечивающие расчёт парциального давления ммиака над не содержащей растворённых солей аммиачной водой и совместным раствором аммиака и хлорида аммония.
- Установлено уменьшение численной величины коэффициента Сеченова для совместного раствора аммиака и хлорида аммония с ростом моляльности NH4Cl.
Рецензенты:
Ульянов В.М., д.т.н., профессор кафедры «Машины и аппараты химических и пищевых производств» ДПИ НГТУ им. Р.Е. Алексеева, г. Дзержинск.
Когтев С.Е., д.т.н., профессор, директор по развитию производства ООО «Синтез–ПКЖ», г.Дзержинск.
Библиографическая ссылка
Гагарина Т.Б., Ксандров Н.В., Ожогина О.Р., Казанкова Т.Н., Перетрутов А.А. ИЗУЧЕНИЕ ЗАВИСИМОСТИ ДАВЛЕНИЯ АММИАКА НАД СОВМЕСТНЫМ ВОДНЫМ РАСТВОРОМ АММИАКА И ХЛОРИДА АММОНИЯ ОТ СОСТАВА РАСТВОРА // Современные проблемы науки и образования. 2014. № 3. ;URL: https://science-education.ru/en/article/view?id=13468 (дата обращения: 13.05.2026).



