Scientific journal
Modern problems of science and education
ISSN 2070-7428
"Перечень" ВАК
ИФ РИНЦ = 0,936
ANALYSIS OF THE QUALITY OF TRAINING OF STUDENTS OF CHEMISTRY AT THE TECHNICAL UNIVERSITY
Новации в сфере высшего образования, происходящие в настоящее время, стимулируют перестройку сознания студента как объекта процесса обучения, так и переориентацию форм обучения с пассивных – классически информационных, на активные, при реализации которых студент становится субъектом познавательного процесса [1,2,5]. Преподаватель перестает быть только носителем знаний, его функции претерпевают существенные изменения с источника знаний на консультирование и побудительную роль к самостоятельному поиску информации.
Создание оптимальной образовательной траектории в системе высшего образования предполагает сочетание нескольких важных составляющих:
-
наличие высокопрофессиональных кадров:
-
необходимый и достаточный начальный уровень школьной подготовки студентов;
-
мотивированность студентов;
-
независимая оценка знаний студентов на всех этапах обучения.
В Томском политехническом университете в последние несколько лет разрабатывается система независимого объективного контроля знаний студентов первого курса по общей и неорганической химии. Все студенты, поступившие на первый курс очной формы обучения, проходят процедуру обязательного входного тестирования, по результатам которого происходит ранжирование студентов на две группы. Первая группа – это студенты, набравшие половину или меньшее количество баллов от максимально возможного, которым в дальнейшем предлагается посещать дополнительные практические занятия, так называемые адаптированные практики. Студенты второй группы свободны в выборе траектории своего обучения, то есть могут ограничиться только обязательными видами занятий. Для проведения входного тестирования были разработаны задания, которые основывались на обязательном минимуме знаний школьного курса химии [3] и включали задания только базового уровня сложности. Данный выбор заданий был обусловлен тем, что целью входного тестирования было не только и не столько последующая дифференциация студентов, сколько определение исходного уровня знаний и сопоставление его с предыдущим годом набора студентов. В 2012 г. уровень знаний студентов, поступивших на первый курс, по химии был достаточно высок [4], что положительно сказалось на успешности их обучению предмету. В 2013 г. произошел «сбой» в процедуре проведения ЕГЭ, и, как оказалось, достаточное количество «случайных» абитуриентов прошло процедуру отбора и поступило на химические направления в ВУЗ. Доказательством этому могут служить цифры, полученные сравнением числа студентов, направленных на адаптированную траекторию обучения в 2013 и 2012 гг. В то время как в 2012 году по адаптированному плану обучения обязаны были заниматься меньше 40 % студентов первокурсников, то в 2013 г. таковых было 60 %.
Обучение студентов химических направлений в техническом университете начинается с изучения общей химии в течение одного семестра. Для того чтобы отследить динамику процесса, был разработан банк тестовых заданий [6,7] и программа, позволяющая моделировать билеты для любого вида контроля, проводить изменение порядка следования дистракторов, тем самым увеличивая вариативность тестовых материалов. Оценка знаний студентов проводилась на 9 и 18 неделях семестра с привлечением компьютерных технологий. К 9 неделе семестра студенты изучили следующие разделы общей химии, которые представлены в таблице 1.
Таблица 1.
Кодификатор элементов содержания первой рубежной контрольной работы
|
Разделы дисциплины |
Темы дисциплины |
Планируемый результат обучения |
|
1. Основные понятия и законы химии |
1.1.Основные классы неорганических соединений. |
Знать основные классы соединений (оксиды, гидроксиды, соли). Уметь характеризовать свойства соединений, записывать уравнения химических реакций. |
|
1.2.Атомно-молекулярное учение. |
Знать сущность основных законов химии (закон сохранение массы-энергии, закон эквивалентов, закон постоянства состава, закон удельных теплоемкостей). Иметь навыки решения расчетных задач. |
|
|
2. Периодическая система и строение атомов элементов
|
2.1.Общие сведения о составе и строении атомов |
Знать качественный состав атомов (электроны, протоны, нейтроны). Уметь определять положение элемента в ПС по наличию элементарных частиц в ядре его атома.
|
|
2.2.Основные представления современной теории строения атома - квантовой механики |
Знать основополагающие идеи квантовой механики: квантование энергии электрона в атоме, двойственная природа электрона, принцип неопределенности. Знать физический смысл 4 квантовых чисел. |
|
|
2.3.Закономерности формирования электронных структур атомов |
Знать принципы заполнения электронами атомных орбиталей, энергетических уровней и подуровней. Уметь записывать электронные и электронно-графические формулы атомов. Уметь характеризовать 4 квантовыми числами любой электрон в атоме. Иметь навыки прогнозирования свойств элемента по электронному строению его атома. |
|
|
2.4.Периодический закон и периодическая система элементов |
Уметь формулировать периодический закон и объяснять структуру периодической системы. Знать сущность основных характеристик атомов (радиус, энергия ионизации, сродство к электрону, электроотрицательность). Уметь объяснять характер их изменения по периодам и группам ПС. |
|
|
3. Химическая связь. Строение вещества в конденсированном состоянии |
3.1.Виды и характеристики химической связи |
Знать 5 видов химического взаимодействия (ковалентная связь, ионная, металлическая, водородная, силы Ван-дер-Ваальса). Уметь по виду химической связи прогнозировать свойства вещества. Знать основные характеристики химической связи (длина, энергия, валентный угол, полярность связи). Уметь предсказывать характер их изменения в ряду однотипных соединений. |
|
3.2.Ковалентная связь. Метод валентных связей (ВС). Гибридизация. Метод молекулярных орбиталей (МО). |
Уметь объяснять механизм образования ковалентной химической связи. Знать свойства ковалентной связи (насыщаемость, направленность). Знать основные положения метода ВС, теории гибридизации, метода ОЭПВО. Уметь строить диаграммы ВС и характеризовать свойства молекул с ковалентной связью. Уметь строить диаграммы МО и характеризовать свойства молекул с ковалентной связью. |
|
|
3.3.Ионная связь. Металлическая связь. |
Уметь объяснять причину образования ионной химической связи. Знать свойства соединений с ионной связью и закономерности их изменения. Уметь объяснять механизм образования металлической связи. Знать свойства соединений с металлической связью. |
|
|
3.4. Комплексные соединения (КС). Химическая связь в комплексах. |
Знать составные части, классификацию и номенклатуру КС. Уметь записывать уравнения диссоциации КС, выражения нестойкости. Уметь описывать образование химической связи и свойства КС методами ВС и ТКП. |
|
|
3.5.Водородная связь. Силы Ван-дер-Ваальса. |
Уметь объяснять механизм образования водородной связи и её влияние на свойства соединений. Знать 3 типа межмолекулярных сил и их влияние на образование веществ в конденсированном состоянии. |
|
Кроме перечисленных тем, в первое рубежное тестирование были включены задания, проверяющие умения и навыки студентов решать задачи на различные способы выражения концентрации растворов. Таким образом, билет первого тестирования содержал 15 заданий. Студенты в течение полутора часов отвечали на вопросы, решали задачи, занося ответы в компьютер, который по окончании тестирования сразу выдавал студенту итоговый результат. Преподавателю предоставлялась распечатка с конкретными данными по каждому студенту и каждому заданию. Одним из условий ликвидности тестирования, о чем студенты были предупреждены неоднократно, являлось наличие пояснения ответов к каждому заданию и решения задач в черновиках, тем самым мы пытаемся, если не устранить, то хотя бы нивелировать эффект от внешней помощи студентам с привлечением современных средств коммуникации. По окончании тестирования черновик каждого студента был проверен на наличие пояснений и положительные результаты тех заданий, к которым пояснения отсутствовали, были аннулированы. Результаты тестирования представлены на рис. 1.
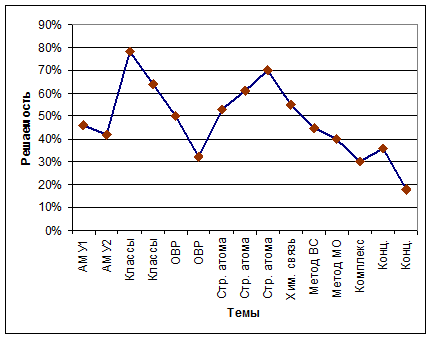
Рисунок 1. Решаемость заданий первого рубежного тестирования
Интересна реакция студентов на процедуру просмотра работ. Ожидалось, что студенты поведут себя агрессивно, будут отстаивать полученные баллы, но все прошло на удивление мирно, быстро достигнуто взаимопонимание и сделаны определенные выводы с двух сторон. Студенты поняли, что тестирование – это не просто нажатие на кнопки клавиатуры, а также, что бесполезно прибегать к внешним силам (использование микронаушников было выявлено в нескольких случаях), а преподаватель – что выбранный путь является верным, что в дальнейшем было подтверждено последующими тестированиями. При обсуждении ситуации мы объясняли студентам, что компьютер лишь облегчает преподавателю процедуру проверки решения заданий, ускоряя её, что логика решения должна быть видна и обозначена, только в этом случае появляется возможность выявления проблем в знаниях, умениях и навыков студентов. Таким образом, мы полагаем, что тестирование несет в себе и образовательную функцию, если умело распорядиться имеющимися ресурсами.
По результатам первого тестирования были сделаны следующие выводы:
1) низкий уровень школьной подготовки по химии студентов 2013 г. набора обусловил снижения качества полученный знаний, полученных в первой половине семестра, по сравнению со студентами 2012 г. набора (рис. 2);
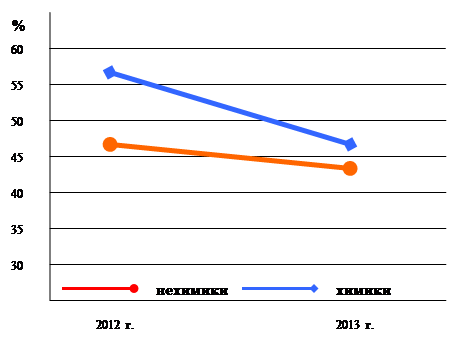
Рисунок 2. Динамика результатов первого рубежного тестирования
2) особую сложность для студентов представляли задания, связанные с решением задач на способы выражения концентрации растворов, а также с уравниванием окислительно-восстановительных реакций методом полуреакций (рис. 1).
Нужно отметить, что разрабатывая задания по теме «Окислительно-восстановительные реакции», мы столкнулись с проблемой, связанной с формой их представления. Для того чтобы проверить умение студентов применять метод полуреакций, мы удалили из схем реакций формулы некоторых соединений:
H2O2 + KMnO4 + ... = O2 + MnSO4 + K2SO4 + ...,
тем самым, предотвратив возможность механистического подбора коэффициентов. В итоге 70 % студентов не справилось с данными заданиями. Оценив ситуацию, мы провели корректирующие мероприятия, и данные задания вновь были включены в структуру билетов второго рубежного тестирования;
3) адаптивная траектория обучения является весьма эффективной и позволяет сохранить контингент студентов, способных к обучению в высшем учебном заведении, но не получивших базовых знаний по предмету в средней школе. Особенно эта проблема остро связана с химическим образованием, которое в школе сведено к минимуму. Адаптивный учебный материал предусматривает дополнительные не обязательные занятия для студентов с низким уровнем знаний, причем формат проведения этих занятий выбирает преподаватель. Как правило, они проводятся в менее формализованном виде, поощряется диалог студент – преподаватель, преподаватель и студенты взаимодействуя друг с другом в ходе занятия, являются активными участниками учебного процесса. Эффективность такого рода занятий высока, что отражается на результатах процесса обучения (рис. 3).
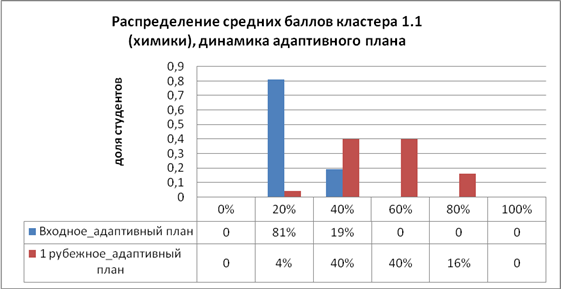
Рисунок 3. Динамика обучения студентов по адаптивному учебному плану
Из графика видно, что большая часть студентов (81 %), направленных по итогам входного тестирования на адаптивную траекторию обучения, не справилась с заданиями входного теста, несмотря на его низкий уровень сложности. В то же время, спустя два месяца обучения в ВУЗе, эти же студенты демонстрируют неплохую динамику обучения: более половины из них успешно справляюся с заданиями первой рубежной контрольной работы. Проведение любого контролирующего мероприятия в тестовой форме может быть эффективным только в том случае, если по его итогам прведено со устное собеседование, во время которого выявляются реальные знания и умения студента. Ограниченность тестового задания состоит в том, что правильность ответа и решения не всегда совпадают: с точки зрения математики ответ может быть верен, а с химической – абсурден. Студент может знать, что таллий окисляется на воздухе, но не в силах описать, протекающие при этом процессы, или доказать амфотерность гидроксида галлия. Таким образом, применение тестовых технологий может освободить преподавателя от некоторой рутинной работы по проверке решения задач, но не должно полностью упразднять контакт студент – преподаватель при проведении контроля, особенно на этапе обучения.
Рецензенты:
Бакибаев А.А., д.х.н., заведующий кафедрой, физической и аналитической химии профессор, Институт природных ресурсов, Федеральное государственное бюджетное образовательное учреждение высшего профессионального образования «Национальный исследовательский Томский политехнический университет», г. Томск.
Ильин А.П., д.ф.-м.н., профессор кафедры общей и неорганической химии, Институт физики высоких технологий, Федеральное государственное бюджетное образовательное учреждение высшего профессионального образования «Национальный исследовательский Томский политехнический университет», г.Томск.
Библиографическая ссылка
Князева Е.М. АНАЛИЗ КАЧЕСТВА ОБУЧЕНИЯ СТУДЕНТОВ ХИМИИ В ТЕХНИЧЕСКОМ УНИВЕРСИТЕТЕ // Современные проблемы науки и образования. 2014. № 3. ;URL: https://science-education.ru/en/article/view?id=13239 (дата обращения: 16.05.2026).



