Scientific journal
Modern problems of science and education
ISSN 2070-7428
"Перечень" ВАК
ИФ РИНЦ = 0,936
DERMATOLOGICAL MANIFESTATIONS OF DIABETES MELLITUS
С патологическими изменениями кожи сталкиваются врачи самых разных специальностей, в том числе и эндокринологи. Поражение кожи может быть как случайной находкой, так и основной жалобой больного. Безобидные на первый взгляд изменения кожи могут оказаться единственным признаком проявления тяжелой болезни. Кожа – самый доступный для исследования орган и одновременно источник важнейшей информации. Поражение кожи может прояснить диагноз при многих внутренних болезнях, в том числе и при сахарном диабете (СД).
Кожные изменения при СД встречаются довольно часто. Тяжелые метаболические нарушения, лежащие в основе патогенеза СД, приводят к изменениям почти во всех органах и тканях, в том числе и в коже [30].
Некоторые диабет-ассоциированные кожные симптомы являются прямым результатом метаболических изменений, таких как гипергликемия и гиперлипидемия [4, 7]. Прогрессирующее повреждение сосудистой, нервной или иммунной систем также в значительной степени способствует развитию кожных проявлений. Механизмы других диабет-ассоциированных дерматологических поражений остаются неизвестными [7, 20].
Способствовать кожным изменениям также может гиперинсулинемия, как это наблюдается на ранних стадиях инсулин-резистентного диабета 2 типа.
Также значительно усугубляют течение кожных осложнений диабета макро- и микроангиопатии. У пациентов с диабетом отмечается повышенная «негерметичность» или проницаемость сосудистой стенки, снижение реактивности сосудов на симпатическую иннервацию и гипоксемический стресс [4, 43]. В сочетании с артериосклерозом крупных сосудов, эти микроваскулярные нарушения способствуют образованию диабетических язв. Кроме того, при диабете развивается потеря кожной иннервационной чувствительности, что предрасполагает к инфекциям и повреждениям [16]. Как правило, диабетические поражения кожи имеют длительное и упорное течение с частыми обострениями и трудно поддаются лечению.
Существует несколько классификаций поражений кожи при СД, в их основе лежит клиническая характеристика и некоторые аспекты патогенеза кожных изменений. Согласно классификации Хлебниковой А.Н., Марычевой Н.В. (2011) [14] условно патологию кожи при СД подразделяют на пять основных групп:
1) дерматозы, связанные с СД;
2) патология кожи, связанная с СД и инсулинорезистентностью;
3) патология кожи, ассоциированная с ангиопатией;
4) идиопатические высыпания;
5) бактериальные и грибковые инфекции.
В классификации, описанной Andrea A. Kalus, Andy J. Chien, John E. Olerud (2012) [4] выделяют следующие группы диабет-ассоциированных кожных поражений:
1) кожные проявления СД, ассоциированные с метаболическими, васкулярными, неврологическими или иммунными нарушениями (диабетическая склередема, черный акантоз, диабетическое утолщение кожи, ограничение подвижности суставов и склеродермоподобный синдром, эруптивные ксантомы, кожные инфекции (бактериальные, грибковые), диабетические язвы);
2) заболевания, связанные с СД, с неясным патогенезом (липоидный некробиоз, кольцевидная гранулема, диабетический пузырь, диабетическая дермопатия).
Данные классификации практически не отличаются и лишь дополняют друг друга.
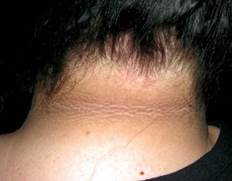
К дерматозам, связанным с СД относят диабетическую склередему. Склередема чаще встречается при длительно текущем СД в сочетании с ожирением и проявляется диффузными симметричными индуративными изменениями кожи преимущественно в области шеи и верхней трети спины по типу апельсиновой корки. По данным разных авторов, частота ее возникновения у больных СД составляет 2,5-14% [28, 25, 50].
Было предположено, что патогенез диабетической склередемы заключается в нерегулируемой продукции молекул экстрацеллюлярного матрикса фибробластами, что ведет к утолщению пучков коллагена и повышенному отложению гликозаминогликанов (ГАГ) [53]. Пациенты с диабетической склередемой могут испытывать снижение болевой и световой чувствительности в области пораженных участков кожи, а также жаловаться на затруднения движений верхних конечностей и шеи. В крайних случаях заболевание может приводить к полной потере подвижности суставов, однако, наличие склередемы не связано с ретинопатией, нефропатией, нейропатией или поражением крупных сосудов [4, 25].
ФОТО 1. Диабетическая склередема

Связь с инсулинорезистентностью и ожирением прослеживается при черном акантозе (acantosis nigricans), который проявляется участками гиперпигментации кожи с папилломатозными разрастаниями в области шеи и крупных складок [34]. Центральную роль в развитии акантоза играет инсулин. У женщин, страдающих акантозом, можно обнаружить утрату функциональных мутаций рецептора инсулина или рецептора антиинсулиновых антител (синдром типа А и типа В) [18, 31]. Считается, что избыточная стимуляция фактора роста в коже вызывает абберантную пролиферацию кератиноцитов и фибробластов, в результате чего развиваются клинические проявления черного акантоза [52]. При состояниях инсулинорезистентности и гиперинсулинемии, акантоз может развиваться вследствие избыточного связывания инсулина к рецепторам ИФР – 1 на кератиноцитах и фибробластах [27]. Данные в пользу роли различных факторов роста в патогенезе черного акантоза продолжают накапливаться.
ФОТО 2. Черный акантоз
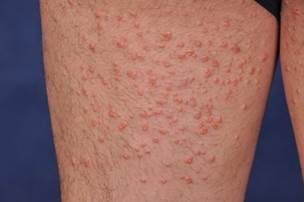
Недиагностированный СД и гипертриглицеридемия могут провоцировать появление на коже эруптивных ксантом [46, 8]. Они представляют собой красновато-желтые папулы размером 1-4 мм., расположенные на ягодицах и разгибательных поверхностях конечностей. Патологические элементы появляются в виде зерен и со временем могут сливаться с образованием бляшек. Изначально в кожных элементах преобладают триглицериды, но так как они мобилизуются легче, чем холестерол, с их распадом в коже накапливается все больше холестерола [47].
Инсулин является важным регулятором активности ЛПНП. Степень ферментной недостаточности и последующего очищения сывороточных триглицеридов пропорциональны показателям дефицита инсулина и гипергликемии [22]. Клиренс липопротеинов плазмы зависит от адекватного уровня инсулина [17]. При неконтролируемом диабете такая неспособность метаболизировать и освобождать насыщенные триглицеридами хиломикроны и липопротеины очень низкой плотности может приводить к повышению уровня триглицеридов плазмы до нескольких тысяч. Неконтролируемый диабет является распространенной причиной массивной гипертриглицеридемии [4, 26, 29].
ФОТО 3 эруптивные ксантомы
Больные СД склонны к развитию кожных инфекционных заболеваний, особенно при неудовлетворительном контроле гликемии. На поверхности кожи больных СД выявляют в 2,5 раза больше микроорганизмов, чем у здоровых лиц, а бактерицидная активность кожи у больных СД ниже в среднем на 20% [9]. Это снижение прямо коррелирует с тяжестью течения СД. Инфекционно-воспалительные заболевания прежде всего развиваются на коже нижних конечностей в связи с ангио- и нейропатиями. Причиной обычно являются полимикробные инфекции: золотистый стафилококк, стрептококки групп А и В, грамотрицательные аэробные бактерии и множество анаэробов. Пиодермии представлены в основном фолликулитами, эктимами, рожей и могут осложняться экзематизацией. Кроме того, возможно развитие фурункулеза, карбункулов, паронихий, инфекций мягких тканей [21].
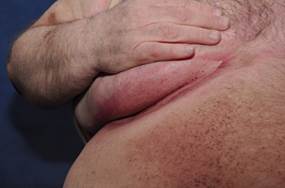
На фоне СД наблюдается повышенная частота грибковых инфекций, которые в структуре заболеваний у больных этой категории, по данным разных авторов, составляют 32,5 – 45% [14, 9]. В условиях гиперкалиемии грибы активно используют сахар для своих метаболических процессов и усиленно размножаются, вызывая болезнь. При СД нарушение микроциркуляции в сосудах нижних конечностей наблюдается в 20 раз чаще, чем у лиц без эндокринной патологии, что способствует развитию грибкового поражения стоп и онихомикоза [1]. Возбудителями грибковых поражений являются дерматофиты и Candida albicans. Причем в нормальной популяции грибковые поражения кожи, обусловленные C. albicans, не превышают 20%, тогда как у соматически отягощенных больных этот показатель повышается до 80 - 90% [12]. Следует отметить, что 80% регистрируемого кандидоза кожи приходится на больных СД [5]. Наиболее распространены интертриго (с поражением подмышечной, паховой областей, межпальцевых промежутков), вульвовагинит, баланит, паронихия, глоссит и ангулярный хейлит. Помимо дрожжевых вагинальных инфекций с клиническими проявлениями, у пациентов с диабетом также повышена частота бессимптомного носительства [36].
ФОТО 4 Кандидоз крупных складок
К заболеваниям, связанным с СД и имеющим неясный патогенез, относят липоидный некробиоз, кольцевидную гранулему, диабетический пузырь и диабетическую дермопатию.
Липоидный некробиоз (болезнь Оппенгейма – Урбаха) – редкое гранулематозное хроническое заболевание сосудисто-обменного характера, представляет собой локализованный липоидоз с отложением липидов в тех участках дермы, где имеется дегенерация или некробиоз коллагена [15]. Первые симптомы дерматоза обычно возникают в возрастной группе от 20 до 60 лет. В детском возрасте болезнь Оппенгейма-Урбаха встречается редко [13]. Частота возникновения липоидного некробиоза среди пациентов с СД составляет 0,1-3% [38, 6].
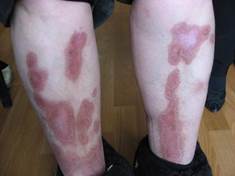
Клиническая картина болезни Оппенгейма-Урбаха весьма многообразна. В процесс могут вовлекаться различные участки кожного покрова, но в первую очередь кожа передних поверхностей голеней. Это можно объяснить, вероятно, тем, что при диабете патологические изменения первоначально происходят в мелких сосудах именно нижних конечностей [10]. Обычно липоидный некробиоз проявляется в виде одной или нескольких четко отграниченных желтовато-коричневых бляшек. Элементы имеют фиолетовые неровные края, которые могут возвышаться над поверхностью кожи или уплотняться. Со временем элементы выравниваются и центральная желтая или оранжевая область становится атрофичной, часто можно видеть телеангиоэктазии, которые придают областям поражения блеск «глазурованного фарфора». В области бляшек встречается потеря чувствительности [44, 2, 42].
ФОТО 5 Липоидный некробиоз
Генерализованная кольцевидная гранулема у 20% больных – первый признак ранее не диагностированного СД 2 типа. Связь кольцевидной гранулемы с СД остается предметом дискуссий, так как она может ассоциироваться и с другими заболеваниями [55]. Наблюдались локализованные, генерализованные, а также подкожные узловатые и перфорирующие формы кольцевидной гранулемы, ассоциированной с СД [3, 37, 24].
Типичный анамнез кольцевидной гранулемы предполагает одну или несколько папул, растущих по периферии с одновременным разрешением в центре. Очаги могут сохранять естественный цвет кожи или же быть эритематозными или фиолетовыми. Обычные размеры очагов от 1 до 5 см в диаметре [41]. Кольцевидная гранулема, как правило, протекает бессимптомно; возможен слабый кожный зуд, болезненные очаги наблюдаются редко [33].
ФОТО 6 Кольцевидная гранулема
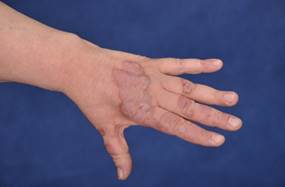
Диабетический буллез – субэпидермальный буллезный дерматоз, встречающийся у больных диабетом [39].
Впервые пузыри в качестве одного из вариантов поражений кожи при диабете наблюдал D. Kramer в 1930 г. [35]. A. Cantwell и W. Martz описали это состояние как диабетический буллез [23,11].
Причина появления пузырей у больных диабетом не ясна. Существуют теории о роли микроангиопатии и местных нарушений метаболизма. Диабетический буллез встречается преимущественно у лиц, длительно страдающих диабетом, несколько чаще – у женщин. Возраст начала заболевания колеблется от 17 до 79 лет.
На неизмененной коже появляются пузыри размером от нескольких миллиметров до нескольких сантиметров (обычно на коже нижних конечностей) [19]. Выделяют два вида поражения: интраэпидермально расположенные пузыри, которые исчезают без образования рубца, и субэпидермальные пузыри, после которых остаются атрофированные рубчики. Высыпания локализуются преимущественно на стопах и голенях, но могут встречаться на кистях и предплечьях. Пузыри самопроизвольно разрешаются через 2-5 недель, возможны рецидивы [45].
ФОТО 7 Диабетический пузырь
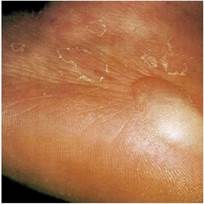
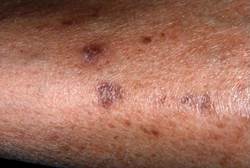
Атрофические кожные изменения нижних конечностей или «пятнистая голень», впервые были описаны и предложены в качестве маркера диабета в 1964 г. [54]. Вскоре после этого Binkley ввел термин диабетическая «дермопатия» с целью соотнесения данных патологических изменений с таковыми при ретинопатии, нефропатии и нейропатии [51]. Диабетическая дермопатия встречается чаще у пациентов с длительным течением диабета и более распространена среди мужчин [29, 40]. Клинически она представляет собой небольшие (менее 1 см) атрофические пятна от розового до коричневого цвета и напоминающие рубцовую ткань, располагающиеся на претибиальных участках. Эти элементы имеют бессимптомное течение и исчезают через 1-2 года, оставляя после себя небольшую атрофию или гипопигментацию [54]. Появление новых элементов позволяет предположить, что пигментация и атрофия являются персистирующими состояниями.
ФОТО 8 Диабетическая дермопатия
Обменно-эндокринные нарушения нередко являются пусковым механизмом развития некоторых дерматозов. Отмечается определенная взаимосвязь течения этих заболеваний с наличием эндокринопатии. Выраженный СД выявлен у 19% пациентов с красным плоским лишаем, у части из них имело место значительное изменение глюкозотолерантного теста [48]. Часто поражение слизистой оболочки полости рта при красном плоском лишае сочетается с СД и артериальной гипертензией (синдром Потекаева-Гриншпана), причем высыпания на слизистой оболочке, как правило, носят эрозивно-язвенный характер. В ходе крупномасштабного исследования для определения связи между псориазом и общим состоянием здоровья было установлено, что женщины, страдающие псориазом, на 63% больше предрасположены к развитию СД, по сравнению с пациентками, не имеющими данного дерматоза [49]. На фоне СД псориаз протекает тяжелее, наблюдаются такие формы как экссудативный псориаз, псориатический полиартрит, псориаз крупный складок [32].
Таким образом, изменения кожи вполне могут быть связаны с системными патологическими процессами, характерными для СД. В основе клинической и патоморфологической картины дерматозов и дермопатий, предшествующих или развивающихся на фоне СД, лежат метаболические, сосудистые, неврологические и иммунные нарушения.
Рецензенты:
Валеева Ф.В., д.м.н., профессор, зав. курсом, эндокринологии, профессор кафедры госпитальной терапии с курсом эндокринологии ГБОУ ВПО «Казанский государственный медицинский университет Министерства Здравоохранения Российской Федерации», г.Казань.
Сергеева И.Г., д.м.н., профессор кафедры фундаментальной медицины ФГБОУ ВПО Новосибирского национального исследовательского государственного университета, г.Новосибирск.
Библиографическая ссылка
Штода Ю.М., Слесаренко Н.А., Родионова Т.И., Утц С.Р., Карпова Е.Н. ДЕРМАТОЛОГИЧЕСКИЕ ПРОЯВЛЕНИЯ САХАРНОГО ДИАБЕТА // Современные проблемы науки и образования. 2014. № 2. ;URL: https://science-education.ru/en/article/view?id=12839 (дата обращения: 13.05.2026).



