Scientific journal
Modern problems of science and education
ISSN 2070-7428
"Перечень" ВАК
ИФ РИНЦ = 0,936
CHOISE OF COMPOSITION FOR A WOUND HEALING OINTMENT WITH PHYTOECDYSTEROIDS
Введение
В последнее время возрос интерес к фитоэкдистероидам – растительным аналогам гормонов линьки насекомых, в связи с их низкой токсичностью и высокой активностью [4]. Институтом биологии Коми Научного центра Уральского отделения Российской Академии наук (ИБ КНЦ УрО РАН) получен патент на сырье для получения биологически активных добавок, которое представляет собой суммарный очищенный препарат фитоэкдистероидов (СОПФ), главным образом 20-гидроксиэкдизон, выделенный из растения Serratula coronata, обладающий ранозаживляющими свойствами [1, 2, 4, 5]. Препараты в виде мягких лекарственных форм (МЛФ) имеют меньше побочных эффектов, в т. ч. системного характера, благодаря этому преимуществу их чаще выбирают для лекарственной терапии ряда заболеваний [3]. Актуальной задачей становится разработка МЛФ с оптимальными биофармацевтическими показателями.
Целью данной работы является выбор состава мягкой лекарственной формы с суммарным очищенным препаратом фитоэкдистероидов.
Экспериментальная часть
В работе использовали СОПФ, полученный от ИБ КНЦ УрО РАН. В качестве вспомогательных веществ изучены натрия карбоксиметилцеллюлоза, глицерин, вазелин, ланолин безводный, вазелиновое масло, моноглицериды дистиллированные, аэросил, вода очищенная.
Компоненты основ сплавляли на водяной бане с учетом их температур плавления. СОПФ при получении МЛФ вводили, растворяя в небольшом объеме этилового спирта. Первичная упаковка перед заполнением подвергалась химической дезинфекции в 6% перекиси водорода. При получении мазевых композиций соблюдались требования асептики.
Составы МЛФ с СОПФ оценивались по следующим технологическим параметрам: внешний вид, коллоидная и термическая устойчивость, значение рН, высвобождение из основы. Определение коллоидной, термической устойчивостей и водородного показателя проводили по методикам, описанным в ГОСТах 29188.2–91и 29188.3–91, с использованием центрифуги ЦЛН-2 (Россия) и иономера ЭВ-74 (Россия).
Биофармацевтические показатели составов определяли методом диффузии через полупроницаемую мембрану (равновесного диализа по Крувчинскому). Точную навеску композиции 0,5 г с помощью шпателя и трафарета наносили ровным слоем на целлофановую пленку, которую затем укрепляли на конце диализной трубки. Диализную трубку с составом вносили в стеклянный сосуд с диализной средой (водой очищенной) в количестве 25 мл и погружали на глубину не более 2 мм. Отбор проб диализата из каждой камеры производили после предварительного перемешивания через 30, 60, 90 минут от начала диализата с обязательным восполнением объема диализной среды. При обзоре литературы выяснилось, что фитоэкдистероиды поглощают в УФ-спектре. Длина волны для измерения оптической плотности испытуемых растворов диализатов была выбрана на основании данных спектрального анализа, согласно которому максимум поглощения приходится на 250 нм. Измерена оптическая плотность 3 серий разведений с концентрацией СОПФ от 5 мкг/мл до 25 мкг/мл. В каждой серии концентрацию действующих веществ определяли при аналитической длине волны.
Для изучения влияния природы мазевой композиции на биофармацевтические и технологические параметры нами проанализировано 4 состава (таб. 1). Экспериментально установлено, что составы однородны по консистенции, являются морозо- и термостойкими, не расслаиваются при хранении, хорошо намазываются на кожные покровы.
Таблица 1.
Составы мазевых композиций с фракцией фитоэкдистероидов
|
Компоненты мазевой композиции, г. |
Номер и тип мазевой композиции |
|||
|
1(Дифильный крем) |
2(Дифильный крем) |
3(Липофильная мазь) |
4(Гидрофильный гель) |
|
|
СОПФ |
0,01 |
0,01 |
0,01 |
0,01 |
|
Вазелин |
- |
11,0 |
40,0 |
- |
|
Аэросил |
1,5 |
1,5 |
- |
- |
|
Моноглицериды дистиллированные (МГД) |
2,0 |
2,0 |
- |
- |
|
Вазелиновое масло |
21,5 |
10,5 |
- |
- |
|
Ланолин безводный |
- |
- |
10,0 |
- |
|
Na-КМЦ |
- |
- |
- |
3,0 |
|
Глицерол |
- |
- |
- |
3,0 |
|
Вода очищенная |
До 50,0 |
До 50,0 |
До 50,0 |
До 50,0 |
Значения водородного показателя мазевых композиций и его метрологические характеристики представлены в таб. 2. Наиболее близкое значение к рН кожи (5,5) отмечается у состава №2. Состав №4 имеет слабощелочную реакцию. Составы №1 и №3 имеют рН близкий к 6. Водородный показатель для дерматологических мазей должен быть в пределах от 5,5 до 6,5. Из таблицы видно, три состава из четырех укладываются в указанные пределы, для этих составов не требуется введения вспомогательных веществ, регулирующих рН.
Таблица 2.
Значение водородного показателя мазевых композиций и его метрологические характеристики
|
№ состава |
f |
рН (Хср) |
S2 |
S |
Sxср |
a, % |
t (a, f) |
ΔХ |
εср, % |
|
1 |
3 |
6,22 |
0,024 |
0,16 |
0,09 |
95 |
3,18 |
0,29 |
4,90 |
|
2 |
3 |
5,85 |
0,018 |
0,13 |
0,08 |
95 |
3,18 |
0,25 |
4,21 |
|
3 |
3 |
6,14 |
0,003 |
0,05 |
0,03 |
95 |
3,18 |
0,10 |
1,55 |
|
4 |
3 |
7,19 |
0,016 |
0,13 |
0,07 |
95 |
3,18 |
0,23 |
3,26 |
Примечание. f – количество степеней свободы; Хср – выборочное среднее; S2 – исправленная выборочная дисперсия; S – исправленное выборочное среднее квадратическое отклонение (стандартное отклонение); Sxср – исправленное среднее квадратическое отклонение средней выборочной (стандартное отклонение); a, % – доверительная вероятность; t (a, f) – коэффициент Стьюдента; ΔХ – полуширина доверительного интервала; εср – относительная погрешность.
Для определения кинетики высвобождения СОПФ нами первоначально выявлена аналитическая длина волны, затем установлена линейность зависимости оптической плотности СОПФ от концентрации в диапазоне от 5 мкг/мл до 25 мкг/мл (рис. 1). Как следует из представленного рисунка, все экспериментальные точки лежат на одной прямой. Поскольку значение коэффициента корреляции составляет 0,998, то это позволяет утверждать о наличии линейной зависимости оптической плотности от концентрации СОПФ в растворе в диапазоне концентраций 5-25 мкг/мл.
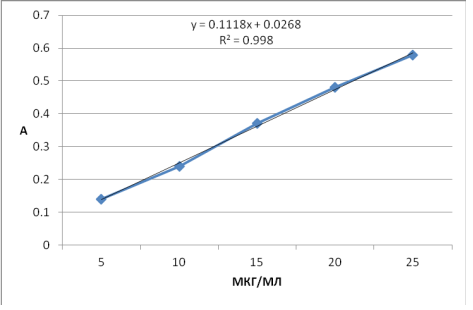
Рис. 1. Калибровочный график фитоэкдистероидов.
Кинетика высвобождения СОПФ представлена на рис. 2. В первые 30 мин. диализа наибольший выход СОПФ отмечается в составе № 1 – 50% от внесенного количества, наименьший – в составе №2 (25%). Наиболее полный выход СОПФ к концу диализа отмечается в составе №2 – 76%. В составе №1 нами была часть вазелинового масла заменена с целью улучшения реологических свойств, как следствие, получился состав №2. Замена части вазелинового масла на вазелин привело к увеличению степени выхода СОПФ из основы.
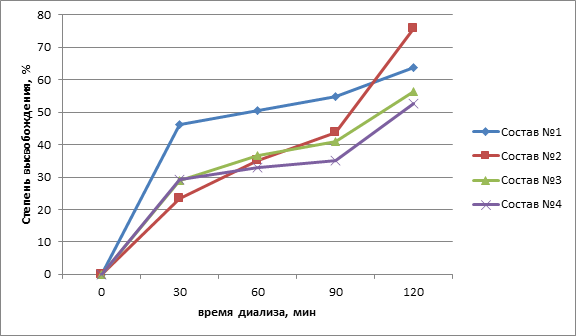
Рис. 2. Зависимость концентрации фитоэкдистероидов в диализате от времени диализа
Выводы
На основании проделанной работы можно сделать заключение, что наиболее подходящим типом основы для СОПФ по основным технологическим параметрам и динамики высвобождения является форма крема, представляющая собой эмульсию II типа (в/м), следующего состава: СОПФ 0,01; вазелин 11,0; вазелиновое масло 10,5; моноглицериды дистиллированные 2,0; аэросил 1,5; воды очищенной до 50,0.
Рецензенты:
Алексеева И.В., д.фарм.н., профессор кафедры фармацевтической технологии, проректор по учебно-воспитательной работе ГБОУ ВПО «Пермская государственная фармацевтическая академия» Министерства здравоохранения Российской Федерации, г. Пермь.
Егорова С.Н., д.фарм.н., профессор, заведующая кафедрой фармации факультета повышения квалификации и профессиональной переподготовки специалистов ГБОУ ВПО «Казанский государственный медицинский университет» Министерства здравоохранения Российской Федерации, г. Казань.
Библиографическая ссылка
Молохова Е.И., Липин Д.Е., Володин В.В. ВЫБОР КОМПОЗИЦИИ ДЛЯ РАНОЗАЖИВЛЯЮЩЕЙ МАЗИ НА ОСНОВЕ ФИТОЭКДИСТЕРОИДОВ // Современные проблемы науки и образования. 2014. № 1. ;URL: https://science-education.ru/en/article/view?id=11986 (дата обращения: 12.05.2026).



