Scientific journal
Modern problems of science and education
ISSN 2070-7428
"Перечень" ВАК
ИФ РИНЦ = 0,936
KINETIC APPROACHES TO A PROBLEM OF ANTIOXIDANT TEST. PART 4. ANTIOXIDANT ACTIVITY OF PYROCATECHINE AND SOME PHARMACEUTICALS
В трех предыдущих сообщениях [1, 2, 3] приведены результаты разработки кинетических моделей тестирования антиоксидантов в безводных и водно-липидных субстратах и результаты тестирования с помощью последней ряда лекарственных препаратов фенольной и тиольной природы. При этом было показано, что ожидания в соответствии с теорией торможения цепных процессов окисления производных углеводородов не всегда оправдываются для водно-липидных систем. Согласно этой теории амины жирного ряда и спирты не проявляют антиоксидантных свойств, а ароматические амины являются слабыми ингибиторами [4, 5, 6]. В то же время, известно торможение микросомального и митохондриального окисления с помощью аминов [7, 8].
В настоящем сообщении приведены результаты тестирования антиоксидантных свойств широко известных лекарственных препаратов: адреналина, метилдофы и их полупродукта - пирокатехина.
Пирокатехин ![]() является двухатомным фенолом и относится к сильным ингибиторам процессов окисления углеводородов и их производных. Адреналин
является двухатомным фенолом и относится к сильным ингибиторам процессов окисления углеводородов и их производных. Адреналин 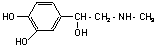 (1-(3´,4´-дигидроксифенил)-2-(N-ме-тил)-аминоэтанол) содержит в своем составе фрагмент пирокатехина, а также спиртовый гидроксил и группу вторичного амина и используется в медицине как адреномиметическое средство. Метилдофа
(1-(3´,4´-дигидроксифенил)-2-(N-ме-тил)-аминоэтанол) содержит в своем составе фрагмент пирокатехина, а также спиртовый гидроксил и группу вторичного амина и используется в медицине как адреномиметическое средство. Метилдофа 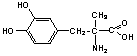 (2-амино-2-метил-3-(3´,4´-дигидрокси)фенилпропановая кислота) также является производным пирокатехина и содержит первичную аминную группу и карбонил. Применяется в медицине как гипотензивное средство.
(2-амино-2-метил-3-(3´,4´-дигидрокси)фенилпропановая кислота) также является производным пирокатехина и содержит первичную аминную группу и карбонил. Применяется в медицине как гипотензивное средство.
Методы эксперимента
В сообщении 2 [2] описаны результаты подбора оптимального состава водно-липидной системы, которая включает этилолеат и воду в соотношении 1 : 3 по объему, эмульгатор - цетилтриметиламмоний бромид и катализатор - хлорид меди (II) в концентрациях (1-3)∙10-3 моль/л, приведены методики получения или очистки цетилтриметиламмония бромида, хлорида меди, этилолеата. Субстанции лекарственных препаратов выделяют из лекарственных форм по стандартным методикам государственной фармакопеи [9]. Окисление пробы осуществляют в термостатированной ячейке при непрерывном перемешивании при 60±0,2оС, объем поглощенного кислорода измеряют волюмометрически. Строят графические зависимости ![]() , в программном продукте Microsoft Word Excel. Кинетические кривые (КК) аппроксимируют по методу наименьших квадратов оптимальными одной или несколькими функциями, с последующим их дифференцированием и определяют количественные критерии эффективности антиоксидантов и механизма их действия. Подробности подхода приведены в сообщении 1 [1].
, в программном продукте Microsoft Word Excel. Кинетические кривые (КК) аппроксимируют по методу наименьших квадратов оптимальными одной или несколькими функциями, с последующим их дифференцированием и определяют количественные критерии эффективности антиоксидантов и механизма их действия. Подробности подхода приведены в сообщении 1 [1].
Кинетические кривые окисления водно-липидного субстрата в зависимости от концентрации пирокатехина приведены на рис. 1., а результаты математической обработки КК в табл. 1.
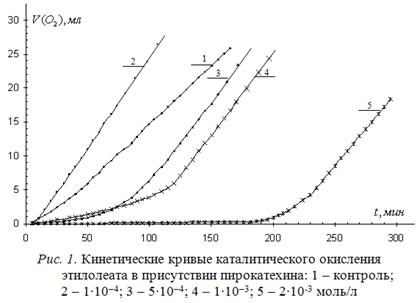
Таблица 1. Кинетические параметры окисления водно-липидного субстрата в присутствии пирокатехина
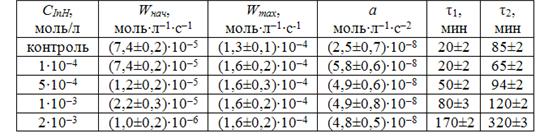
Показано резкое изменение характера влияния при изменении концентрации пирокатехина. При концентрации пирокатехина 1·10-4моль/л и 20-кратном избытке катализатора наблюдается резкое ускорение процесса, его протекание с максимальной скоростью примерно в два раза более высокой по отношению к контрольной пробе. При снижении избытка катализатора по отношению к пирокатехину возрастает эффективность торможения, происходит снижение начальной скорости процесса и периода торможения пропорционально концентрации пирокатехина. Максимальная скорость и ускорение не зависят от этих концентраций.
Представленные результаты могут быть объяснены конкуренцией нескольких реакций. При большом избытке катализатора, вероятно, весь пирокатехин израсходован на образование хелатного комплекса (1):
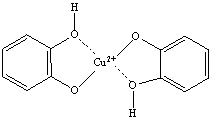
Судя по увеличению скорости окисления, вероятно, что этот комплекс является более сильным катализатором, чем хлорид меди (II).
При уменьшении избытка меди, концентрация такого комплекса уменьшается вплоть до полного исчезновения при концентрации пирокатехина 2·10-3моль/л. В этих условиях, пирокатехин существует, вероятно, в виде внутримолекулярного комплекса или комплексов с водой (2):
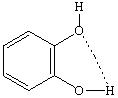
В этих условиях пирокатехин действует как сильный катализатор, эффективно обрывая цепи. После израсходования комплекса (2) процесс протекает под влиянием хелата (1), обеспечивая выход на максимальную скорость процесса. Показано, что некоординированный пирокатехин действует как сильный ингибитор, эффективно обрывающий цепи, комплекс с катионами меди оказываются более сильным катализатором, чем Cu2+.
Типичные КК окисления водно-липидного субстрата в зависимости от концентрации адреналина приведены на рис. 2.
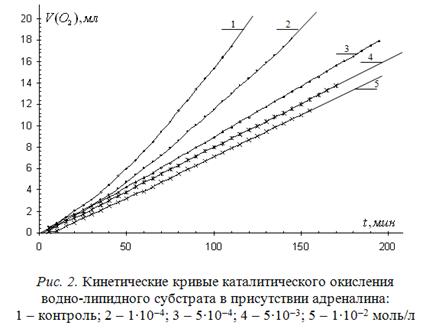
По характеру КК в присутствии адреналина отличаются от КК в присутствии пирокатехина. Адреналин слабо тормозит процесс. Окисление протекает практически без периода торможения, сопровождается уменьшением максимальной скорости пропорционально концентрации. Расчет кинетических параметров приведен в табл. 2.
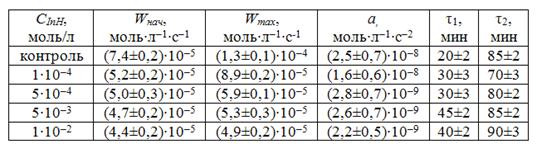
Из табл. видно уменьшение всех кинетических параметров с увеличением концентрации адреналина: начальная скорость уменьшается в 1,5-2 раза, максимальная - в 1,5-3 раза; ускорение - в 1,5-10 раз по сравнению с кинетическими параметрами контрольной пробы. Снижение начальной и максимальной скоростей, вероятно, связано с превращением части катализатора в менее активную форму Cu1+ и участие продуктов окисления адреналина в реакциях обрыва цепей.
Таблица 2. Кинетические параметры окисления водно-липидного субстрата в присутствии адреналина
При сравнении кинетических параметров окисления субстрата в присутствии одинаковых концентраций адреналина и пирокатехина наблюдается уменьшение всех кинетических параметров и отсутствие периодов полного торможения в присутствии адреналина, что свидетельствует о более низкой антиоксидантной активности адреналина.
КК окисления водно-липидного субстрата в зависимости от концентрации метилдофы приведены на рис. 3, а результаты математической обработки КК в табл. 3.
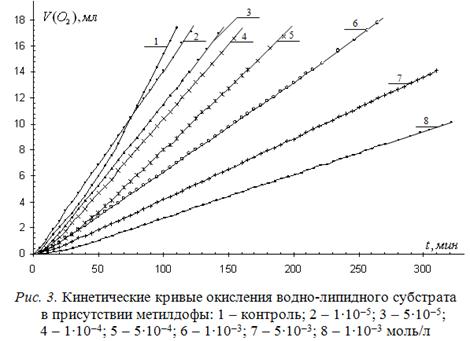
Таблица 3. Кинетические параметры окисления водно-липидного субстрата в присутствии метилдофы
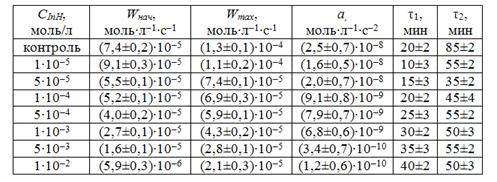
Показано, что при соотношении ингибитора и катализатора 1:200 наблюдается ускорение процесса, увеличение начальной и снижение максимальной скоростей по сравнению с кинетическими параметрами контрольной пробы. При соотношении 1:40 и ниже наблюдается снижение периодов окончания ускорения без периодов полного торможения и замедление процесса окисления в 1,5-15 раз во всех стадиях практически пропорционально увеличению концентрации ингибитора. Полученные результаты свидетельствуют об отсутствии эффекта комплексообразования метилдофы с катионами меди. Снижение максимальной скорости свидетельствует об участии продуктов окисления в реакциях обрыва цепей, а отсутствие периода полного торможения - о низкой антиоксидантной активности метилдофы в водно-липидном субстрате.
Сравнение кинетических параметров окисления водно-липидного субстрата в присутствии одинаковых концентраций лекарственных препаратов и адреналина (табл. 4) показывает, что минимальная величина начальной скорости и наибольшая величина значения периода полного торможения свидетельствует об эффективном участии пирокатехина в реакциях обрыва цепей.
Таблица 4. Кинетические параметры окисления водно-липидного субстрата в присутствии ингибиторов в концентрации 5·10-4 моль/л
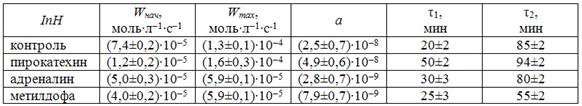
Из табл. 4 видно уменьшение антиоксидантной активности препаратов в ряду: пирокатехин > адреналин > метилдофа.
Предложенная модель позволяет оценить процесс комплексообразования ингибитора и катализатора и механизм их действия. Показана высокая эффективность водно-липидной модели для тестирования лекарственных препаратов.
СПИСОК ЛИТЕРАТУРЫ:
- 1. Журавлева Л.А. Кинетические подходы к проблеме тестирования антиоксидантов. С.1. Метиллинолеатная модель / Л.А. Журавлева, В.Н. Ушкалова // Современные проблемы науки и образования. - 2008. - № 3. - С. 143 - 153.
- 2. Журавлева Л.А. Кинетические подходы к проблеме тестирования антиоксидантов. С.2. Водно-липидная модель / Л.А. Журавлева, В.В. Крайник, В.Н. Ушкалова // Современные проблемы науки и образования. - 2008. - № 3. - С. 154 - 161.
- 3. Журавлева Л.А. Кинетические подходы к проблеме тестирования антиоксидантов. С.3. Тестирование некоторых лекарственных препаратов / Л.А. Журавлева, В.Н. Ушкалова // Современные проблемы науки и образования. - 2008. - № 3. - С. 162 - 168.
- 4. Байрамов В.М. Основы химической кинетики и катализа / Под ред. В.В. Лукина. - М.: Академия, 2003. - 256 с.
- 5. Рогинский В.А. Фенольные антиоксиданты. - М.: Наука, 1988. - 247 с.
- 6. Сторожок Н.М. Взаимосвязь между ингибирующими свойствами и активностью феноксильных радикалов антиоксидантов различного химического строения / Н.М. Сторожок, Н.В. Гуреева, А.П. Крысин, В.Е. Борисенко, И.Ф. Русина, Н.Г. Храпова, Е.Б. Бурлакова // Кинетика и катализ. - 2004. - Т. 45, № 4. - С. 519-527.
- 7. Бурлакова Е.Б. Изучение суммарной активности природных антиоксидантов липидов хемилюминесцентным методом / Е.Б. Бурлакова, Н.М. Сторжок, Н.Г. Храпова // Биофизика. - 1988. - Т. 33. - вып. 4. - С. 584 - 588.
- 8. Харитонова А.А. Кинетический анализ свойств антиоксидантов в сложных композициях с помощью модельной цепной реакции / А.А. Харитонова, З.К. Козлова, Б.Ф. Цепалов, Г.П. Гладышев // Кинетика и катализ. - 1979. - Т. 20. - № 3. - С. 593 - 599.
- 9. Государственная фармакопея СССР / Под ред. М.Д. Машковского. - М.: Медицина, 1987. - 333 с.
Библиографическая ссылка
Журавлева Л.А., Усманова Г.А., Ушкалова В.Н. КИНЕТИЧЕСКИЕ ПОДХОДЫ К ПРОБЛЕМЕ ТЕСТИРОВАНИЯ АНТИОКСИДАНТОВ. С. 4. АНТИОКСИДАНТНЫЕ СВОЙСТВА ПИРОКАТЕХИНА И ЕГО ПРОИЗВОДНЫХ // Современные проблемы науки и образования. 2009. № 3. ;URL: https://science-education.ru/en/article/view?id=1197 (дата обращения: 17.05.2026).



