Scientific journal
Modern problems of science and education
ISSN 2070-7428
"Перечень" ВАК
ИФ РИНЦ = 0,936
TECHNOLOGICAL RESEARCH NONINVASIVE OF WOUND COVERINGS WITH THE JUICE OF PLANTAIN AND ANALYSIS OF THE ADSORPTION OF BIOLOGICALLY ACTIVE SUBSTANCES JUICE ON COLLAGEN
Современные перевязочные средства по своему дизайну и свойствам существенно отличаются от традиционных. Под термином «раневое покрытие» подразумеваются не только привычные текстильные материалы (марля, сетка, трикотаж, нетканое полотно), но и пленки, пленкообразующие композиции, губки, гидроколлоиды, гели, порошки, пасты, комбинации различных материалов.
Раневое покрытие должно дренировать раневую поверхность, поддерживать оптимальный микроклимат, повязка должна хорошо моделироваться на ране, быть атравматичной, обеспечивать возможность бесконтактного визуального контроля за раной, не оказывать токсического и местнораздражающего действия, защищать от проникновения патогенной микрофлоры из окружающей среды. Перевязочное средство должно обладать лечебным действием, поэтому многие из них являются носителями биологически активных веществ, десорбируемых в рану в необходимой дозировке [3; 4].
Целью наших исследований являлись разработка состава, технологии атравматичного раневого покрытия с соком подорожника и анализ адсорбции биологически активных веществ на коллагене.
Противовоспалительный, рано- и язвозаживляющий эффекты сока подорожника связаны с наличием полисахаридов, пектиновых и дубильных веществ, бензойной и салициловой кислот. Полисахариды активизируют интерферонообразование, цинк и флавоноиды способствуют нормализации фагоцитоза [1; 2].
Известно, что препараты из свежесобранного сырья проявляют гораздо более высокую терапевтическую активность за счет сохранения исходного количества биологически активных веществ [6]. По традиционной схеме нами был наработан сок из свежесобранных листьев растения, выход сока составил около 50%. Оптимальным пленкообразователем, способным сформировать пленку-матрицу после проведения отсеивающего эксперимента, был выбран коллаген сухой фармацевтический (лиофильно высушенная и измельченная масса коллагена), для растворения которого использовали полученный сок подорожника. Уникальная молекулярная структура коллагена, наличие на его поверхности большого количества активных функциональных группировок позволяют использовать его в качестве матрицы для иммобилизации различных биологически активных и лекарственных веществ. Преимущество коллагена перед синтетическими полимерами, применяемыми с этой целью, заключается в том, что он полностью утилизируется организмом. С целью придания пленкам необходимой эластичности в состав вводили пластификатор-натальгин (альгинат натрия), в концентрации 3%, способный обеспечить пленкам достаточную пластичность, технологичность и хороший внешний вид [5].
Пленки получали методом полива пленочной массы. Суть технологии атравматичного раневого покрытия методом полива заключалась в возможности включения биологически активных веществ подорожника в виде молекулярных растворов в носитель (коллаген), и после удаления растворителя в получении эластичной, гомогенной пленки.
Предложена технологическая схема производства покрытия, включающая вспомогательные работы, основные стадии технологического процесса, упаковки, маркировки.
Ввиду того что раневые покрытия предлагается применять для лечения ожогов, инфицированных и долго незаживающих ран, травмированных тканей (ушибы, порезы), их получение предусматривает соблюдение условий, предотвращающих микробное и другое загрязнение на всех этапах технологического процесса, т.е. асептики.
С целью подтверждения эффективности использования коллагена в качестве основы для получения атравматических раневых повязок был проведен дифференциальный термический (калориметрический) анализ адсорбции биологически активных веществ сока подорожника большого на коллагене.
Для измерения теплового эффекта адсорбции был использован лабораторный комплекс УЛК «ХИМИЯ». Для измерений использовался термодатчик (разъем «1»). Подключали модуль «Термостат» к модулю «Контроллер», который с помощью провода RS-232 к COM-порту соединялся с компьютером.
Для проведения эксперимента отмеривали в стакан № 1 30 мл сока подорожника, приблизительно 25 мл из них помещали в стакан № 2, стакан № 1 с оставшимися 5 мл сока устанавливали в непосредственной близости от калориметра, чтобы его температура не отличалась от температуры воды в калориметре.
В стакан № 2 опускали чисто вымытый магнитный стержень и помещали стакан в калориметр, закрывали последний крышкой с термодатчиком, так чтобы термодатчик попадал в стакан. В большое отверстие в крышке калориметра вставляли воронку.
Во вкладке «Управление» окна программы «Система управления» включали магнитную мешалку и регулировали скорость ее вращения. Нами была выбрана скорость 2 для того, чтобы снизить количество выделяемой энергии при трении магнитного стержня о дно стаканчика и ее влияние на измерения.
На вкладке «Управление» выбирали кнопку «Текущее состояние» и устанавливали параметр «Число измерений» равным 30, а параметр «интервал измерений» - равным 30 секундам.
Через 10 минут после включения во вкладке «Управление» выбирали кнопку «Измерение» и проводили его в течение 5 минут (300 секунд) (предварительный период).
По истечении 300 секунд в калориметрический сосуд вносили точную навеску коллагена (частички адсорбента, приставшие к воронке и к стенкам сосуда, смывали 5 мл сока подорожника из стакана № 1).
Продолжили измерение температуры до окончания ее понижения (главный период).
После начала повышения температуры вели измерение еще 300 секунд (заключительный период) и нажимали в окне «Обмен данными с контроллером» кнопку «Стоп».
Открывали вкладку «Графики» и на панели инструментов выбирали кнопку «Добавить рабочий график» («+»): в открывшемся окне «Выберите канал» в поле «На Х» выбирали «Время», в поле «На Y» выбирали «1. Термодатчик» и нажимали «Принять».
Полученные данные сохранялись в текстовом документе, и в последующем по ним нами были построены графики в программе Excel.
По вышеописанной методике были проведены эксперименты с соком подорожника в концентрациях 60, 70, 80, 90 и 100%.
По полученным экспериментальным данным строились графики в координатах температура – время, которые представлены на рисунке 1.
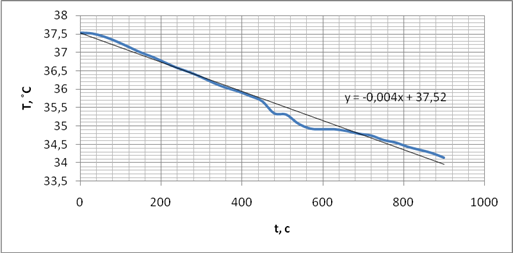
Рисунок 1 – Температурная кривая адсорбции БАВ 100%-ного сока подорожника на коллагене
Далее методом наименьших квадратов для каждой температурной кривой было получено уравнение усредняющей прямой и вычислено изменение температуры, вызванное адсорбцией по формуле:
![]() ,
,
где t – время, с
T – температура, °C
a – константа уравнения усредняющей прямой, K/с
b – константа уравнения усредняющей прямой, К
ΔT – изменение температуры, вызванное адсорбцией, К
Дифференциальная температурная кривая адсорбции БАВ 100%-ного сока подорожника на коллагене представлена на рисунке 2.
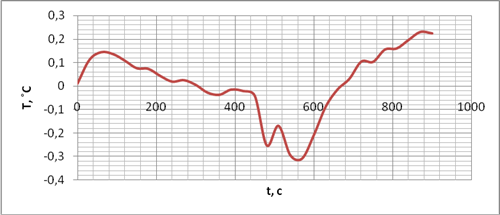
Рисунок 2 – Дифференциальная температурная кривая адсорбции БАВ 100%-ного сока подорожника на коллагене
В качестве контрольного образца для определения теплового значения калориметра была измерена теплота растворения калия хлорида в воде очищенной.
Тепловое значение калориметра:
![]() ,
,
где n – количество вещества в молях;
∆H – теплота растворения KCl, кДж/моль;
∆T – изменение температуры при растворении KCl , К.
Согласно полученным экспериментальным данным проводился расчет теплового значения калориметра:
W=![]() кДж/К.
кДж/К.
Для определения содержания адсорбируемых на коллагене веществ был проведен опыт по определению сухого остатка сока подорожника большого. Для этого на аналитических весах взвешивалась выпарительная чашка с точно известной массой (26,0890 г), с соком подорожника, ее средний вес по результатам 3-х последовательных измерений составил 32,5900 г. На водяной бане проводили выпаривание до полного испарения жидкости, затем помещали в сухожаровой шкаф на 30 минут, затем взвешивали и снова помешали в сушильный шкаф до тех пор, пока разница между двумя последними измерениями не превысила 0,005. Масса выпарительной чашки после высушивания составила 26,3890.
Таким образом, мы получили данные о содержание сухих веществ в соке подорожника большого различной концентрации (табл. 1).
Таблица 1 – Содержание сухих веществ в соке подорожника большого
|
Концентрация сока подорожника |
Содержание сухих веществ, в % |
|
100% |
4,63 |
|
90% |
4,167 |
|
80% |
3,704 |
|
70% |
3,241 |
|
60% |
2,778 |
Нами была рассчитана энергия в джоулях, выделившаяся при адсорбции для каждого раствора для каждой концентрации сока (Х1), по формуле:
![]() ,
,
где ∆T – изменение температуры, вызванное адсорбцией, К;
W – тепловое значение калориметра, кДж/К.
Из таблицы видно, что Х1 зависит от концентрации сухих веществ подорожника (коэффициент корреляции R2 = 0,66), что свидетельствует о том, что эти вещества адсорбируются на коллагене.
И была определена энергия в Дж на 1 кг адсорбента на 1 кг сухого вещества подорожника (Х2):
![]()
Таблица 2 – Тепловые эффекты адсорбции БАВ сока подорожника большого на коллагене
|
Концентрация сока подорожника, % |
Х1, кДж |
Х2, кДж/(кг·кг) |
|
60 |
0,0034704 |
0,024985 |
|
70 |
0,006507 |
0,0401543 |
|
80 |
0,0198825 |
0,1074 |
|
90 |
0,010845 |
0,052052 |
|
100 |
0,023136 |
0,09994 |
Среднее значение для Х2 составило 0,06490626 ±0,025842.Среднее значение Х2 может быть использовано для сравнения между собой различных адсорбентов.
Значительный тепловой эффект наблюдается при диапазоне концентраций БАВ 4,63- 3,704%.
Таким образом, в результате проведенных исследований установлено, что зависимость теплового эффекта адсорбции от концентрации биологически активных веществ подтверждает целесообразность использования коллагена в качестве основы для атравматичного раневого покрытия с соком подорожника.
Рецензенты:
Компанцева Е.В., д.фарм.н., профессор кафедры фармацевтической химии Пятигорского медико-фармацевтического института – филиала ГБОУ ВПО «ВолгГМУ Минздрава России», г. Пятигорск.
Хаджиева З.Д., д.фарм.н., профессор кафедры технологии лекарств Пятигорского медико-фармацевтического института – филиала ГБОУ ВПО «ВолгГМУ Минздрава России», г.Пятигорск.
Библиографическая ссылка
Кузнецова Л.С., Глушко А.А. ТЕХНОЛОГИЧЕСКИЕ ИССЛЕДОВАНИЯ АТРАВМАТИЧНОГО РАНЕВОГО ПОКРЫТИЯ С СОКОМ ПОДОРОЖНИКА И АНАЛИЗ АДСОРБЦИИ БИОЛОГИЧЕСКИ АКТИВНЫХ ВЕЩЕСТВ СОКА НА КОЛЛАГЕНЕ // Современные проблемы науки и образования. 2013. № 6. ;URL: https://science-education.ru/en/article/view?id=11775 (дата обращения: 02.06.2026).



