Scientific journal
Modern problems of science and education
ISSN 2070-7428
"Перечень" ВАК
ИФ РИНЦ = 0,936
THE ROLE OF POLYPROPYLENE IMPLANT IN THE TREATMENT OF PATIENTS WITH GASTROESOPHAGEAL REFLUX DESEASE AND HIATAL HERNIA
Введение
Грыжа пищеводного отверстия диафрагмы (ГПОД) – это смещение в средостение желудка, его части или иного органа из брюшной полости, пищеводное отверстие диафрагмы при этом является грыжевыми воротами.
ГПОД чаще проявляется вместе с гастроэзофагеальной рефлюксной болезнью (ГЭРБ). Симптомы грыжи, как правило, вызываются ГЭРБ. ГПОД вместе с ГЭРБ в настоящее время занимают одно из ведущих мест в современной гастроэнтерологии.
Согласно определению ВОЗ, ГЭРБ – это хроническое рецидивирующее заболевание, возникающее в результате регулярного заброса агрессивного желудочного содержимого в пищевод, с развитием характерных клинических симптомов (изжоги, отрыжки кислым) и, приводящее к повреждению слизистой оболочки с образованием эрозий и язв.
В последнее десятилетие значительно снизилась потребность в оперативном лечении благодаря высоким возможностям медикаментозной терапии, которая позволяет избавлять большинство больных от симптомов ГЭРБ, но не способна устранить те анатомические изменения, которые создают предпосылки для развития заболевания при ГПОД. Поэтому у значительной части больных с нарастающей симптоматикой или развитием осложнений, необходимость оперативного лечения становится очевидна. Однако на сегодняшний день остается ряд нерешенных проблем хирургического лечения ГЭРБ и ГПОД. В частности: при открытом доступе особенно травматично проходит этап мобилизации и последующего образования муфты; по литературным данным все больные до и 56% после операции имеют функциональные расстройства работы желудка и двенадцатиперстной кишки, проявляющиеся болями, чувством распирания, тяжести, переполнения и другими.
Главная, с нашей точки зрения, причина - нарушения иннервации, связанные с травматизацией блуждаюших нервов, как до операции, так и в последующем вследствие многократных перемещений через пищеводное отверстие диафрагмы пищеводно-желудочного перехода до операции и вынужденно во время его выделения интраоперационно. В основе ГЭРБ лежит нарушение замыкательной функции пищевода (кардии) и развивающееся в последующем поражение его слизистой оболочки вплоть до злокачественного перерождения [1, 6]. Для улучшения результатов лечения ГПОД и ГЭРБ совершенствуются классические антирефлюксные операции (по Nissen, Toupet, Rampalle, А.Ф.Черноусову), но и они не всегда полностью удовлетворяют пациентов и хирургов [3, 5]. Поэтому продолжается поиск, в том числе малоинвазивных, эндоскопических методов, которые направлены на уменьшение травматизации пищеводно-желудочного перехода и улучшение функциональных результатов [2, 4].
Цель исследования: изучить и сравнить результаты антирефлюксных операций по классической методике и с помощью полипропиленового имплантата (авторский способ).
Материалы и методы исследования
Для уменьшения травматизации, улучшения фиксации, создания полноценного угла Гиса нами используется метод, прототипом которого является методика изменения угла Гиса выкроенной круглой связкой печени по Rampal (рис. 1).
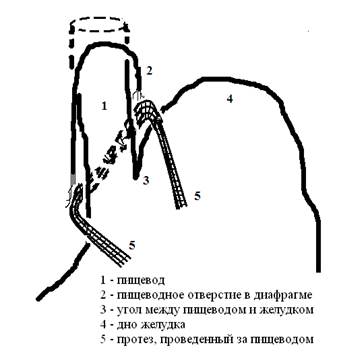
Рис. 1 Метод фиксации угла Гиса полипропиленовой лентой.
Поскольку такая структура как круглая связка не является достаточно крепкой для фиксации угла Гиса, мы используем полипропиленовую сетку, смоделированную в виде ленты, которую подшиваем по оригинальной методике (способ профессора А.А. Баулина – Патент № 2 431 448). Способ реализуется, как классическим доступом, так и эндоскопическим. Операция может выполняться по общепринятым канонам: выделяются ножки диафрагмы, производится крурорафия, желудок фиксируется имплантатом, проведенным позади пищевода к передней брюшной стенке. В обязательном порядке при открытом способе производим пилоропластику как второе дополнение. С нашей точки зрения, при ГПОД всегда происходит, а после операции усугубляется, травматизация блуждающих нервов, и как следствие этого возникают эвакуаторные расстройства. Первые операции показали, что не обязательно выполнять крурорафию и создавать муфту вокруг пищевода, поскольку установленный сетчатый имплантат полностью восстанавливает замыкательную функцию кардии. Отсутствует смещение органов в средостение, отсутствует рефлюкс и смещение пищеводно-желудочного перехода, что доказано рентгенологически, а эндоскопически подтверждается регресс патологических изменений в нижней трети пищевода, воссоздаётся клапан Губарева, кардия смыкается (рис. 2).
а 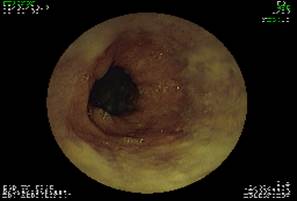
б 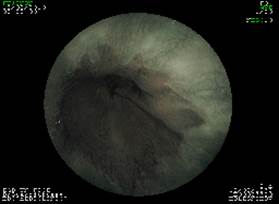
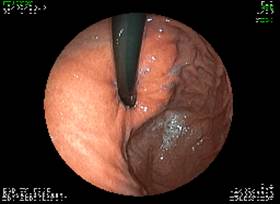
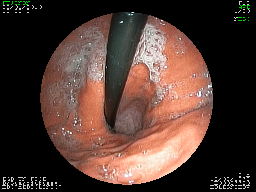
Рис. 2 Вид слизистой оболочки пищевода (слева - с применением электронной хромоскопии) и слизистой оболочки кардии (справа - в естественном свете) до операции (а) и после операции (б).
В окончательном варианте видеоэндоскопическая операция выглядит следующим образом (рис. 3). Эндоскоп устанавливаем у пупка (№ 4), два 11 мм порта в подреберьях справа (№ 2) и слева (№ 3) симметрично, 5 мм справа по среднеключичной линии на 5 см ниже подреберья (№ 1).
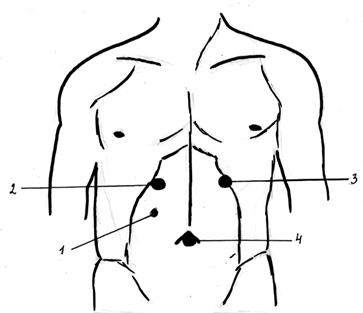
Рис. 3 Оригинальная методика расстановки троакаров. Стрелками указаны: 1 – 5-мм троакар по среднеключичной линии справа на 5 см ниже подреберья; 2 – 11-мм троакар в правом подреберье; 3 – 11-мм троакар в левом подреберье; 4 – эндоскоп у пупка.
После осмотра и отведения левой доли печени ретрактором из доступа № 2, желудок за тело и дно переводим в брюшную полость. Анестезиолог вводит в пищевод толстый зонд, наблюдаем за его прохождением - это значительно облегчает поиск пищевода, ориентировку по стенкам. Рассекаем (расслаиваем) брюшину ближе к стенке желудка в свободной от сосудов зоне в области перехода левой стенки пищевода в дно желудка (угол Гиса). Это место ориентирует точку выхода инструмента справа-налево или используем её для проведения специального изгибающегося инструмента слева-направо. Вскрываем малый сальник в бессосудистой зоне. Постепенно тупо инструментом из 1-ой точки, помогая другими инструментами, слева от края правой ножки вскрываем париетальную брюшину и попадаем в клетчатку позади пищеводно-желудочного перехода, где осторожно формируем и расширяем тоннель. Зажим выходит без усилий с противоположной стороны. В брюшную полость доставляется свёрнутый в виде ленты сетчатый имплантат и подается к зажиму. Лента проводится позади пищеводно-желудочного перехода, концы ее выравниваются по длине. Зажимами из 11 мм портов концы ленты выводятся наружу, пальцами прижимаются отверстия с целью герметизации брюшной полости. Визуально определяем месторасположение имплантата, контролируем, что зонд расположен в петле, нивелируем степень натяжения ленты. Кожные разрезы в подреберьях при необходимости немного увеличиваем для фиксации концов сетки к передней стенке влагалищ прямых мышц живота двумя швами. Иногда устанавливаем 2 тонких дренажа к месту операции. Пневмоперитонеум распускаем, накладываем швы на кожу.
Результаты исследования и их обсуждение
По новой методике оперировано 118 больных (группа сравнения), в качестве контрольной группы отобраны пациенты, которым выполнялась фундопликация по Ниссену.
Мы изучили эндоскопическую и рентгенологическую картину на предмет изменений слизистой, эвакуаторных расстройств функции пищевода, желудка, 12-перстной кишки у 68 больных контрольной группы с ГПОД до операции и у 28 – после – по Ниссену. Операции сопровождались осложнениями: повреждение стенки пищевода и желудка – 2, спленэтомия – 2, прорезывание швов диафрагмы – 2, кровотечение из зоны операции – 2, различные послеоперационные осложнения – 6, в том числе 3 с гиперфункцией муфты. До операции у всех отмечалось зияние, заброс, воспалительные изменения слизистой, пролабирование в пищевод и другие. Рентгенологически: несвоевременное начало эвакуации, задержка полной эвакуации, явления дискордантных движений 12-перстной кишки, опущение нижней границы тела желудка, явления гастродуоденостаза и другие. В сроки более 12 месяцев у 67,7% заброс в пищевод не отмечается, однако у 85,3% произошло клинически и рентгенологически усугубление эвакуаторных расстройств в виде гастростаза и опущения тела желудка в малый таз. 70% больных ощущают боли, дискомфорт и переполнение желудка, причем у большинства более тягостный, чем до операции. Эндоскопически натощак в желудке определялась мутная жидкость, у некоторых в довольно большом количестве, примесь жёлчи, отмечался дуоденально-гастральный рефлюкс, явления гастрита и другие. Больные с пилоропластикой подобные явления не отмечали совсем или в меньшей степени, эвакуаторных расстройств не выявлялось.
В группе сравнения из 85 больных получены обнадёживающие результаты. Осложнение возникло у 4 больных: у одной связано с повреждением стенки желудка зондом и инфицированием, сетку пришлось удалить; у второго из-за нагноения вокруг имплантата - лапароскопически сетку удалили; у двух происходит прорезывание протеза без клинических проявлений с хорошим субъективным и объективным исходом, проводим контрольные эндоскопии, сроки наблюдения более 2 лет. Послеоперационный период протекает легче, сроки госпитализации короче, лишь у двух больных отмечались явления дисфагии до 1,5 месяцев, у одной прошли полностью самостоятельно, у второй потребовалась повторная операция – отсечение одного из концов сетки, выполнена лапароскопически, явления дисфагии регрессировали. Сроки наблюдения всех больных до 5-ти лет. Больные с пилоропластикой клинически не отмечали эвакуаторных расстройств, рентгенологически они были менее выраженные. Результаты мы оценили как хорошие. Все больные обследованы эндоскопически и рентгенологически, замыкательная функция восстановлена у 93 %, эзофагит регрессировал, складка Губарева хорошо выражена, недостаточность кардии 1 степени сохранилась у 4, от коррекции воздерживаются, так как клинически чувствуют себя хорошо. Рентгенологически у части больных находят данные, которые трактуют как за ГПОД (следует подчеркнуть, что мы и не зашивали пищеводное отверстие диафргамы), эвакуаторных расстройств желудка нет, у одной больной сохраняются явления эзофагита и замедление эвакуации (хотя эндоскоп проходит свободно).
Выводы
1. Неблагоприятные исходы классических операций связаны с методикой операции и с тем, что до операции уже происходит травматизация блуждающих нервов, а во время нее усугубляется.
2. Первый опыт даёт основание считать перспективным направление лечения ГЭРБ и ГПОД с применением малотравматичного метода восстановления угла Гиса фиксацией пищеводно-желудочного перехода имплантатом по оригинальной методике.
3. Одним из важных дополнений при открытых операциях мы считаем выполнение пилоропластики, что улучшает функциональные результаты операций и ликвидирует расстройства в отдалённом периоде.
Рецензенты:
Смолькина А.В., д.м.н., профессор кафедры госпитальной хирургии медицинского факультета им. Т.З. Биктимирова ФГБО ВПО «Ульяновский государственный университет», г.Ульяновск.
Зимин Ю.И., д.м.н., доцент кафедры онкологии ГБОУ ДПО «Пензенский институт усовершенствования врачей» Минздрава России, г. Пенза.
Библиографическая ссылка
Баулин А.А., Баулин В.А., Стародубцев В.А., Баулина О.А., Сигаева Н.С., Баулина Е.А., Креймер В.Д., Акжигитова А.А., Стешкина И.В. РОЛЬ ПОЛИПРОПИЛЕНОВОГО ИМПЛАНТАТА В ЛЕЧЕНИИ ПАЦИЕНТОВ С ГАСТРОЭЗОФАГЕАЛЬНОЙ РЕФЛЮКСНОЙ БОЛЕЗНЬЮ И ГРЫЖАМИ ПИЩЕВОДНОГО ОТВЕРСТИЯ ДИАФРАГМЫ // Современные проблемы науки и образования. 2013. № 6. ;URL: https://science-education.ru/en/article/view?id=11548 (дата обращения: 16.05.2026).



