Scientific journal
Modern problems of science and education
ISSN 2070-7428
"Перечень" ВАК
ИФ РИНЦ = 0,936
EARLY PATHOGENESIS MECHANISMS OF KIDNEY AND LIVER LESIONS WITH BREAKING OXIDATIVE PHOSPHORYLATION
Введение. Известно, что введение 2,4 – динитрофенола вызывает развитие острой тканевой гипоксии [4] из-за разобщения процессов окисления и фосфорилирования, что приводит к расстройству функции почек с нарушением главного энергозависимого процесса - реабсорбции ионов натрия, белка в проксимальном отделе нефрона, повреждения печени [1]. В развитии ранних механизмов повреждения печени и почек при данных условиях могут играть цитокины, продукты окислительной модификации белков с формированием синдромов транслокации и потери ионов натрия с мочой. Как средство патогенетической коррекции этих нарушений целесообразно использовать антиоксидант мелатонин.
Цель исследования. Выяснить ранние механизмы повреждения печени и почек при условии гипонатриевого рациона питания в условиях острой тканевой гипоксии, вызванной введением 2,4-динитрофенола с разработкой путей патогенетической коррекции выявленных нарушений путем использования мелатонина.
Материал и методы исследования
В экспериментах на 120 самцах белых нелинейных крыс массой 0,16-0,20 кг исследовали острую тканевую гипоксию, которую моделировали путем введения 0,1% раствора 2,4- динитрофенола внутрибрюшинно в дозе 3 мг/кг однократно [3]. Устойчивость крыс к острой гипоксии оценивали по времени потери позы на “высотном плато“ острой гипобарической гипоксии и временем общего пребывания животных от момента достижения “высоты“ 12000 м до появления второго агонального вдоха (время жизни или резервное время), а также с учетом времени восстановления позы с момента начала спуска. Выделяли 3 группы животных: высоко-, средне- и низкоустойчивые [2]. Все дальнейшие исследования проводили на среднеустойчивых крысах.
Участки тканей печени и почек фиксировали в течении 48 часов в 10% растворе нейтрального забуференного формалина, после чего проводили процедуру обезвоживания в восходящей батарее этанола и парафиновую заливку при температуре 580С. Для оценки окислительной модификации белков срезы гистохимически окрашивали бромфеноловым синим по Микель-Кальво. Компьютерную спектрометрию осуществляли при помощи компьютерной программы ColorPic (Graphic Art Tools, 2004). Способ гистохимического определения соотношения между основными и кислыми группами белков, основанный на измерении интенсивности красного и синего цветов спектра при компютерно-спектральном анализе цифровых изображений микроскопческих объектов и расчета коэфициента R/B, как соотношения между интенсивностью окрашивания в участке красного спектра (R) к интенсивности окрашивания в участке синего спектра (B) [6].
Функциональное состояние почек исследовали при условии водной нагрузки, для чего крысам внутрижелудочно, при помощи металлического зонда, вводили водопроводную воду подогретую до температуры 37оС в количестве 5% от массы тела. Величину диуреза (V) оценивали в мл/2 часа ּ100 г. После водной нагрузки с целью получения плазмы проводили эвтаназию животных путем декапитации под легким эфирным наркозом, кровь собирали в пробирки с гепарином. Скорость клубочковой фильтрации (Сcr) оценивали по клиренсу эндогенного креатинина, которую расчитывали по формуле:
Сcr = Ucr ּ V/Pcr
где Ucr и Pcr - концентрация креатинина в моче и плазме крови соответственно. Концентрации ионов натрия, калия в моче и плазме крови оценивали методом пламенной фотометрии, концентрацию белка мочи определяли сульфосалициловым методом. Исследовали проксимальную и дистальную реабсорбцию ионов натрия (ТрNa+, TdNa+). Расчеты проводили по формулам:
TpNa+ = (Ccr - V) ּ PNa+ ּ
TdNa+ = (PNa+- UNa+) ּ V [7]
Цитокины крови определяли иммуноферментным методом [2, 3, 4].
Экзогенный мелатонин вводили в дозе 3,5 мг/кг однократно [8].
Статистическую обработку полученных данных проводили на компютере с помощью программы “Statgrafics” и “Excell 7.0”. Все исследования выполнены на основании Конвенции Совета Европы по охране позвоночных животных, которых используют в экспериментах и других научных целях (от 18.03.1986 г.), Директивы ЕЭС № 609 (от 24.11.1986 г.), приказов МЗ Украины № 960 от 23.09.2009 г и № 944 от 14.12.2009 г.
Результаты исследования и их обсуждение. Результаты исследований показали возрастание концентраций фактора некроза опухолей-α, интерлейкина -1β, интерлейкина-6 в плазме крови (рис.1) через 2 часа после введения 2, 4 – динитрофенола в дозе 3 мг/кг в условиях гипонатриевого рациона питания.
При введении 2, 4 – динитрофенола величина мочевыделения снижалась, возрастала концентрация ионов калия, белка в моче, снижалась клубочковая фильтрация (табл. 1). Концентрации креатинина в плазме крови и моче не изменялись. Оценка транспорта ионов натрия при условии введения 2, 4 – динитрофенола характеризовалась возрастанием концентрации ионов натрия в моче. Проксимальная реабсорбция ионов натрия характеризовалась тенденцией к торможению, а дистальная реабсорбция этого электролита снижалась достоверно. Концентрация ионов натрия в плазме крови не изменялась.
На рис. 2 показан форест-график сравнительной оценки защитного влияния мелатонина на коэффициент R/B цитоплазмы эпителия проксимальних канальцев, экскрецию ионов натрия, клиренс ионов натрия, концентрационный индекс ионов натрия через 2 часа после введения 2, 4 – динитрофенола в дозе 3 мг/кг при условии гипонатриевого рациона питания при водном индуцированном диурезе в объеме 5% от массы тела. Контроль для всех исследований представлено в виде вертикальной линии и принято за 1.
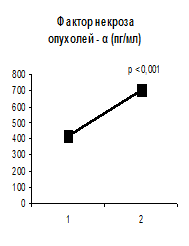
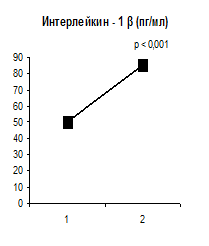
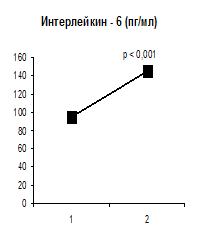
Рис.1. Концентрации фактора некроза опухолей- α, интерлейкина -1 β, интерлейкина - 6 в плазме крови (пг/мл) через 2 часа после введения 2, 4 – динитрофенола в дозе 3 мг/кг при условии гипонатриевого рациона питания при водном индуцированном диурезе в объеме 5% от массы тела.
1- контроль, 2 - введение 2, 4 – динитрофенола.
p – достоверность отличий в сравнении с контролем.
Таблица 1
Показатели функции почек через 2 часа после введения 2, 4 – динитрофенола в дозе 3 мг/кг при условии гипонатриевого рациона питания при водном индуцированном диурезе в объеме 5% от массы тела (x±Sx)
|
Показатели |
Контроль (n=10) |
2, 4 – динитро-фенол (n=10) |
|
Диурез, мл/2 час ∙ 100 г |
4,58±0,299 |
3,72±0,253 p< 0,05 |
|
Концентрация ионов калия в моче, ммоль/л |
15,30±1,963 |
26,90±4,394 p< 0,02 |
|
Концентрация креатинина в моче , ммоль/л |
1,46±0,086 |
1,41±0,058 |
|
Концентрация креатинина в плазме крови, ммоль/л |
53,50±3,106 |
47,10±2,030 |
|
Клубочковая фильтрация, мкл/мин ∙100 г |
1096,6±136,57 |
919,1±42,61 |
|
Концентрация белка в моче, г/л |
0,019±0,0037 |
0,032±0,0063 |
|
Концентрация ионов натрия в моче, ммоль/л |
0,37±0,053 |
0,76±0,061 p< 0,001 |
|
Концентрация ионов натрия в плазме крови, ммоль/л |
135,5±1,89 |
136,0±1,675 |
|
Дистальная реабсорбция ионов натрия, мкмоль/2 часа ∙ 100 г |
618,1±40,88 |
503,5±34,73 p< 0,05 |
|
Проксимальная реабсорбция ионов натрия, ммоль/2 часа ∙ 100 г |
17,29±2,293 |
14,53±0,811 |
p – достоверность отличий в сравнении с контролем; n - число наблюдений.
Как видно из приведенного графика найболее существенное протекторное влияние в условиях опыта мелатонин выявлял на концентрационный индекс ионов натрия.
Введение 2,4-динитрофенола приводило к усилению окислительной модификации белков по возрастанию показателя R/B в проксимальных канальцах, мозговых толстых восходящих отделах петли нефрона, собирательных канальцах сосочка почек, в белковых массах цитоплазмы гепатоцитов (табл. 2).
Таблица 2
Степень окислительной модификации белков по коеффициенту R/B (усл. ед.) при гистохимическом анализе срезов почек и печени крыс после введения 2, 4 – динитрофенола и при действии мелатонина (Х±Sx)
|
Структура, где измерялся показатель R/B |
Группы исследования |
||
|
Контроль, интактные животные (n = 8) |
Введение 2,4-динитрофенола (n = 8) |
Введение 2,4-динитрофенола на фоне мела-тонина (n =8) |
|
|
Цитоплазма эпителия проксимальных канальцев |
1,08±0,005 |
1,39±0,009 p < 0,001 |
1,24±0,008 р1< 0,001 |
|
Цитоплазма эпителия мозговых толстых восходящих частей петли нефрона |
1,04±0,004 |
1,18±0,007 p < 0,001 |
1,05±0,004 р1< 0,001 |
|
Цитоплазма эпителия трубочек сосочка |
1,03±0,004 |
1,15±0,008 p < 0,001 |
1,04±0,005 р1< 0,001 |
|
Белковые массы цитоплазмы гепатоцитов |
1,12±0,006 |
1,26±0,009 p < 0,001 |
1,19±0,008 р1< 0,001 |
р – достоверность отличий в сравнении с контролем, р1- достоверность отличий в сравнении с введением 2,4-динитрофенола, n – число наблюдений.
Введение 2, 4 – динитрофенола обусловливало снижение уровня АТФ в почечных канальцах в среднем в 2 раза [2] за счет расщепления окисления и фосфорилирования. Дефицит АТФ обусловливал нарушения главного энергозависимого процесса почечных канальцев – реабсорбции ионов натрия, что приводило к развитию синдрома потери исследуемого катиона. Обозначенное подтверджено ростом концентрации ионов натрия в моче. Тенденция к снижению проксимальной реабсорбции ионов натрия обусловлена “скрытым” повреждением проксимального отдела нефрона [7], а вероятное снижение дистальной реабсорбции исследуемого катиона обусловлено тем, что процессы транспорта в дистальном канальце есть более энергозависимы нежели в проксимальном отделе нефрона.
В тоже время, степень проявлений синдрома потери был несущественным, поскольку концентрация ионов натрия в плазме крови не менялась, а несущественная активация ренин-ангиотензин-альдостероновой системы вызывала только вероятное снижение диуреза, возрастание концентрации ионов калия в моче при наличии тенденции к торможению клубочковой фильтрации. Повреждение баръеров кишечника и печени на фоне энергодефицита приводило к транслокации эндотоксина с просвета кишечника в кровь [5], который обусловливал возрастание концентраций фактора некроза опухолей-α, интерлейкина-1β и интерлейкина-6, которые у свою очередь вызывали дополнительные реакции повреждения почечных канальцев с усилением проявления синдрома потери ионов натрия.
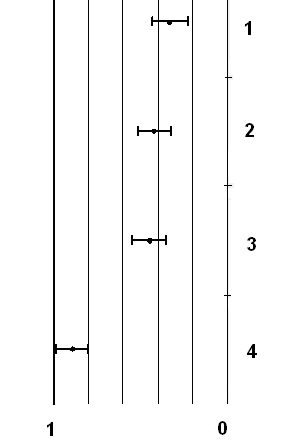
Рис. 2. Форест-график сравнительной оценки защитного влияния мелатонина на коеффициент R/B цитоплазмы эпителия проксимальных канальцев, экскрецию ионов натрия, клиренс ионов натрия, концентрационный индекс ионов натрия через 2 часа после введения 2, 4 – динитрофенола в дозе 3 мг/кг при условии гипонатриевого рациона питания при водном индуцированном диурезе в объеме 5% от массы тела.
1- концентрационный индекс ионов натрия (усл. ед.); 2- клиренс ионов натрия (мл/2 часа ∙ 100 г); 3- экскреция ионов натрия (мкмоль/2 часа ∙ 100 г); 4 – коефициент R/B цитоплазмы эпителия проксимальных канальцев – (усл. ед.); Контроль для всех исследований представлено в виде вертикальной линии и принято за 1.
При гипонатриевом рационе питания через 2 часа моделирования тканевой гипоксии после введения 2,4-динитрофенола установлено возрастание концентраций фактора некроза опухолей- α, интерлейкинов 1β и -6 в плазме крови, показано повышение степени окислительно-модифицированных белков в почках и печени крыс по коэфициенту R/B, которые вызывали повреждения печени и почек, нарушения энергетического обмена с развитием синдромов транслокации и потери ионов натрия с мочой с возрастанием его экскреции. Мелатонин за счет антиоксидантных свойств проявлял защитное влияние на течение псевдогепаторенального синдрома [9, 10] при тканевой гипоксии, который выявлял защитное влияние на степень окислительно-модифицированых белков в почках и печени крыс, уменьшал уровень коефициента R/B в проксимальных, дистальных отделах нефрона, собирательных канальцах сосочка почек и белковых массах цитоплазмы гепатоцитов в сравнении со значениями при интоксикации 2,4-динитрофенолом.
Вывод
В опытах на белых нелинейных половозрелых крысах-самцах при гипонатриевом рационе питания в условиях моделирования тканевой гипоксии с позиций доказательной медицины приведено теоретическое обобщение и новое решение научной задачи относительно ранних механизмов патогенеза псевдогепаторенального синдрома как основания ухудшения течения почечной и печеночной недостатности при разобщении окисления и фосфорилирования на фоне введения 2,4- динитрофенола.
Рецензенты:
Швец В.И., д.б.н., профессор, профессор кафедры физиологии имени Я.Д.Киршенблата Буковинского государственного медицинского университета МЗ Украины, г.Черновцы.
Заморский И.И., д.м.н., профессор, заведующий кафедрой фармакологии Буковинского государственного медицинского университета МЗ Украины, г.Черновцы.
Библиографическая ссылка
Роговый Ю.Е., Белявский В.В., Филипова Л.О., Дорошко В.А. РАННИЕ МЕХАНИЗМЫ ПАТОГЕНЕЗА ПОВРЕЖДЕНИЯ ПОЧЕК И ПЕЧЕНИ ПРИ РАЗОБЩЕНИИ ОКИСЛЕНИЯ И ФОСФОРИЛИРОВАНИЯ // Современные проблемы науки и образования. 2013. № 6. ;URL: https://science-education.ru/en/article/view?id=11345 (дата обращения: 27.04.2026).



