Scientific journal
Modern problems of science and education
ISSN 2070-7428
"Перечень" ВАК
ИФ РИНЦ = 0,936
RESEARCH OF SCN SORBENT USE CAPABILITY FOR WATER PURIFICATION FROM PHENOLS
Введение
В настоящее время существует проблема обеспечения населения качественной питьевой водой. Основным критерием качества питьевой воды является влияние ее состава на здоровье человека. Загрязнение источников водоснабжения примесями техногенной природы вызывает проблемы при водоподготовке. Наиболее часто встречаемыми, токсичными и одновременно трудноудаляемыми техногенными загрязнениями являются нефтепродукты и фенолы, концентрации которых могут достигать 1-40 ПДК (предельно допустимых концентраций) [1]. При хлорировании воды эти вещества способны образовывать галогенсодержащие соединения, обладающие высокой биологической активностью, что способствуют развитию злокачественных опухолей, генетических болезней и т.д. [4]. Современные требования к качеству питьевой воды становятся более жесткими, и традиционные методы (аэрация, коагуляция в сочетании с хлорированием и последующим фильтрованием через песчаные фильтры) ‒ не дают удовлетворительных результатов по удалению токсичных органических соединений. Поэтому в действующие схемы водоочистки необходимо включать дополнительные стадии обработки воды, например колонны с сорбентами. Новые сорбенты, например углеродные волокнистые материалы, волокнистый оксогидроксид алюминия, железоуглеродные сорбенты, обладают уникальными свойствами благодаря развитой поверхности, что обеспечивает сочетание высокой сорбционной емкости с высокими кинетическими характеристиками [5-7; 10]. Из известных сорбентов наиболее эффективными являются активированные угли. Они хорошо сорбируют фенолы, большинство нефтепродуктов, хлор- и фторорганические пестициды и т.д. [8]. В настоящее время одной из актуальных задач является проблема выбора эффективного сорбента, обладающего высокими сорбционными свойствами к тем или иным токсичным реагентам. Кроме того, современные сорбенты должны подвергаться регенерации, обладать высокой механической прочностью и утилизироваться без нарушения экологических норм.
Целью настоящей работы является изучение сорбционных характеристик энтеросорбента СКН в статическом и динамическом режимах и влияние ионов железа на динамическую емкость сорбента по отношению к фенолу.
Материалы и методы исследования
Объектами исследований в данной работе выступали – энтеросорбент СКН (гранулированная, модифицированная форма активированного угля), модельные растворы, содержащие в одном случае только фенол, в другом – фенол и ионы железа (II). Для приготовления модельных растворов использовали реактивы марки ЧДА – фенол по ГОСТ 6417, железо сернокислое по ГОСТ 4148, дистиллированную воду по ГОСТ 6709. Концентрацию фенола и железа определяли фотоколориметрически [3].
Сорбцию фенола в статическом режиме проводили по следующей методике. Стаканчики, содержащие одинаковое количество СКН (1 г), заполняли раствором с содержанием фенола в интервале от 5 до 35 мг объемом 50 мл и выдерживали при перемешивании в течение 24 часов. Указанное время соответствует времени достижения равновесной концентрации фенола в растворе [2].
При регистрации динамических кривых загружали фиксированную навеску СКН в колонну диаметром 1,8 см с разными высотами слоя сорбента – 0,82, 1,65, 3,30 см и пропускали через нее модельный раствор фенола с исходной концентрацией 10 мг/л, заведомо большей ПДК. Скорость протекания исходного раствора варьировалась и составляла 0,16, 0,50, 1,00, 1,50, 2,00, 3,00 л/ч, что соответствует в выбранной геометрии эксперимента линейным скоростям 0,015, 0,048, 0,096, 0,144, 0,192, 0,240 и 0,288 см/с.
Для определения динамической емкости СКН 35 л модельного раствора с концентрацией фенола 10 мг/л пропускали через колонку с навеской сорбента 10 г со скоростью 0,048 см/с.
Для установления влияния ионов железа на динамическую емкость сорбента по отношению к фенолу эксперимент проводили на модельном растворе, содержащем также 10 мг/л фенола и железа (II) в концентрации от 0,3 до 2,0 мг/л.
Результаты исследования
Результаты эксперимента по определению сорбции фенола на сорбенте СКН в статическом режиме представлены на рис. 1.
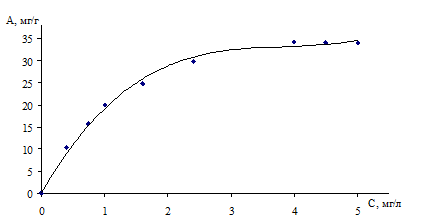
Рис. 1. Изотерма сорбции фенола на СКН
Полученная изотерма сорбции была обработана в координатах уравнения Лэнгмюра, которое обычно используется для определения константы равновесия при изучении механизма процесса сорбции.
![]()
![]() ,
,
где А – сорбированное количество фенола (мг/г),
![]() – предельная концентрация поглощенного фенола в адсорбенте (мг/г),
– предельная концентрация поглощенного фенола в адсорбенте (мг/г),
С – равновесная концентрация фенола (мг/л),
К – константа адсорбционного равновесия.
Как видно из рис. 2, в изученном интервале концентраций фенола изотерма сорбции хорошо описывается данным уравнением с коэффициентом корреляции ![]() . На основе изотермы сорбции, путем графического решения уравнения Лэнгмюра (рис. 2), были определены максимальная сорбционная емкость, которая составила 35,0 мг/г, и константа процесса сорбции, которая составила 1,17 л/мг соответственно.
. На основе изотермы сорбции, путем графического решения уравнения Лэнгмюра (рис. 2), были определены максимальная сорбционная емкость, которая составила 35,0 мг/г, и константа процесса сорбции, которая составила 1,17 л/мг соответственно.
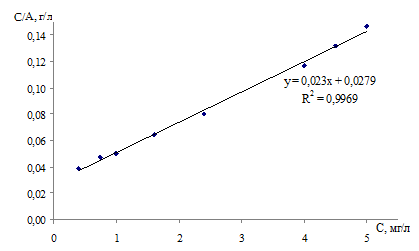
Рис. 2. Линеаризованная форма изотермы сорбции
Результаты эксперимента по определению сорбции фенола в динамическом режиме приведены в табл. 1.
Таблица 1. Концентрация фенола в фильтрате при различных скоростях ![]() пропускания модельного раствора с концентрацией фенола 10 мг/л и различной высоте слоя сорбента
пропускания модельного раствора с концентрацией фенола 10 мг/л и различной высоте слоя сорбента
|
|
|
|
|||
|
|
[фенол], мг/л |
|
[фенол], мг/л |
|
[фенол], мг/л |
|
0,015 |
н/о |
0,048 |
н/о |
0,048 |
н/о |
|
0,048 |
0,10 |
0,096 |
0,10 |
0,144 |
н/о |
|
0,096 |
0,25 |
0,144 |
0,15 |
0,192 |
н/о |
|
0,144 |
0,50 |
0,192 |
0,50 |
0,240 |
0,10 |
|
0,240 |
1,10 |
0,288 |
1,00 |
0,288 |
0,15 |
Из таблицы видно, что появление проскоковой концентрации фенола зависит как от высоты слоя сорбента, так и от скорости протекания раствора. Используя экспериментальные данные табл. 1 и методику расчета, приведенную в работе [2], по сорбционной очистке воды от растворимых органических компонентов на углях, был построен график зависимости длины сорбционного слоя СКН от скорости протекания раствора при появлении проскоковой концентрации фенола (рис. 3). Как видно из рисунка, зависимость ![]() линейна. Тангенс угла наклона полученной прямой характеризует кинетический коэффициент внешней диффузии в соответствии с уравнением [2]:
линейна. Тангенс угла наклона полученной прямой характеризует кинетический коэффициент внешней диффузии в соответствии с уравнением [2]:
![]() ,
,
где ![]() – кинетический коэффициент внешней диффузии (с-1),
– кинетический коэффициент внешней диффузии (с-1),
![]() – безразмерная величина, характеризующая характер процесса диффузии,
– безразмерная величина, характеризующая характер процесса диффузии,
![]() – высота слоя сорбента (см),
– высота слоя сорбента (см),
![]() – линейная скорость протекания раствора (см/с).
– линейная скорость протекания раствора (см/с).
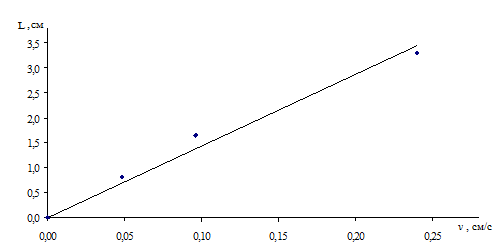
Рис. 3. Зависимость длины сорбционного слоя СКН от скорости протекания раствора при появлении проскоковой концентрации фенола
Величина ![]() , равная тангенсу угла наклона прямой (рис. 3), определяет минимальное время контакта раствора, содержащего фенол, с сорбентом, необходимое для протекания полной сорбции фенола, и оно равно
, равная тангенсу угла наклона прямой (рис. 3), определяет минимальное время контакта раствора, содержащего фенол, с сорбентом, необходимое для протекания полной сорбции фенола, и оно равно ![]() .
.
Результаты определения динамической емкости СКН на модельном растворе фенола представлены в табл. 2.
Таблица 2. Концентрация фенола в фильтрате
|
Объем модельного раствора, прошедшего через сорбент, л |
1…32 |
33 |
34 |
35 |
|
Концентрация фенола в фильтрате, мг/л |
н/о |
0,1 |
0,15 |
0,5 |
Как видно из таблицы, взятые для исследования 10 г сорбента поглощают весь фенол, находящийся в 32 л раствора. Динамическая емкость СКН, по данным таблицы, составила 30 мг/г. Так как в природных водах зачастую присутствуют соединения железа [9], было исследовано влияние ионов железа на динамическую емкость сорбента по отношению к фенолу. Экспериментальные результаты представлены в табл. 3.
Таблица 3. Влияние ионов железа на динамическую емкость сорбента фенола
|
Концентрация ионов железа (II) в модельном растворе, мг/л |
0 |
0,3 |
0,6 |
0,9 |
1,2 |
1,5 |
1,7 |
2,0 |
|
Концентрация фенола в фильтрате, мг/л |
н/о |
н/о |
н/о |
н/о |
0,015 |
0,1 |
0,5 |
1,0 |
Результаты таблицы показали, что наличие ионов двухвалентного железа на уровне ПДК и до 0,9 мг/л не влияет на сорбционную емкость сорбента. При концентрации более 1,2 мг/л сразу появляется проскоковая концентрация фенола. Таким образом, в присутствии ионов железа, начиная с концентрации 1,2 мг/л, сорбционная емкость сорбента по фенолу равна нулю. Следовательно, использование данного сорбента для очистки воды от фенола возможно только после очистки воды от ионов железа.
Положительным качеством данного сорбента является то, что он способен подвергаться регенерации. После насыщения фенолом сорбент прокаливают при температуре 180 °C и повторно пропускают раствор, содержащий фенол. Регенерация восстанавливает сорбционную активность СКН на 80%.
Выводы
1. Рассчитана максимальная сорбционная емкость сорбента СКН по фенолу в статических условиях, равная 35,0 мг/г.
2. Определена динамическая емкость энтеросорбента СКН по фенолу, которая равна 30 мг/г.
3. Показано, что при проектировании фильтров очистки воды от фенола необходимо учитывать время контакта исходного раствора с СКН, которое составляет не менее 15 с.
4. Показано, что при очистке питьевой воды от фенола в присутствии соединений железа отравление сорбента происходит при концентрации железа более 1,2 мг/л.
Работа выполнена при поддержке Государственного задания «Наука» 12.14.2012
Рецензенты:
Сечин А.И., д.т.н., профессор, Федеральное агентство по образованию, ФГБОУ ВПО «Национальный исследовательский Томский политехнический университет», г. Томск.
Хан В.А., д.т.н., ведущий научный сотрудник лаборатории оптической локации, Институт оптики атмосферы СО РАН, г. Томск.
Библиографическая ссылка
Юрмазова Т.А., Шиян Л.Н., Тропина Е.А., Войно Д.А. ИЗУЧЕНИЕ ВОЗМОЖНОСТИ ИСПОЛЬЗОВАНИЯ СОРБЕНТА СКН ДЛЯ ОЧИСТКИ ВОДЫ ОТ ФЕНОЛОВ // Современные проблемы науки и образования. 2013. № 6. ;URL: https://science-education.ru/en/article/view?id=11173 (дата обращения: 02.06.2026).



