Введение
Венозный тромбоз – острое заболевание, вызванное свертыванием крови в просвете вены, что приводит к нарушению ее проходимости [3]. По данным [7], ежегодная частота выявления тромбоза глубоких вен нижних конечностей составляет 84 случая на 100 000 населения. Однако суммарное число таких больных и значимость патологии значительно больше, если принять во внимание «скрыто» протекающие и не диагностируемые случаи тромбозов [1,10].
Тромбоз глубоких вен нижних конечностей является одной из наиболее грозных опасностей, с которыми приходится сталкиваться врачу любой специальности в его практике [6]. Согласно [8], на протяжении трех лет после возникновения тромбоза вен посттромбофлебитический синдром обнаруживается у 35-69 % больных, а на протяжении 5-10 лет - в 49-100 % случаев. Спустя несколько лет у большинства таких больных в виду выраженности посттромботических расстройств гемодинамики в конечности развиваются отек голени, трофические язвы, ведущие к инвалидизации пациентов [6,9].
В связи с этим для улучшения клинических результатов необходимо более полное и глубокое исследование патогенетических механизмов нарушений гомеостаза при остром тромбофлебите, что позволит выработать новые медицинские технологии в лечении этих заболеваний.
В анализируемой литературе мы не встретили работ, в которых бы изучались важнейшие биохимические показатели (перекисное окисление липидов, общая и эффективная концентрация альбуминов, активность SH - групп крови и др.) при тромбофлебите глубоких вен нижних конечностей у женщин.
Цель работы: исследовать интенсивность реакций перекисного окисления липидов, антиоксидантной системы и связывающей способности альбумина при тромбофлебите глубоких вен нижних конечностей у женщин до- и после лечения.
Материалы и методы исследования. Под нашим наблюдением находилось 35 женщин с острым тромбофлебитом глубоких вен нижних конечностей (основная группа). Группу сравнения составили 30 здоровых женщин. По возрасту, обследованные пациентки были сопоставимы, в среднем он составил 44,7 ± 3,4 года.
Все пациентки основной группы получали противовоспалительную, антикоагулянтную, дезагрегантную терапию и препараты, улучшающие микроциркуляцию.
Интенсивность реакций ПОЛ определяли по накоплению малонового диальдегида (МДА) плазмы и эритроцитов (Колясова О.Е., Маркина А.А., Федорова Т.Н., 1984). Об антиоксидантной активности крови судили по уровню в ней каталазы (Бурлакова Е.Б., Архипова Г.В., Голощапов А.Н., 1982). Гидрофобный компонент эндогенной интоксикации (ЭИ) оценивали, определяя общую и эффективную концентрацию альбумина (ОКА и ЭКА) флуоресцентным методом на анализаторе АКЛ-01 с помощью набора реактивов «Зонд – альбумин». Рассчитывали индекс токсичности (ИТ) по формуле: ИТ = (ОКА/ЭКА) – 1 и резерв связывания альбумина (РСА) по формуле: РСА = ЭКА/ОКА [2]. Оценивали содержание общих и свободных SH-групп по методу В.Ф. Фаломеева (1981). Рассчитывали индекс детоксикации (ИДТ) по формуле: ИДТ = SHсвободные/SHобщие; коэффициент МДАпл/КА, который свидетельствует о сдвиге реакции ПОЛ в прооксидантную или антиоксидантную сторону. Рассчитывали модифицированный лейкоцитарный индекс интоксикации (ЛИИм) по В.К. Островскому с соавт. (1983) по формуле: ЛИИм = мц. + пл.кл. + ю. + п. +с./лимф. +мон. + э. + б. [4].
Повторные обследования проводили на 3 и 8 сутки лечения.
Статистическую обработку результатов выполняли на персональном компьютере по программе МЕДСТАТ (В.Л. Акимов). Вычисляли среднюю арифметическую (М) и стандартную ошибку средней арифметической (m). Для оценки критической достоверности различий сравниваемых средних величин применяли критерий Стьюдента. Различия признавались статистически достоверными при Р < 0,05.
Корреляционный анализ параметрических данных проводился по методу Пирсона с использованием программы «Microsoft Excel» и таблицы минимальных значений коэффициентов корреляции Пирсона. При ±1>r>±0,7 отмечалась сильная, при ±0,69>r>±0,3 - средняя, при ±0,29>r>±0 - слабая прямая или обратная корреляционная связь.
Результаты исследований. Клинически эндогенная интоксикация проявлялась повышением температуры, слабостью, недомоганием. Одновременно с этим происходило увеличение лейкоцитарного индекса интоксикации (ЛИИм) по В.К. Островскому на 66,7% относительно группы сравнения (норма – 2,0±0,01 у.е.).
При исследовании показателей ПОЛ – АОС до начала лечения было установлено повышение содержания МДА плазмы и эритроцитов до 10,60±0,21 мкмоль/л и 37,97±3,00 мкмоль/л, т.е. на 61,3% (p<0,01) и на 28,% (p<0,05) выше, чем у здоровых женщин (табл. 1).
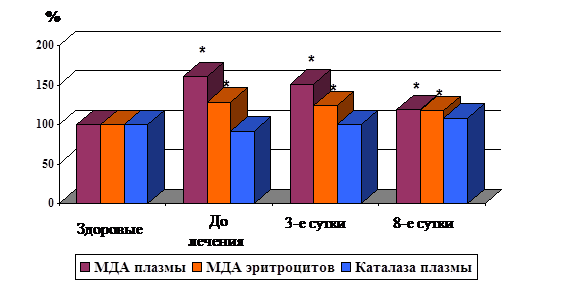
Рис. 1. Динамика МДА плазмы, эритроцитов и каталазы плазмы при остром тромбофлебите
Примечание: * - достоверность показателя по отношению к группе сравнения (p<0,05)
К третьим суткам лечения наметился положительный сдвиг в динамике этих показателей и их снижение на 5,8% и 3,5 % (p1>0,05). К 8 суткам (окончание терапии) произошло достоверное снижение МДА плазмы на 26,0% (p1<0,05), и была отмечена тенденция к уменьшению МДА эритроцитов на 8,5% (p1>0,05). МДА плазмы и эритроцитов по своему значению стал выше показателя в контрольной группе на 9,3% и 17,6% соответственно (p>0,05) (рис. 1).
Каталаза плазмы до лечения имела значение 2,23±0,06 мккат/л и была ниже, чем у здоровых женщин, на 7,2% (p<0,05). К третьим суткам лечения не произошло достоверных изменений в содержании каталазы, а к восьмым суткам уровень этого показателя увеличился на 15,4% (p1<0,05), составил 2,58±0,08 мккат/л и достоверно был выше на 7,1% (p<0,05) величины в группе сравнения.
Отношение МДА/КА до лечения возрастало на 44,6% (p<0,05) и составило 4,80±0,44 у.е., что свидетельствует о сдвиге процессов ПОЛ в прооксидантную сторону, подтверждая роль свободнорадикальных реакций в развитии эндогенной интоксикации при данном заболевании.
Оценивая корреляцию в группе пациенток с острым тромбофлебитом, мы выявили до лечения среднюю обратную корреляционную взаимосвязь между уровнем МДА и каталазы плазмы (r = -0,67) и сильную обратную корреляционную взаимосвязь между этими показателями после лечения (r = -0,72).
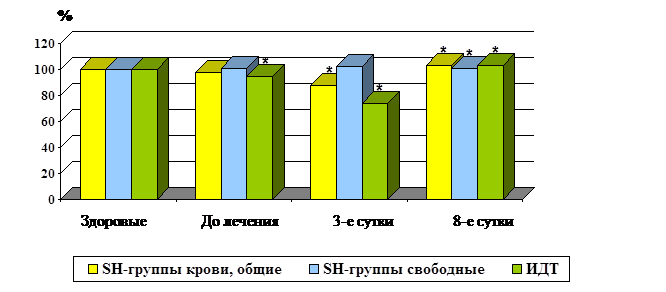
Рис. 2. Динамика концентраций SH-групп при остром тромбофлебите
Примечание: * - достоверность показателя по отношению к группе сравнения (p<0,05)
Исключительно важной функциональной частью АОС является её тиолдисульфидное звено, представленное веществами с небольшой молекулярной массой и разнообразными белками (в том числе ферментами), химические и биологические свойства которых обусловлены присутствием в составе их молекул высокореакционноспособных тиоловых (-SH-) групп. Взаимодействуя с радикалами и перекисями, тиолы окисляются с образованием дисульфитов и могут вновь регенерировать при восстановительном расщеплении дисульфидной (-S-S-) связи, что в определённых условиях обеспечивает возможность сохранения антиоксидантного гомеостаза [5].
Содержание общих и свободных тиолсульфидных групп достоверно не отличалось у здоровых женщин и пациенток, находившихся на стационарном лечении по поводу острого тромбофлебита до начала терапии (табл. 1). К 3 суткам лечения произошло уменьшение общих SH-групп на 10,6% (p1<0,05), а к 8 суткам наблюдалось недостоверное повышение показателя на 5,2% (p1>0,05), и он стал равным соответствующему значению у здоровых женщин, что свидетельствует об усилении антиоксидантной защиты за счет тиосульфидного звена, что, как мы полагаем, привело к снижению МДА плазмы без значимого повышения уровня в ней каталазы (рис. 2).
Оценивая корреляцию в группе пациенток с острым тромбофлебитом, мы выявили до- и после лечения среднюю обратную корреляционную взаимосвязь между уровнем МДА плазмы и SH-групп общих (до лечения r = -0,41; после лечения r = -0,39).
|
Показатель |
Группа сравнения, n=30 |
До лечения |
На фоне лечения |
|
|
3-и сутки лечения |
8-е сутки после лечения |
|||
|
МДА плазмы, мкмоль/л |
6,57±0,31 |
10,60±0,21* |
9,99± 1,02 |
7,84±0,27² |
|
МДА эритроцитов, мкмоль/л |
29,53±1,49 |
37,97±3,00* |
36,63±2,59* |
34,73±3,19 |
|
Каталаза плазмы, мккат/л |
2,41±0,07 |
2,23±0,06* |
2,38±0,08 |
2,58±0,08² |
|
МДА/КА, у.е. |
3,32±0,86 |
4,80±0,44 |
4,30±0,59 |
3,04±0,64 |
|
SH-группы крови общие, ммоль/л |
153,09±3,88 |
149,69±4,60 |
133,85±4,62² |
157,44±3,86 |
|
SH-группы свободные, ммоль/л |
94,60±2,89 |
94,76±2,07 |
96,77±1,76 |
95,34±1,55 |
|
ИДТ |
0,38±0,014 |
0,36±0,015 |
0,28 ±0,012² |
0,39±0,015 |
|
ОКА, % |
60,19±0,46 |
51,92±1,01* |
53,02±0,95 |
59,12±0,99² |
|
ЭКА,% |
39,86±0,37 |
29,76 ±0,87* |
34,31±0,93² |
37,08 ±1,47² |
|
РСА, усл. ед. |
0,66±0,016 |
0,57±0,019* |
0,65±0,018² |
0,63±0,020² |
|
ИТ, усл. ед. |
0,51±0,022 |
0,74±0,012* |
0,55±0,025² |
0,59±0,014² |
Таблица 1. Динамика биохимических показателей при остром тромбофлебите
Примечание: * – достоверность показателя по отношению к группе сравнения; ″ – достоверность показателя по отношению к соответствующему значению до лечения
Концентрация свободных SH-групп имела тенденцию к повышению на 2,1 % (p1>0,05) на третьи сутки лечения, но и по его окончанию значение показателя не отличалось от нормативного. Наибольшие изменения были выявлены при расчете индекса детоксикации. Так, до лечения он был снижен до 0,36±0,015 усл. ед., что оказалось на 5,3% (p<0,05) меньше, чем у здоровых. Спустя 3-е суток на фоне проводимого лечения ИДТ снизился на 22,2% (p1<0,01), а к 8-м суткам повысился на 8,2% (p1>0,05) по сравнению с исходным и достиг нормативного показателя (p>0,05).
Оценивая корреляцию в группе пациенток с острым тромбофлебитом, мы выявили слабую обратную корреляционную взаимосвязь между уровнем МДА плазмы и SH-групп свободных до лечения (r = -0,15) и среднюю обратную после лечения (r = -0,30).
Известно, что течение и исход интоксикаций различного генеза существенным образом зависят от состояния транспортных функций сывороточного альбумина, обеспечивающего перенос различных низкомолекулярных соединений, таких как жирные кислоты, билирубин, некоторые нейтральные жиры, углеводы, лекарственные вещества, ионы металлов, гормоны и другие биологически активные вещества. Транспортная функция альбумина снижается при нарушении синтеза альбумина, когда его становится меньше, или при изменении его структуры [2].
Результаты исследования детоксикационных свойств альбумина у данной группы пациенток (табл. 1) выявили снижение показателей ОКА на 13,7% (p<0,05), а ЭКА на 25,3% (p<0,01) относительно значений в группе сравнения. РСА, таким образом, был ниже на 13,6% (p<0,05). В сравнении с ИТ у здоровых женщин, ИТ в данной группе пациенток вырос на 45,1% (p<0,01).
В процессе лечения, согласно с исследуемым сроком, происходили значительные изменения в показателях эндогенной интоксикации. ОКА начала повышаться: к третьим суткам лечения незначительно, а к 8-м – на 13,9% (p1<0,05) по сравнению с исходным показателем. Ее уровень составил 59,12±0,99%, что практически не отличалось от показателя группы сравнения. Повышение ЭКА оказалось более значимым. На третьи сутки лечения значение показателя стало 34,31±0,93%, а на 8-е, продолжая повышаться - 37,08±1,47%, что было выше исходного показателя на 15,3% (p1<0,05) и 24,6% (p1<0,05) соответственно и по сравнению с показателем у здоровых женщин ЭКА практически не отличалась.
Динамика эффективной концентрации альбумина способствовала повышению резерва связывания альбумина на 14,0% (p1<0,05) к третьим суткам терапии и на 10,5% (p1<0,05) к восьмым. Значение РСА в эти сроки составляло 0,65±0,018 усл.ед. и 0,63±0,020 усл. ед., оставаясь на уровне контрольного показателя. С увеличением уровня ЭКА было связано снижение индекса токсичности при лечении острого тромбофлебита. К третьим суткам произошло уменьшение показателя на 27,0% (p1<0,01) и ИТ составил 0,55±0,025 усл.ед. К восьмым суткам ИТ снизился на 50,3% (p1<0,01) от исходного уровня, достигнув значения 0,59±0,014 усл.ед. Несмотря на значительные положительные сдвиги, ИТ в группе пациенток с острым тромбофлебитом был больше, чем у здоровых женщин, на 15,7% (p<0,05).
Оценивая корреляцию в группе пациенток с острым тромбофлебитом, мы выявили до- и после лечения среднюю обратную корреляционную взаимосвязь между уровнем МДА плазмы и ОКА (до лечения r = -0,49; после лечения r = -0,44); среднюю обратную – между ИДТ и ИТ до лечения (r = -0,57) и сильную обратную после лечения (r = -0,93).
Таким образом, проведенное лечение, направленное на коррекцию воспалительной реакции стенок сосудов и нормализацию микроциркуляции в них, способствовало уменьшению продукции эндогенных токсических субстанций и снижению лабораторных показателей метаболических нарушений при остром тромбофлебите.
Рецензенты:
Плотникова Н.А., д.м.н., профессор, заведующий кафедрой патологии с курсом патологической физиологии медицинский институт ФГБОУ ВПО «Мордовский государственный университет им. Н. П. Огарева», г. Саранск.
Бякин С.П., д.м.н., профессор кафедры госпитальной хирургии медицинского института ФГБОУ ВПО «Мордовский государственный университет им. Н. П. Огарева», г. Саранск.



