Создание оригинальных отечественных препаратов так называемого полного цикла производства - от субстанции до лекарственной формы, является актуальной и приоритетной задачей российской фармации в современных условиях. Особое внимание следует уделять расширению номенклатуры детских лекарственных средств, обладающих интерферон-индуцирующей активностью. Одним из представителей данной группы препаратов является Циклоферон, который широко применяется как средство неспецифической профилактики острых респираторных заболеваний и гриппа у детей во время сезонного подъема заболеваемости [2; 4].
С целью устранения негативных факторов при приеме таблетированной формы и повышения комплаентности к приему лекарства у детей, сотрудниками фармацевтического факультета ОмГМУ была разработана корригированная лекарственная форма – сироп, содержащий в качестве действующего вещества субстанцию циклоферона [3].
На следующем этапе необходимо провести исследование по нормированию показателей подлинности, чистоты и количественного содержания циклоферона в составе лекарственного сиропа.
Целью данной статьи является представление результатов исследования по разработке валидированных методик определения подлинности и доброкачественности циклоферона в составе лекарственного сиропа.
Материалы и методы исследования
Определение подлинности состава лекарственной формы проводили спектрофотометрически на приборе UNICO 2802S (UNICO, США). Оптическую плотность измеряли в интервале длин волн от 200 до 500 нм в кювете с толщиной слоя 1 см. В качестве раствора сравнения использовали 0,1 М раствор натрия гидроксида.
Для определения подлинности циклоферона был приготовлен раствор А: 0,028 г препарата в 100 мл 0,1 М раствора натрия гидроксида и проведены разведения от 0,0056 до 0,00028%.
При разработке методики количественного определения меглумина акридонацетата в сиропе руководствовались методиками его количественного определения в пересчете на акридонуксусную кислоту, приведенными в нормативных документах [6-8].
Методика. Около 4,0 г препарата (точная навеска) помещают в мерную колбу вместимостью 25 мл, растворяют в 0,1 М растворе натрия гидроксида, доводят тем же растворителем до метки, перемешивают. 1 мл полученного раствора переносят в мерную колбу вместимостью 250 мл и доводят объем раствора до метки 0,1 М раствором натрия гидроксида. Измеряют оптическую плотность раствора в максимуме поглощения при 409 нм в кювете с толщиной слоя 1 см. Одновременно измеряют оптическую плотность раствора рабочего стандартного образца (РСО) акридонуксусной кислоты. Раствор сравнения - 0,1 М раствор натрия гидроксида.
Приготовление раствора РСО. Около 0,05 г (точная навеска) акридонуксусной кислоты помещают в мерную колбу на 50 мл и доводят объем до метки 0,1 М раствором натрия гидроксида. 1 мл полученного раствора переносят в колбу вместимостью 50 мл и доводят объем до метки 0,1 М раствором натрия гидроксида.
Содержание акридонуксусной кислоты (Х) в мг в 1 мл препарата вычисляют по формуле (1), а содержание акридонуксусной кислоты (Х) в г в 100 г препарата вычисляют по формуле (2):
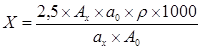 (1) ,
(1) ,
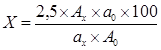 (2),
(2),
где Ах – значение оптической плотности испытуемого раствора,
А0 – значение оптической плотности раствора акридонуксусной кислоты,
ах – точная навеска препарата, взятая для испытания в граммах,
а0 - точная навеска акридонуксусной кислоты в граммах,
ρ – плотность сиропа (1,34 г/мл),
2,5 – разведение испытуемого препарата.
Результаты и их обсуждение
В таблице 1 приведены результаты спектрофотометрического определения подлинности циклоферона в лекарственной форме с учетом проведенных разведений.
Таблица 1
Зависимость значений оптической плотности растворов лекарственной формы от разведения
|
Разведения |
Концентрация растворов,% |
Максимумы (длина волны - значение оптической плотности) |
|
|
референтные пики |
нереферентные пики |
||
|
0,028 г в 100 мл (раствор А) |
0,02800 |
- |
- |
|
5 мл раствора А в 25 мл |
0,00560 |
392 нм – 1,0589 409 нм – 1,0488 |
- |
|
4 мл раствора А в 25 мл |
0,00448 |
392 нм – 0,7844 409 нм – 0,7795 |
251 нм – 2,5202 253 нм – 2,5157 |
|
3 мл раствора А в 25 мл |
0,00336 |
392 нм – 0,6068 409 нм – 0,6024 |
251 нм – 2,4492 253 нм – 2,4557 |
|
2 мл раствора А в 25 мл |
0,00224 |
392 нм – 0,3866 409 нм – 0,3846 |
257 нм – 2,1903 |
|
1 мл раствора А в 25 мл |
0,00112 |
392 нм – 0,1876 409 нм – 0,1875 |
257 нм – 1,2730 |
|
0,5 мл раствора А в 25 мл |
0,00056 |
391 нм – 0,1382 408 нм – 0,1342 |
257 нм – 0,7765 |
|
0,25 мл раствора А в 25 мл |
0,00028 |
391 нм – 0,0793 408 нм – 0,0758 |
257 нм – 0,3472 |
На рис. 1 приведены спектры в УФ-видимой области растворов лекарственной формы.
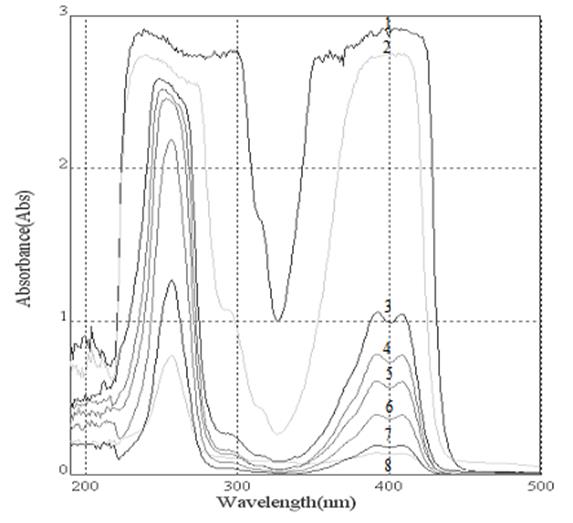
Рис. 1. Электронные спектры поглощения растворов меглумина акридонацетата: 1 - 0,028% раствор; 2 - 0,0056% раствор; 3 - 0,00448% раствор; 4 - 0,00336% раствор; 5 - 0,00224% раствор; 6 - 0,00112% раствор; 7 - 0,00056% раствор; 8 - 0,00028% раствор
На основании результатов определения подлинности были выявлены максимумы поглощения циклоферона в сиропе в области от 200 до 500 нм, при этом значения длин волн максимумов нереферентных пиков не постоянны, в связи с чем было предложено проводить количественное определение на длине волны максимума 409 нм.
Важнейшим критерием оценки аналитической методики служит доказательство ее валидности, включающей взаимосвязанную систему характеристик – линейность, прецизионность (воспроизводимость) и точность [1; 5]. В связи с чем предложенная методика количественного определения меглумина акридонацетата была валидирована по указанным показателям.
Линейность и аналитическая область методики была подтверждена анализом 7 проб разных концентраций в диапазоне от 70 до 130% от концентрации, принятой за 100%. Для обоснования линейной зависимости предлагаемой методики строили градуировочный график зависимости оптической плотности растворов от концентрации, рассчитывали уравнение регрессии и коэффициент корреляции. Графическая зависимость проведенных исследований отражена на рис. 2. По оси абсцисс (Х) – концентрация, г/мл; по оси ординат (Y) – оптическая плотность.
![]()
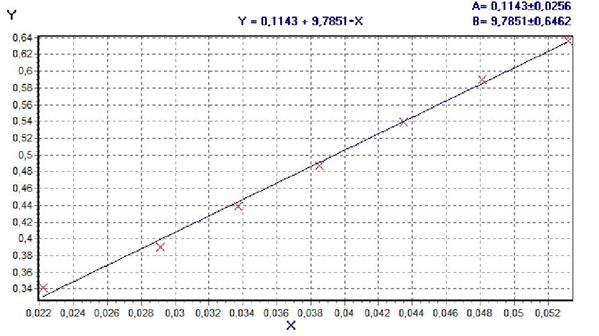
Рис. 2. Градуировочный график зависимости оптической плотности от содержания меглумина акридонацетата в лекарственной форме
Установлено, что в заданной области концентраций меглумина акридонацетата в лекарственной форме график имеет линейный характер и описывается уравнением Y=9,7851·Х+0,1143. Коэффициент корреляции (r) равен 0,998, что позволяет использовать предложенную методику для количественного определения меглумина акридонацетата в сиропе в данном диапазоне концентраций.
Для установления прецизионности (воспроизводимости) проводили 6 параллельных определений, затем вычисляли величину стандартного отклонения (SD) и относительного стандартного отклонения (RSD). Результаты определения воспроизводимости методики количественного определения меглумина акридонацетата в исследуемом сиропе приведены в табл. 2.
Таблица 2
Результаты определения воспроизводимости методики количественного определения меглумина акридонацетата в сиропе
|
Навеска сиропа, г
|
Оптическая плотность |
Найдено циклоферона, г/100 г сиропа |
Метрологические характеристики (Р=0,95) |
|
3,9751 |
0,3419 |
2,2201 |
‾Х=2,2284 SD=0,0089 Δх=0,0093 RSD=0,40% |
|
3,9850 |
0,3435 |
2,2211 |
|
|
3,9945 |
0,3468 |
2,2273 |
|
|
4,0031 |
0,3480 |
2,2407 |
|
|
3,9980 |
0,3465 |
2,2268 |
|
|
4,0005 |
0,3469 |
2,2347 |
Согласно полученным данным величина относительного стандартного отклонения в предложенной методике составляет менее 5%, что характеризует надежность анализа в выбранных условиях [1].
Определение правильности проводили на трех уровнях концентраций анализируемого вещества (80, 100, 120%). Оценка проводилась путем сравнения полученного результата с ожидаемым значением. В результате получены 9 значений открываемости (R), для которых вычисляли величину стандартного отклонения (SD) и относительного стандартного отклонения (RSD). Данные, полученные при изучении правильности спектрофотометрической методики определения меглумина акридонацетата в сиропе, представлены в табл. 3.
Таблица 3
Метрологические характеристики установления правильности спектрофотометрической методики определения меглумина акридонацетата в сиропе
|
Уровень |
Навеска сиропа, г |
Меглумина акридонацетата в сиропе, г |
Найдено меглумина акридонацетата в сиропе, г |
R, % |
Метрологические характеристики (Р=0,95) |
|
1 |
3,0889 |
0,0695 |
0,0682 |
98,13 |
R=98,73% SD=0,4359 Δх=0,34 RSD=0,44% |
|
1 |
3,1289 |
0,0704 |
0,0697 |
99,01 |
|
|
1 |
3,1067 |
0,0699 |
0,0689 |
98,57 |
|
|
2 |
3,8889 |
0,0875 |
0,0863 |
98,67 |
|
|
2 |
3,8844 |
0,0874 |
0,0868 |
99,31 |
|
|
2 |
3,8399 |
0,0864 |
0,0852 |
98,61 |
|
|
3 |
4,6711 |
0,1051 |
0,1045 |
99,43 |
|
|
3 |
4,6622 |
0,1049 |
0,1033 |
98,47 |
|
|
3 |
4,4578 |
0,1003 |
0,0986 |
98,35 |
Результаты определения правильности методики показали, что теоретические и экспериментальные значения количественного содержания меглумина акридонацетата в сиропе практически полностью совпадают. Величина относительного стандартного отклонения не превышает 5%, а открываемость составляет 98,73%, что характеризует правильность методики как удовлетворительную и согласуется с требованиями нормативной документации [1; 5].
Заключение
На основании проведенных исследований были предложены спектрофотометрические методики определения подлинности и количественного содержания меглумина акридонацетата в составе лекарственной формы. Установлено, что методика количественного определения меглумина акридонацетата в пересчете на акридонуксусную кислоту является точной, линейной и воспроизводимой. Полученные результаты могут быть рекомендованы для установления норм качества сиропа и разработки проекта фармакопейной статьи на лекарственную форму.
Рецензенты:
Гришин А.В., д.фарм.н., профессор, ректор АНО ДПО «Сибирская фармацевтическая академия», г. Омск;
Ливзан М.А., д.м.н., профессор, зав. кафедрой факультетской терапии с курсом профессиональных болезней ГБОУ ВПО «Омский государственный медицинский университет» Минздрава России, г. Омск;
Библиографическая ссылка
Лукша Е.А., Корнеева И.Н., Савченко И.А., Погодин И.С., Иванова Е.В., Володина Т.А., Оздоев М.М. ОПРЕДЕЛЕНИЕ МЕГЛУМИНА АКРИДОНАЦЕТАТА В КОРРИГИРОВАННОЙ ЛЕКАРСТВЕННОЙ ФОРМЕ // Современные проблемы науки и образования. 2015. № 2-2. ;URL: https://science-education.ru/ru/article/view?id=21793 (дата обращения: 01.03.2026).



