Дубильные вещества находят широкое применение в фармации, они обладают вяжущим, противовоспалительным, бактерицидным и кровоостанавливающимдействием, которое основано на способности связываться с белками с образованием плотныхальбуминатов. Кроме того они способны образовывать осадки с алкалоидами, сердечными гликозидами, солями тяжелых металлов что позволяет использовать их в качестве антидотов при отравлении этими веществами. В медицине дубильные вещества применяются в терапии таких заболеваний как стоматиты, гингивиты, фарингиты, ангины, колиты, энтероколиты, дизентерии, применяют их и при ожогах, маточных, желудочных и геморроидальных кровотечениях. Широта медицинского применения делает эту группу биологически активных веществ интересной для поиска и изучения новых источников сырья содержащего дубильные вещества.[5,6]
Экспериментальная часть
Объектом нашего исследования являлась трава горца сахалинскогоинтродуцированного в условиях Кавказских Минеральных Вод и собранного в разные фенологические фазы (бутонизации, цветения и плодоношения).
Горец (рейноутрия) сахалинский-Polygonumsachalinense(ReynoutriasachalinensisF.Schmidt(Nakai) многолетнее травянистое растение, достигающее высоты 3 м. Подземные органы представлены ползучим корневищем с тонкими шнуровидными придаточными корнями, от которого отходят многочисленные прямые, полые, прочные стебли, зеленого или бурого цвета. Листья яйцевидно-сердцевидные, широкоовальные или овально-продолговатые, на коротких черешках, длиной до 20 см. Цветки мелкие, многочисленные, беловато - кремовые, собранные в короткие пазушные метельчатые соцветия. Околоцветник воронковидный, при плодах сильно разрастающийся и скрывающий плод. Плод - трёхгранный темно-бурый блестящий орешек. Цветет этот вид в августе-сентябре.[3]
По качественному составу дубильные вещества горца сахалинского в большей степениконденсированные (черно-зеленое окрашивание с железоаммониевыми квасцами), но также присутствуют производные пирогаллола[1].Для количественного определения дубильных веществ в растении мы использовали титриметрический (перманганатометрия) и УФ-спектрофотометрический методы[4]. Методика перманганатометрического титрования применялась в двух модификациях:
- перманганатометрический метод Левенталя в модификации А.Л.Курсанова;
- перманганатометрический методЛевенталя в модификации А.Л.Курсанова, в сочетании с осаждением дубильных веществ желатином;
- спектрофотометрический метод.
Перманганатометрический метод Левенталя в модификации А.Л.Курсанова является фармакопейными и основан на способности дубильных веществ быстро окисляться перманганатом калия.
Для проведения анализа готовили 3 извлечения из сырья горца сахалинского собранного в фазы бутонизации, массового цветения и плодоношения.Около 1 г (точная навеска) измельченного сырья горца сахалинского, просеянного сквозь сито с диаметром отверстий 3 мм, заливали 100 мл кипящей воды и нагревали на водяной бане в течение 30 минут при частом перемешивании.Затем в течение 30 минут извлечение отстаивали при комнатной температуре и фильтровали через бумажный складчатый фильтр в колбу емкостью 100мл и доводили водой до метки. 10 мл извлечения помещали в коническую колбу вместимостью 1 л, добавляли 750 мл воды и 25 мл раствора индигосульфокислоты и титровали при постоянном перемешивании 0,1 н. перманганатом калия до золотисто-желтого окрашивания.Количественное содержание вычисляли по формуле 1:
X =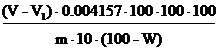 (1)
(1)
где,V – объем раствора калия перманганата (0,02 моль/л), израсходованное на титрование извлечения, в мл;V1 – объем раствора калия перманганата (0,02 моль/л), израсходованное на титрование в контрольном опыте, в мл; m – навеска сырья, г; 0.004157 – количество дубильных веществ, соответствующих 1 мл раствора калия перманганата (0,02 моль/л) (в пересчете на танин), в г;W – потеря в массе при высушивании сырья, в %. [2]
Однако, перманганатометрический метод не совсем точный т.к. окислению поддаются не только дубильные вещества, но и другие полифенольные соединения. Для вычисления количества других окисляющихся веществ использовали осаждение дубильных веществ желатином. Для этого 20 мл извлечения осаждали 1% раствором желатина в 10% растворе натрия хлорида. Образовавшийся осадок отфильтровывали, а 10 мл фильтрата подвергали титрованию аналогично описанной выше методике. Расчет проводили по формуле 1, где V- объем раствора калия перманганата (0,02 моль/л), израсходованное на титрование извлечения после осаждения. Содержание дубильных веществ (Х) рассчитывали по формуле 2:
![]() (2)
(2)
Где Х1 – общее содержание веществ, окисляющихся при титровании раствором калия перманганата; Х2 – содержание других окисляющихся веществ.
Спектрофотометрическое определение дубильных веществ.
5 мл из полученного извлечения помещали в мерную колбу вместимостью 50 мл, доводили его до метки спиртом этиловым 70%, затем 2,5 мл полученного раствора помещали в мерную колбу на 25 мл и доводили его до метки спиртом этиловым 70%. Измеряли оптическую плотность полученного раствора на спектрофотометре СФ-101 в кювете с толщиной слоя 10 мм при длине волны 275нм относительно спирта этилового 70%. Параллельно определяли оптическую плотность раствора стандартного образца танина.
Приготовление раствора стандартного образца танина.Около 0,0025г (точная навеска) стандартного образца танина, высушенного до постоянной массы при температуре 100-105˚С, помещали в мерную колбу вместимостью 50 мли растворяли его при постоянном перемешивании, в 50 мл спирта этилового 70%, добавляя его порциями по 25 мл. 2,5 мл полученного раствора помещали в мерную колбу на 25 мл и доводили до метки спиртом этиловым 70%.[5]
Суммарное содержание дубильных веществ в пересчете на воздушно-сухое сырье (X,%) определяли по формуле3
![]() (3)
(3)
где Mcm– масса ГСОтанина, г;Mx – масса сырья, г;Dcm – оптическая плотность ГСОтанина;Dx – оптическая плотность исследуемого раствора.
Результаты исследования представлены в таблице 1.
Таблица 1
Содержание дубильных веществ в траве горца сахалинского, в зависимости от фенологической фазы
|
Метод |
Фаза |
Содержание в % |
|
Перманганатометрический |
Фаза бутонизации |
13,8±0,15 |
|
Фаза массового цветения |
17,1±0,15 |
|
|
Фаза плодоношения |
17,33±0,16 |
|
|
Перманганатометрический в сочетании с осаждением желатином |
Фаза бутонизации |
10,3±0,27 |
|
Фаза массового цветения |
11,18±0,22 |
|
|
Фаза плодоношения |
12,27±0,32 |
|
|
Спектрофотометрический |
Фаза бутонизации |
3,67±0,108 |
|
Фаза массового цветения |
4,45±0,11 |
|
|
Фаза плодоношения |
5,08±0,16 |
Исходя из данных таблицы все 3 метода показали максимальное содержание дубильных веществ в траве горца сахалинского в фазу плодоношения.
Выводы
Таким образом, с помощью различных аналитических методов нами было определенно содержание дубильных веществ в траве горца сахалинского в разные фенологические фазы, и установлено что максимальное накопление данной группы веществ в траве горца сахалинского происходит в фазу плодоношения.
Исходя из результатов исследования, для анализа дубильных веществ в траве горца сахалинского оптимальным, на наш взгляд,является метод 2, т.к. позволяет определить обе группы дубильных веществ, в отличие от спектрофотометрического метода, в котором в качестве стандарта мы использовали танин,который по своей структуре относится кгидролизуемым дубильным веществам.
Рецензенты:Андреева И.Н., д.фарм.н., профессор кафедры экономики и организации здравоохранения и фармации, ГБОУ ВПО Пятигорский медико-фармацевтический институт филиал Волгоградского Государственного медицинского университета МЗ РФ, г. Пятигорск;
Мелик-Гусейнов В.В., д.б.н., профессор кафедры фармации Факультета последипломного образования, ГБОУ ВПО Пятигорский медико-фармацевтический институт филиал Волгоградского Государственного медицинского университета МЗ РФ, г. Пятигорск.



