Исследование липофильных свойств биологически активных веществ играет важную роль в изучении связи структура – активность [5]. Липофильность влияет на проникновение биологически активных веществ через клеточные мембраны и является одним из ключевых детерминантов фармакокинетических свойств, значения которого позволяют предсказывать биологическую активность веществ. Характеристика распределения органических веществ в двухфазной системе октанол/вода – липофильность (log P) является физико-химическим параметром, который характеризует способность транспорта лекарственных веществ через клеточные мембраны [6, 8], определяя их абсорбцию и распределение в различных системах организма [3].
Цель данной работы заключается в установлении количественной зависимости между экспериментально определенными константами липофильности (logPэксп) и величиной противовоспалительной активности (ПВА). Объектом исследования являются производные антраниловой кислоты, при атоме азота которых содержатся ацильные или бензильный заместители, под общим названием N–арилзамещенные производные антраниловой кислоты (7 соединений).
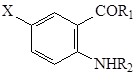
X=H, R1=OH, R2= CH2C6H5 (I); X=Br, R1=NH2, R2= COC6H4 (2-COOH) (II); X= I, R1= NHCH2C6H5, R2= COCH2C6H5 (III); X= I, R1= NHCH2CH2OH, R2= COCH2C6H5 (IV); X=I, R1= NHCH2CH2OH, R2= COC6H5 (V); X=I, R1= NHCH3, R2= COC6H5 (VI); X=I, R1= NHCH2CH2OH, R2= CO(2-фурил) (VII).
Для изучения количественной зависимости фармакологического действия от физико-химических свойств соединений экспериментально определены величины коэффициента распределения октанол–вода (log Pэксп) спектрофотометрическим методом [4, 7]. Полученные результаты и их метрологические характеристики (S – стандартное отклонение среднего результата, ±∆ logP средний и ![]() – значение относительной погрешности среднего результата при уровне значимости (α=0,05)) для 7 соединений этого ряда (I – VII), приведены в таблице 1. Значения log Pэксп лежат в интервале от 1,81 до 2,85.
– значение относительной погрешности среднего результата при уровне значимости (α=0,05)) для 7 соединений этого ряда (I – VII), приведены в таблице 1. Значения log Pэксп лежат в интервале от 1,81 до 2,85.
Для исследования связи структура – противовоспалительная активность использовали значения ПВАэксп (%) определенные через 4 часа, а для соединений ПВАэксп которых определено через 3 и 5 часов, среднее значение (таблица 1).
Таблица 1
Противовоспалительная активность и константы липофильности N– арилзамещенных производных антраниловой кислоты (I – VII)
|
Соединение |
Метрологические характеристики logPэксп |
ПВАэксп, % |
|||
|
logPэксп средний |
S |
±∆ logPэксп средний |
|
||
|
I |
2,46 |
0,0208 |
0,09 |
2,10 |
13,50 |
|
II |
1,81 |
0,0291 |
0,13 |
3,98 |
59,95 |
|
III |
2,85 |
0,0361 |
0,16 |
3,14 |
12,90 |
|
IV |
2,45 |
0,0120 |
0,05 |
1,22 |
11,50 |
|
V |
2,78 |
0,0273 |
0,12 |
2,44 |
21,30 |
|
VI |
2,68 |
0,0233 |
0,10 |
2,16 |
32,70 |
|
VII |
2,60 |
0,0219 |
0,09 |
2,09 |
25,10 |
С целью установления корреляционной зависимости между константой липофильности и ПВАэксп был проведен регрессионный анализ с использованием программы Statistica 6. В результате составлены три уравнения линейной, логарифмической и полиномиальной регрессии (таблица 2). На основании вычисленного значения р (при α=0,05) и критериев Фишера и Стьюдента значимыми являются уравнения 1 и 2.
Таблица 2
Корреляционные уравнения взаимосвязи констант липофильности с ПВАэксп
|
№ |
Корреляционное уравнение |
N |
R |
F |
t |
р |
|
1 |
ПВАэксп = 119,204 – 37,293 × logP |
7 |
0,755 |
6,67 |
3,25 |
0,049 |
|
2 |
ПВАэксп = 105,521 – 202,064 × log (logP) |
7 |
0,783 |
7,93 |
3,65 |
0,037 |
|
3 |
ПВАэксп = 460,797 – 340,994 × log P + + 65,666 × log P2 |
7 |
0,866 |
6,00 |
2,25 |
0,062 |
Для того чтобы проверить прогнозирующую способность составленных регрессионных уравнений, определены значения logPэксп трёх новых соединений из ряда N- арилзамещенных производных антраниловой кислоты (VIII – X) (таблица 3), которые были использованы для расчёта ПВА с помощью уравнений 1 и 2.
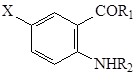
X=Br, R1=NH2, R2= COC6H5 (VIII); X=Br, R1=NH2, R2= COC6H4(4-NO2) (IX); X=H, R1=OH, R2= COC6H4(2, 4–Cl2) (X).
Таблица 3
Константы липофильности N-арилзамещенных производных антраниловой кислоты
(VIII – X)
|
Соединение |
Метрологические характеристики logPэксп |
|||
|
logPэксп средний |
S |
±∆ logPэксп средний |
|
|
|
VIII |
2,09 |
0,0176 |
0,08 |
2,09 |
|
IX |
1,56 |
0,0273 |
0,12 |
4,34 |
|
X |
2,07 |
0,0219 |
0,09 |
2,63 |
Полученные результаты ПВАрассч и доверительные интервалы среднего предсказанного значения (Δ ПВАрассч) приведены в таблице 4. Доверительный интервал среднего предсказанного значения рассчитывали по формуле 1 [1]:
Δ ПВАрассч = t0,05 (n-k) × S × 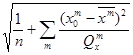 (1)
(1)
где, t0,05 – коэффициент Стьюдента при уровне значимости (α=0,05);
n – число наблюдений в уравнении (n=7);
k – число оцениваемых параметров регрессионной модели (k=2);
m – независимая переменная, используемая в уравнении регрессии (logP);
S – среднее квадратичное отклонение ошибок наблюдений;
![]() – значение независимой переменной (log P), используемой в расчётах;
– значение независимой переменной (log P), используемой в расчётах;
![]() – среднее значение независимой переменной (log P), входящей в расчётную модель;
– среднее значение независимой переменной (log P), входящей в расчётную модель;
![]() – сумма квадратов отклонений независимой переменной (log P), используемой в расчётной модели.
– сумма квадратов отклонений независимой переменной (log P), используемой в расчётной модели.
Теоретически рассчитанные величины ПВА соединений (VIII–X) подтверждены экспериментальными данными, которые приведены в таблице 4.
Таблица 4
Теоретически рассчитанные и экспериментальные значения ПВА N-арилзамещенных производных антраниловой кислоты (VIII–X)
|
Соединение |
уравнение 1 |
уравнение 2 |
ПВАэксп, % |
||
|
ПВАрассч |
∆ ПВАрассч |
ПВАрассч |
∆ ПВАрассч |
||
|
VIII |
41,26 |
23,35 – 59,17 |
40,83 |
23,82 – 57,85 |
38,75 |
|
IX |
61,03 |
41,68 – 80,38 |
66,50 |
48,12 – 84,88 |
46,15 |
|
X |
42,01 |
24,04 – 59,97 |
41,67 |
24,61 – 58,74 |
52,20 |
По расчётам процент торможения каррегинового отёка составил свыше 30 %. Экспериментально определенные значения ПВА для соединений VIII–X находятся в интервале 38,75 – 52,20 %.
Таким образом, можно сделать вывод, что рассчитанные уравнения могут быть использованы в дальнейших исследованиях для поиска активных соединений с противовоспалительным действием в ряду N-арилзамещенных производных антраниловой кислоты.
Экспериментальная часть
Экспериментальное определение величин констант липофильности N-арилзамещенных производных антраниловой кислоты проводилось спектрофотометрическим методом в системе октанол – вода [4, 7]. Полученные результаты и их метрологические характеристики (S – стандартное отклонение среднего результата, ±∆ logP средний и ![]() – значение относительной погрешности среднего результата при уровне значимости (α=0,05)) для 10 соединения этого ряда (I–X), приведены в таблицах 1 и 3.
– значение относительной погрешности среднего результата при уровне значимости (α=0,05)) для 10 соединения этого ряда (I–X), приведены в таблицах 1 и 3.
Противовоспалительное действие соединений (I–X) (таблицы 1 и 4) исследовали на белых нелинейных крысах массой 200–220 г на модели каррагенинового отёка. Изучаемые вещества вводили внутрибрюшинно в дозе 50 мг/кг в виде водной суспензии, стабилизированной твином–80, за 1 ч до инъекции флогогена. Крысам контрольной серии вводили эквивалентное количество раствора твина. В качестве препарата сравнения использовали ортофен, который вводили из расчёта 10 мг/кг в условиях, аналогичных описанным для тестируемых соединений. Объем лап животных измеряли онкометрически до и через 3, 4 и 5 ч после инициации воспаления [2]. Эффект оценивали по уменьшению прироста отека лап в сравнении с контрольной группой крыс.
Рецензенты:
Михайловский А. Г., д-р фармац. наук, профессор, зав. кафедрой неорганической химии, ГБОУ ВПО ПГФА Министерства здравоохранения Российской Федерации, г. Пермь.
Ярыгина Татьяна Ивановна, д-р фармац. наук, профессор кафедры фармацевтической химии очного факультета ГБОУ ВПО ПГФА Министерства здравоохранения Российской Федерации, г. Пермь.
Степанова Элеонора Федоровна, д-р фармац. наук, профессор кафедры ГОУ ВПО Пятигорской фармацевтической академии, Росздраватехнологии лекарств, г. Пятигорск.
Библиографическая ссылка
Коркодинова Л.М., Андрюков К.В., Вейхман Г.А., Ендальцева О.С., Визгунова О.Л. КОНСТАНТЫ ЛИПОФИЛЬНОСТИ N–АРИЛЗАМЕЩЕННЫХ ПРОИЗВОДНЫХ АНТРАНИЛОВОЙ КИСЛОТЫ В ИЗУЧЕНИИ СВЯЗИ СТРУКТУРА – ПРОТИВОВОСПАЛИТЕЛЬНАЯ АКТИВНОСТЬ // Современные проблемы науки и образования. 2013. № 3. ;URL: https://science-education.ru/ru/article/view?id=9397 (дата обращения: 16.05.2026).



