Введение
Химический состав растений рода Barbarea R. Br. разнообразен, но к настоящему времени изучен недостаточно. Растения данного рода накапливают тритерпеновые сапонины, глюкозинолаты [9, 10], тиогликозиды [2] и флавоноиды [7]. В надземной части растения присутствует значительное количество дериватов феруловой и изоферуловой кислот, а также кофейной кислоты, характерных и для других растений семейства Brassicaceae [8].
Среди перечисленного разнообразия классов природных соединений особо следует выделить группу флавоноидов. В работе [6] указывается на то, что для всех видов сем. Brassicaceae характерно накопление гликозидов кемпферола, кверцетина, лютеолина и апигенина, при этом род Barbarea R. Br. является среди всего семейства одним из исключений, так как одновременно накапливает гликозиды и флавонов, и флавонолов, в то время как для большинства родов данного семейства характерно накопление флавонолов [1, 4].
В связи с тем, что надземная часть данного растения накапливает значительный комплекс биологически активных соединений, следует предположить и наличие существенной фармакологической активности, основанием для этого могут служить работы [3, 5], при этом особый интерес может представлять нефропротекторное действие биологически активных веществ.
Объектом исследования являлась надземная часть двулетнего травянистого растения сурепки дуговидной (с. обыкновенной) – Barbarea arcuata Reichenb.(B. vulgaris auct.) сем. капустных (Brassicaceaea), заготовленная в районе Кавказских Минеральных Вод (Ставропольский край) в период цветения (2010–2012 гг.).
Данный вид из рода Сурепка является наиболее распространенным в дикорастущей флоре и введен в культуру, т.к. имеет сельскохозяйственное значение, что и предопределяет его достаточную ресурсную базу.
В связи со сложностью химического состава данного растения на первом этапе исследований проводили изучение спектра агликонов флавоноидов.
Экспериментальная часть
Для проведения исследования точную навеску сырья (около 1 г) помещали в колбу с обратным холодильником и экстрагировали при умеренном кипении 50 мл смеси спирта этилового 95 % и кислоты хлороводородной, разведенной 7:3 в течение 1 часа. При этом происходит экстракция и гидролиз всех флавоноидов, находящихся в гликозилированной форме, затем извлечение декантировали в мерную колбу вместимостью 50 мл, охлаждали и доводили спиртом этиловым до метки. После перемешивания 2 мл извлечения осторожно упаривали в токе воздуха и растворяли в 2 мл диметилформамида, полученный раствор после центрифугирования использовался для ВЭЖХ анализа.
В работе использовали систему для ВЭЖХ UltiMate 3000 (Dionex), сопряженную с МС детектором AmaZon SL (Bruker), ионизация – электрораспылением. Хроматографирование вели в градиенте от 5 до 60 % ацетонитрила за 40 минут, при скорости потока 0,3 мл/мин, в качестве второго компонента подвижной фазы использовали раствор кислоты муравьиной в воде (2 г/л), для разделения использовали колонку 150×4,6 мм, заполненную обращеннофазным сорбентом с привитыми октадецильными остатками.
Результаты и обсуждение
При этом установлено, что на хроматограмме извлечения из цветков и листьев, полученных с применением детектирования при 360 нм, отмечаются 3 основных пика, которые могут быть отнесены к агликонам флавоноидов, и ряд минорных пиков (рис. 1–2).
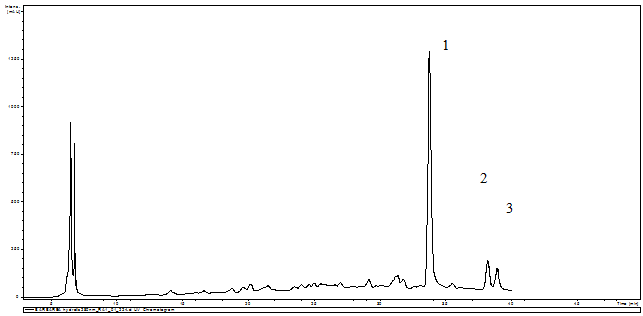
Рис. 1. Хроматограмма суммы биологически активных веществ цветков Barbarea arcuata после кислотного гидролиза, пик 1 – кверцетин, пик 2 – кемпферол, пик 3 – изорамнетин
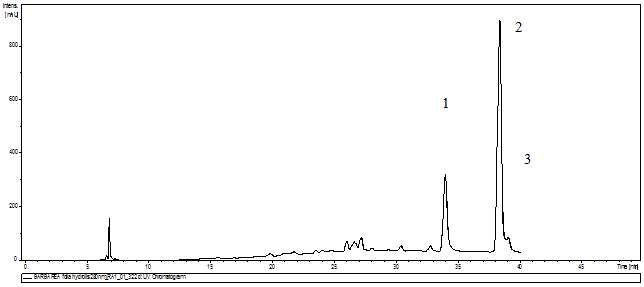
Рис 2. Хроматограмма суммы биологически активных веществ листьев Barbarea arcuata после кислотного гидролиза, пик 1 – кверцетин, пик 2 – кемпферол, пик 3 – изорамнетин
Анализ масс-спектров основных пиков показал наличие ионов с массами (m/z+) 303,2+; 317,1+; 287,2+. При этом основному пику на хроматограмме извлечения из цветков соответствует величина m/z+ равная 303,2, что соответствует флавоноиду с молекулярной массой 302,1 Полученные результаты и анализ литературных данных позволяет предположить наличие в цветках кверцетина в качестве основного агликона, а также изорамнетина (рис. 3, 4).
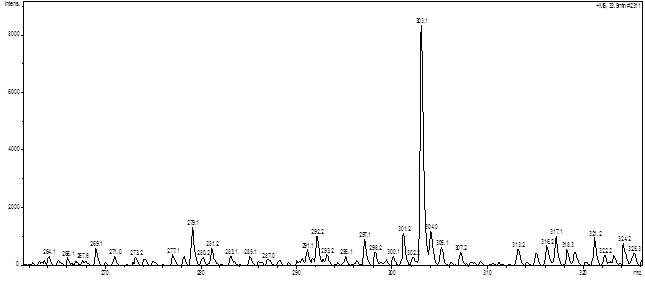
Рис. 3. Фрагмент хромотограммы извеления из листьев Barbarea arcuata с и масс-спектром кверцетина ( m/z+ - 303,1)
а)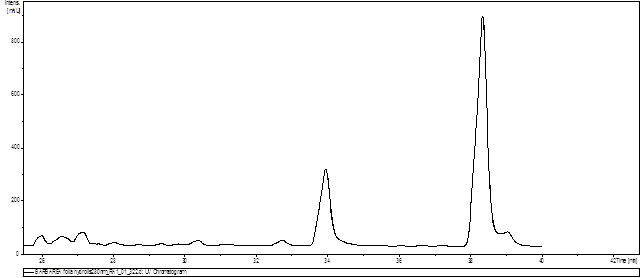
б) 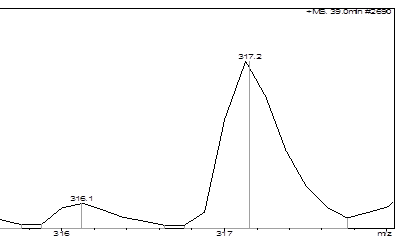
Рис. 4. Фрагмент хроматограммы извлечения из листьев Barbarea arcuata с пиком (A) и масс-спектром (Б) изорамнетина (m/z+ – 317,1)
Сигнал с массовым числом 278,2+ может быть характерен как для кемпферола, так и для лютеолина. В литературе имеются сведения о возможности наличия в данном сырье гликозидов лютеолина [6]. Анализ хроматограмм растворов стандартных образцов, полученных в аналогичных условиях, позволил отнести пик с временем удерживания около 38 минут к кемпферолу (рис. 5). В то же время на хроматограмме имеется минорный пик с временем удерживания около 26 минут, которому соответствует массовое число 278,2+, что может свидетельствовать о наличии лишь следовых количеств лютеолина.
а)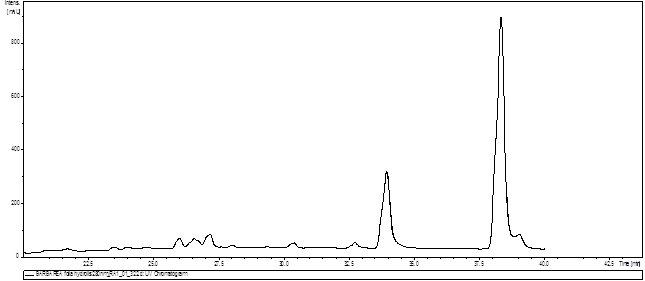
б)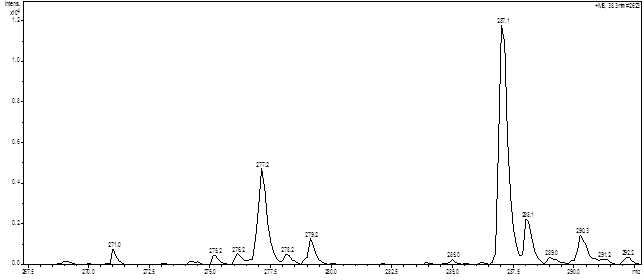
Рис. 5. Фрагмент хроматограммы извлечения из листьев Barbarea arcuata с пиком (A) и масс-спектром (Б) кемпферола (m/z+- 287,1)
Таким образом, проведенные исследования позволили подтвердить присутствие в цветках кверцетина, кемпферола и изорамненина, при этом основным агликоном является кверцетин.
Следующим этапом исследования стало изучение качественного состава агликонов листьев. При этом установлено, что в листьях сурепки дуговидной накапливаются те же агликоны флавоноидов, но превалирующим соединением является кемпферол, при этом изорамнетин находится в минорных количествах. Следует отметить, что в листьях также присутствует лютеолин, но его содержание заметно больше чем в цветках и находится на уровне изорамнетина.
Таким образом, проведенные исследования впервые позволили достоверно идентифицировать агликоны флавоноидов цветков и листьев Barbarea arcuata, произрастающей в районе Кавказских Минеральных Вод. При этом интересным является тот факт, что превалирующим агликоном листьев является кемпферол, а цветков – кверцетин.
Полученные результаты позволяют считать надземную часть Barbarea arcuata перспективным лекарственным растением, способным оказывать диуретическое и нефропротекторное действие.
Рецензенты:
Лазарян Джон Седракович, д.ф.н., профессор, зав. кафедрой токсикологической химии Пятигорского филиала ГБОУ ВПО ВолгГМУ Минздрава России, г. Пятигорск.
Вергейчик Евгений Николаевич, д.ф.н., профессор кафедры фармацевтической химии Пятигорского филиала ГБОУ ВПО ВолгГМУ Минздрава России, г. Пятигорск.
Библиографическая ссылка
Орловская Т.В., Гаврилин М.В., Антюшин А.В. ИДЕНТИФИКАЦИЯ АГЛИКОНОВ ФЛАВОНОИДОВ В ЛИСТЬЯХ И ЦВЕТКАХ СУРЕПКИ ДУГОВИДНОЙ МЕТОДОМ ВЭЖХ/МС // Современные проблемы науки и образования. 2013. № 1. ;URL: https://science-education.ru/ru/article/view?id=8481 (дата обращения: 09.06.2026).



