Введение. Проблеме реакции тканей полости рта на металлические включения посвящено большое количество работ отечественных и зарубежных ученых, однако до настоящего времени ответы на вопросы этиологии, патогенеза, диагностики и предупреждения возникновения непереносимости металлических включений в полости рта неоднозначны [3; 6; 7]. Свести к минимуму вероятность неблагоприятного воздействия металлов на ткани полости рта возможно, применив для изготовления протезов сплавы благородных металлов, которые обладают положительным потенциалом. Наибольшим положительным электродным потенциалом, лучшей биологической совместимостью обладают золото и его сплавы, которые не могут заменить в стоматологии сплавы неблагородных металлов по ряду физических свойств и экономическим причинам. Теоретически обоснованным и технически разработанным решением этой проблемы является применение электролитического золочения элементов протеза, выполненных из сплавов неблагородных металлов [1; 2; 5].
Широкому применению этого метода препятствует недостаточное количество и узкий спектр проведенных исследований, которые носили в большинстве технический характер.
Цель исследования: экспериментальное обоснование применения золотосодержащего покрытия для повышения биологической инертности стоматологических конструкционных сплавов.
Материал и методы исследования. Эксперимент проводили на 18 животных (кроликах), которых разделили на 3 группы. Во время проведения эксперимента животных содержали в виварии на одинаковом пищевом рационе и в идентичных условиях. Каждой группе кроликов вводили под кожу металлические пластинки размером 10-5-1 мм.
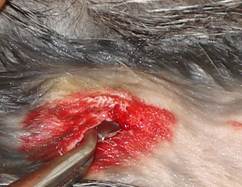
Рис. 1. Подкожное введение в первой группе животных пластины из кобальто-хромового сплава RemaniumStar (Dentfurum).
В первой группе животным вводили пластинки из кобальто-хромового сплава RemaniumStar (Dentfurum), во второй группе – пластинки из золотого сплава «Супер-ТЗ» (НПК «Суперметалл»), в третьей группе – пластинки из кобальто-хромового сплава RemaniumStar (Dentfurum) с золото-циркониевым покрытием «Кэмадент» (НПК «Суперметалл»).
Пластинки вводили под инфильтрационной анестезией Sol. Lidocaine 4%-2ml. Пластинки удаляли через 3, 7, 14, 21 и 30 суток. Для гистологического исследования брали фрагменты кожи из подкожных тканей экспериментальных животных.
Результаты исследования
Патогистологические изменения в тканях лабораторных животных после вживления пластинки из кобальто-хромового сплава. Через трое суток от начала эксперимента в дерме обнаружена полость прямоугольной формы. Края полости (раны) неровные, покрыты неравномерным слоем некротических масс с большим количеством нейтрофильных лейкоцитов, гемолизированных эритроцитов. Среди некротических масс определяются глыбки бурого пигмента.
В окружающих тканях отмечается отек, сосудистые нарушения в виде полнокровия, стазов, обширных кровоизлияний. Коллагеновые волокна набухшие, гомогенизированы, склеены между собой с признаками некробиоза и некроза. Отмечается отек и диффузная инфильтрация дермы полиморфноядерными лейкоцитами с примесью макрофагов. Лейкоцитарная инфильтрация распространяется на всю толщину дермы и переходит на подкожно-жировую клетчатку.
Через 7 суток после начала эксперимента наблюдается частичное рассасывание некротических масс и неполное очищение краев раны. На поверхности раны сохраняется четко очерченная полоса из гомогенных эозинофильных масс, представленных некротизированными коллагеновыми волокнами. Сохраняется перифокальная воспалительная реакция в виде отека, гиперемии и инфильтрации полиморфно ядерными лейкоцитами. По сравнению с 3-ми сутками интенсивность отека несколько понижается. В инфильтрате уменьшается количество нейтральных лейкоцитов и увеличивается число лимфоцитов и плазматических клеток.
Через 14 суток в краях раны определяются фокусы формирующейся грануляционной ткани, богатой сосудами капиллярного типа и клеточными элементами. Между капиллярами располагаются многочисленные клеточные элементы: фибробласты, фиброциты, лимфоциты, плазматические клетки, макрофаги. На поверхности грануляционной ткани определяется тонкая полоска тканевого детрита. В толще грануляционной ткани отмечается диффузная воспалительная инфильтрация полиморфно ядерными лейкоцитами с примесью макрофагов.
В окружающих тканях отмечается значительное уменьшение отека, сосудистая реакция полностью купируется, наблюдается умеренная воспалительная реакция с преобладанием в инфильтрате лимфоцитов и плазматических клеток и уменьшением числа нейтральных лейкоцитов. Вокруг сосудов появляется очаговая пролиферация фибробластов.
Таким образом, через 14 суток после начала эксперимента происходит частичное очищение поверхности раны от некротических масс, образование юной грануляционной ткани, в подлежащих тканях значительно уменьшается отек, купируются сосудистые нарушения, уменьшается интенсивность воспалительной инфильтрации и изменяется состав инфильтрата.
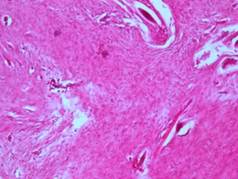
Рис. 2. Формирование зрелой соединительной ткани на месте повреждения (28-е сутки) в 1 группе. Окраска: гематоксилином и эозином х100.
Через 21 сутки от начала эксперимента происходит полное очищение поверхности раны, в грануляционной ткани уменьшается количество сосудов и клеточных элементов, увеличивается количество волокнистых структур, отмечается усиленная пролиферация фибробластов.
Таким образом, через 21 сутки в ране происходит созревание грануляционной ткани с уменьшением количества кровеносных сосудов, клеточных элементов и формированием молодой соединительной ткани, поверхность которой эпителизируется.
На 28-е сутки происходит окончательное созревание молодой соединительной ткани с образованием рубца из зрелой соединительной ткани (рис. 2).
Гистологические исследования позволяют констатировать, при вживлении в кожу пластинки из кобальто-хромового сплава в дерме появляется рана, покрытая некротическими массами, развивается серозное, а затем гнойное воспаление, формируется грануляционная ткань, на 28-е сутки образуется рубец из зрелой соединительной ткани. Особенностью является присутствие пигмента коричневого цвета. Заживление раны происходит путем вторичного натяжения.
Патогистологические изменения в коже лабораторных животных после вживления пластинок из сплава на основе золота. Через 3 суток от начала эксперимента в коже определяется резаная рана, проникающая через эпидермис и дерму до подкожно-жирового слоя. В дерме на поверхности раны определяется тканевой детрит, представленный некротическими массами, свернувшейся кровью с небольшим количеством лейкоцитов. В подлежащей соединительной ткани отмечается умеренно выраженный диффузный отек, сосудистые нарушения в виде полнокровия, кровоизлияний.
Серозное воспаление характеризуется накоплением серозного экссудата с наличием в инфильтрате небольшого количества лимфоцитов и примесью макрофагов и единичных нейтрофилов.
Через 7 суток наблюдается рассасывание тканевого детрита и лизис эритроцитов макрофагами. На поверхности раны сохраняются лишь небольшие скопления некротических масс. В окружающих тканях значительно уменьшается отек, купируется сосудистая реакция, снижается интенсивность воспалительной реакции. В краях раны появляются фибробласты, которые пролиферуют и растут навстречу друг другу, а также новообразованные капилляры. В эти сроки начинается образование юной грануляционной ткани. В отличие от первой экспериментальной группы гнойное воспаление в ране не наблюдается, отсутствует инфильтрация грануляционной ткани лимфоцитами, формирование грануляционной ткани начинается раньше и происходит более интенсивно.
Через 14-е сутки отмечается полное очищение раны от некротических масс. Раневой дефект заполнен грануляционной тканью, образован нежный рубец. Поверхность раны эпителизирована за счет разрастания 2-3 слоев плоского эпителия. Произошло заживление раны первичным натяжением.
Через 21 сутки наблюдается созревание грануляционной ткани, образуется молодая соединительная ткань и окончательно формируется рубец. В новообразованной соединительной ткани преобладают волокнистые структуры преимущественно коллагеновые волокна, а также встречаются новообразованные полнокровные сосуды. Поверхность рубца покрыта 4-5 рядами эпителия. Эпителиальный пласт частично дифференцирован на базальный и шиповатый слои.
На 28-е сутки наблюдается дальнейшее созревание и формирование рубца, а также дифференцировка эпидермиса (рис. 3).
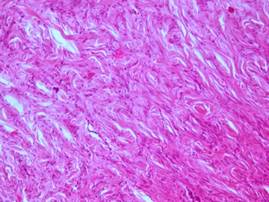
Рис. 3. Созревание и формирование рубца (28-е сутки исследования) во 2 группе. Окраска: гематоксилином и эозином х100.
Таким образом, при вживлении пластинок из сплава на основе золота заживление раны происходит первичным натяжением без гнойного воспаления. Формируется тонкий линейный рубец. Заживление раны происходит быстрее. В окружающих тканях развивается серозное воспаление в ответ на механическое повреждение и присутствие инородного тела.
Патогистологические изменения в коже лабораторных животных после вживления пластинок кобальто-хромового сплава с золото-циркониевым покрытием. Через трое суток от начала эксперимента в коже обнаружена рана с ровными краями. В краях раны наблюдается отек, кровоизлияния, кровеносные сосуды расширены и полнокровные. На поверхности раны видны отложения некротических масс, лейкоцитов, гемолизированных эритроцитов, небольшое количество фибрина. По периферии раневого дефекта в дерме и подлежащей жировой ткани отмечается отек, сосудистые нарушения и незначительная лимфоцитарная инфильтрация с примесью единичных нейтрофилов и макрофагов. Патогистологические изменения на третьи сутки аналогичны гистологической картине во второй экспериментальной группе в эти же сроки и в целом характеризуются сосудистыми нарушениями умеренной степени и развитием серозного воспаления.
Через семь суток отмечается рассасывание значительного количества некротических масс, фибрина и эритроцитов. Поверхность раны представлена формирующейся грануляционной тканью, в которой видны многочисленные капилляры. Между капиллярами по ходу фибриновых нитей отмечается усиленная пролиферация фибробластов.
В подлежащих тканях отмечается уменьшение интенсивности отека и частичное купирование сосудистых нарушений, очаговые лимфоцитарные инфильтраты. В указанные сроки в краях раны и подлежащих тканях гнойное воспаление не развивается. Наблюдается картина серозного воспаления, как и во второй экспериментальной группе. Грануляционная ткань формируется в те же сроки, что и во второй экспериментальной группе.
Через 14 суток наблюдается полное рассасывание тканевого детрита, заполнение раневого дефекта юной грануляционной тканью. В грануляционной ткани воспалительная инфильтрация не выявлена. В подлежащих тканях отмечается исчезновение отека и полное купирование сосудистых нарушений. Кое-где встречаются очаговые лимфоцитарные инфильтраты.
Через 21 сутки формируется молодая соединительная ткань, в которой уменьшается количество капилляров, количество клеточных элементов и увеличивается число волокнистых структур преимущественно коллагеновых волокон. Новообразованная молодая соединительная ткань заполняет полностью раневой дефект.
Поверхность соединительной ткани покрыта 2-3 рядами клеток плоского эпителия. Воспалительная инфильтрация в подлежащих тканях полностью купирована.
На 28-е сутки определяется окончательно сформированный рубец, состоящий из зрелой соединительной ткани (рис. 4).
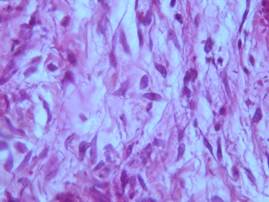
Рис. 4. Новообразованная соединительная ткань (21-е сутки в 3 группе). Окраска: гематоксилином и эозином х200.
Таким образом, при вживлении пластинок из кобальто-хромового сплава RemaniumStar (Dentfurum) с золото-циркониевым покрытием «Кэмадент» (НПК «Суперметалл») заживление раны происходит в те же сроки, что и при вживлении пластины из золотого сплава «Супер-ТЗ» (НПК «Суперметалл»). Заживление раны происходит путем первичного натяжения с формированием нежного рубца. В окружающих тканях гнойное воспаление не развивается, происходит более быстрое очищение раны.
Выводы
1. При имплантации пластинок из сплава на основе золота и кобальто-хромового сплава с золото-циркониевым покрытием структурные изменения в тканях одинаковые. Деструктивные изменения в тканях менее выражены по сравнению с изменениями тканей в ответ на имплантирование пластинок из кобальто-хромового сплава. В ответ на повреждение развивается асептическое серозное воспаление. В ране образуется грануляционная ткань, заживление происходит путем первичного натяжения и в более короткие сроки.
2. Для повышения биологической инертности конструкционных стоматологических кобальто-хромовых сплавов эффективно использование золотосодержащего композиционного покрытия.
Рецензенты:
Долгалев Александр Анатольевич, д.м.н., профессор кафедры ортопедической стоматологии ГБОУ ВПО «Ставропольская государственная медицинская академия» Министерства здравоохранения РФ, г. Ставрополь.
Николай Николаевич Гаража, д.м.н., профессор кафедры пропедевтики стоматологических заболеваний ГБОУ ВПО «Ставропольская государственная медицинская академия» Министерства здравоохранения РФ, г. Ставрополь.
Библиографическая ссылка
Гаража С.Н., Казарьянц Э.А., Гришилова Е.Н., Шармазанов В.З. ЭКСПЕРИМЕНТАЛЬНОЕ ОБОСНОВАНИЕ ПРИМЕНЕНИЯ ЗОЛОТОСОДЕРЖАЩЕГО ПОКРЫТИЯ ДЛЯ ПОВЫШЕНИЯ БИОЛОГИЧЕСКОЙ ИНЕРТНОСТИ СТОМАТОЛОГИЧЕСКИХ КОНСТРУКЦИОННЫХ СПЛАВОВ // Современные проблемы науки и образования. 2013. № 1. ;URL: https://science-education.ru/ru/article/view?id=8454 (дата обращения: 16.05.2026).



