Введение
Повышенная продукция глюкозы печенью в результате угнетения гликолиза и усиления глюконеогенеза является характерной чертой сахарного диабета (СД) 2 типа. Данные процессы – ответственные за гипергликемию у больных СД 2 типа натощак. В то же время рост концентрации глюкозы в крови после приема пищи (постпрандиальной гликемии) связан с торможением утилизации глюкозы периферическими тканями, в первую очередь мышцами [1]. Это обусловлено нарушением синтеза гликогена в результате снижения активности гликогенсинтетазы и ослабления процессов окисления глюкозы вследствие дефекта в пируватдегидрогеназном комплексе. Свой вклад в данный процесс вносят изменения в секреторной функции панкреатических бета-клеток, что проявляется в торможении первой фазы инсулинового ответа и развитии гипергликемии [5; 8].С целью изучения сравнительной характеристики ультраструктуры печени в норме и при сахарном диабете в эксперименте проведено настоящее исследование.
Материал и методы исследования
Материалом исследования явились половозрелые крысы-самцы линии «Вистар» массой 100-130 г в количестве 90 штук. Перед забором материала подопытных животных усыпляли с помощью внутрибрюшинного наркоза с использованием тиопентала натрия. Забирали небольшую часть ткани печени крыс, которую помещали сразу в большую каплю 2%-ного раствора четырехокиси осмия на 0,1 М фосфатном буфере с сахарозой. Далее вырезали полоски ткани печени размером 0,8 х 0,1 х 0,1 см и переносили их в другую каплю фиксирующего раствора, размещенного на кусочке зубоврачебного воска ледяной плиты. Из полосок вырезали блоки ткани печени кубической формы размером 1 мм3, которые фиксировали 2%-ным раствором четырехокиси осмия на 0,1 М фосфатном буфере (рН 7,36) с добавлением сахарозы в течение двух часов на ледяной бане, после чего их отмывали буферным раствором [1]. Водонерастворимые смолами и отмытые от остатков фиксаторов тканевые блоки проводили через спирты восходящей концентрации и абсолютный ацетон. Затем материал помещали в смесь эпоксидных смол эпон-аралдит путем проведения через растворы возрастающей концентрации, после чего их помещали в эпон-аралдит, находившийся в глицериновых капсулах [2; 3]. Полимеризацию материала проводили поэтапно при разных температурах от 36 до 60 °С в течение 24 часов. Ультратонкие срезы готовили на ультрамикротоме УМТП - 3М с помощью стеклянных ножей, изготовленных на приборе ССН - 1. Для исследования отбирали срезы серебристого или нежно-лимонного цвета. Срезы контрастировали сначала в 2℅-ном растворе уранилацетата [7], а затем – цитрата свинца [6]. Изучение и фотографирование материала проводили с помощью микроскопа УЕМВ - 100К .
Результаты исследования
В норме у интактных крыс печеночные пластинки построены из гепатоцитов, объединенных с помощью плотных контактов, образующих желчные канальцы. При ультраструктурном исследовании в цитоплазме гепатоцитов хорошо выражены канальцы эндоплазматической сети, многочисленные лизосомы и пероксисомы, цистерны комплекса Гольджи, расположенные в различных отделах клеток. Митохондрии имеют сферическую или овальную форму от 0,8 до 2 мкм в диаметре, небольшую численность крист и электронноплотный матрикс с митохондриальными гранулами. В цитоплазме гепатоцитов находятся включения гликогена и липидов. Гранулы гликогена местами образуют агрегаты в виде розеток, тогда как липидные гранулы имеют вариабельнную электронную плотность и не окружены мембранами. Ядра, как правило, расположены в центре гепатоцитов и имеют овальную или сферическую форму с просветленным хроматином. Ядра содержат 1-2 ядрышка и имеют широкопетлистую ретикулярную структуру (рис. 1).
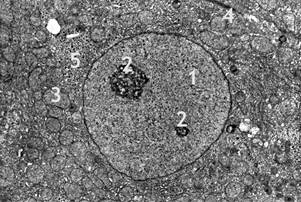
Рис. 1. Печень интактной крысы. Фрагмент гепатоцита. Увеличение x 5000.
1 – ядро; 2 – ядрышки; 3 – митохондрии; 4 – канальцы эндоплазматической сети; 5 – включения гликогена.
Эндотелиоциты отделяют пространства синусоидов от пиресинусоидальних пространств и имеют продолговатую форму, а их ядра располагаются в центре. Вокруг полюсов ядра находится компактная зона органелл с цистернами комплекса Гольджи, канальцами агранулярной и гранулярной эндоплазматической сети и многочисленными митохондриями. Наибольшей протяженностью характеризуется периферийная зона, в которой расположены немногочисленные органеллы. Она содержит плазмолемные везикулы, связанные с базальной и адлюменальной поверхностями плазмолемы. В периферийной части эндотелиоцитов расположены фенестры, не затянутые диафрагмами. В месте контактов эндотелиоциты содержат многочисленные отростки, благодаря которым образуются ситообразные зоны в стенке синусоидов. Базальная мембрана вокруг эндотелиальных клеток не образует сплошного слоя, ее фрагменты выявляются вокруг периферической зоны эндотелиоцитов. В просветах синусоидов и между эндотелиоцитами расположены звездчатые макрофагоциты. Они имеют многочисленные псевдоподии и складки мембраны с ядрами бобовидной формы. Вблизи вогнутой поверхности ядра находятся цистерны комплекса Гольджи и многочисленные лизосомы. В просветах синусоидов обнаруживаются печеночные клетки-убийцы. Они имеют сферическую форму, электронноплотные ядра и своими отростками фиксируются к плазмолемме эндотелиоцитов. Их цитоплазма содержит гранулы с электронноплотным центром, а также фагоцитарные пузырьки. При ультраструктурном исследовании портальных триад обнаруживаются междольковые артерии, вены, желчные протоки, а также лимфатические сосуды. Стенка междольковых артерий состоит из трех оболочек. Во внутренней оболочке находится сплошной пласт эндотелиальных клеток, расположенных на базальной мембране. В подэндотелиальном слое расположены малодифференцированные клетки, эластичные и коллагеновые волокна. В междольковых артериях хорошо выражена внутренняя эластическая мембрана. Средняя оболочка включает 1-2 слоя гладких миоцитов. Внешняя оболочка состоит из адвентициальних клеток. Вокруг артерий расположены фибробласты, коллагеновые и эластичные волокна. В просветах междольковых вен иногда оказываются моноциты и лимфоциты. В средней оболочке гладкие миоциты не образуют сплошного слоя, их внешняя оболочка состоит из рыхлой соединительной ткани, а в периваскулярном пространстве расположены фибробласты, коллагеновые и эластичные волокна, а также одиночные лимфоциты. Стенка междольковых желчных протоков состоит из кубических клеток с электронно-светлой цитоплазмой и ядрами. Вокруг желчных протоков находятся фибробласты, коллагеновые и эластичные волокна, а также единичные лимфоциты.
Через 8 недель развития экспериментального СД нами отмечено увеличение численности и размеров жировых включений в цитоплазме гепатоцитов и уменьшение включений гликогена (рис. 2).
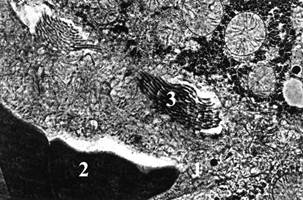
Рис. 2. Печень крыс через 8 недель после введения стрептозотоцина. Сб. × 7000.
1 – отек эндотелиоцитов; 2 – сладж эритроцитов в просвете синусоида; 3 – гиперплазия коллагеновых волокон в перисинусоидальных пространствах.
Возрастает число митохондрий и гетерогенность в структуре ядер. При этом встречаются сферические ядра со структурой хроматина и ядрышек, подобных интактным животным, но с увеличенной численностью гиперхромных ядер и конденсированным по краям хроматином. Перинуклеарные пространства вокруг таких ядер значительно расширены. Обнаруживаются гепатоциты с пикнотическими ядрами, которые имеют причудливую форму. Межклеточные пространства гепатоцитов видоизменены и расширены, в них выявляются коллагеновые фибриллы и фибробласты. Перисинусоидальные пространства расширены, заполнены коллагеновыми волокнами, среди которых обнаруживаются многочисленные фибробласты, звездчатые макрофагоциты и редко перисинусоидальные жиронакопительные клетки, в цитоплазме которых находятся гигантские удлиненные митохондрии червеобразной формы с многочисленными плотноупакованными кристами. Диаметры синусоидов сужены, часто встречается сладж эритроцитов, а также многочисленные звездчатые макрофагоциты и тромбоциты, которые контактируют с плазмолемой эндотелиоцитов. Эндотелиоциты в периферийной зоне утолщены. Их цитоплазма имеет неоднородную электронную плотность и содержит темные и светлые клетки, вакуоли, канальцы эндоплазматической сети, а также расширенные комплексы Гольджи и полиморфные митохондрии. Часто обнаруживаются просветленные митохондрии с деструктурированными кристами. Плазмолемальных везикул в таких клетках мало по сравнению с интактной группой животных. Ядра в эндотелиоцитах часто отечны, осмиофильные (рис. 3).
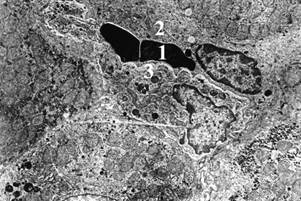
Рис. 3. Печень крыс через 8 недель после введения стрептозотоцина.
1 – сужение просветов синусоидов; 2 – утолщенные стенки синусоидов; 3 – базальная мембрана вокруг эндотелиоцитов.
Вокруг эндотелиоцитов обнаруживается базальная мембрана. В портальных трактах – выраженный склероз. Стенки артериол утолщены, эндотелиальная выстилка в них не сплошная. В средней оболочке наблюдаются процессы гипертрофии и гиперплазии гладких миоцитов. Стенка вен склерозирована и утолщена с наличием деструктивных фибробластов. Пространство желчных протоков расширено и заполнено остатками эпителиоцитов. Вокруг желчных протоков наблюдается гистиолимфоцитарная инфильтрация с отечными эндотелиоцитами и расширение диаметров лимфатических сосудов.
Через 10 недель эксперимента, наряду с вышеуказанными изменениями, отмечается увеличение числа деструктуризированых митохондрий и крупных жировых включений в гепатоцитах с уменьшением в них содержания гликогена (рис. 4).

Рис. 4. Печень крыс через 10 недель после введения стрептозотоцина. Сб. × 3000.
1 – деструкция митохондрий; 2 – выраженная жировая дистрофия цитоплазмы гепатоцитов.
Возрастает количество пикнотичных и формализованных ядер в гепатоцитах, расширяются их межклеточные и перисинусоидальные пространства и просветы в желчных капиллярах. Обнаруживаются разрастания коллагеновых волокон с гипертрофией и гиперплазией фибробластов. Возрастает численность снежных макрофагоцитов, суживаются синусоидальные капилляры и уменьшается численность перисинусоидальных жиронакопительных клеток. В них часто обнаруживается сладж эритроцитов и лейкоцитов. Эндотелиальные клетки в стенке синусоидных капилляров полиморфны. Их цитоплазма неоднородна с малым количеством органелл и деструктироваными митохондриями. Ядра часто выступают в просвет синусоидов, в них наблюдается маргинальная агрегация хроматина, ядрышки не определяются. Вокруг зоны органелл часто образуется базальная мембрана. В портальных трактах наблюдается склероз и гиперплазия фибробластов. При этом стенки междольковых артерий утолщены и склерозированы, в их просветах часто появляются пристеночные тромбы. Диаметры междольковых желчных протоков расширены, их стенки утолщены, лимфатические сосуды расширены.
Таким образом, на поздних этапах развития экспериментального СД происходят изменения в артериолах, характеризующиеся деструкцией эндотелиоцитов, гипертрофией и гиперплазией гладких миоцитов, сужением просвета и гиперплазией фибробластов в наружной оболочке артериол, а также гиперемией центральных и междольковых вен. В синусоидах, наряду с деструктивными изменениями в эндотелиоцитах, проходят процессы активации и увеличения численности макрофагоцитов и их миграция в перисинусоидальные пространства, что приводит к трансформации жиронакопительных клеток в фибробласты и разрастанию коллагеновых волокон. Расширение перисинусоидальных пространств приводит к утолщению барьера между кровью и гепатоцитами с последующим нарушением обмена веществ.
Рецензенты:
Матещук-Вацеба Л.Р., д.м.н., профессор кафедры нормальной анатомии Львовского национального медицинского университета им. Данила Галицкого, г. Львов.
Жилякова Е.Т., д.ф.н., профессор, зам. директора ООО «Асклепий», г. Белгород.
Библиографическая ссылка
Согуйко Ю.Р., Кривко Ю.Я., Крикун Е.Н., Новиков О.О. МОРФОФУНКЦИОНАЛЬНАЯ ХАРАКТЕРИСТИКА ПЕЧЕНИ КРЫС В НОРМЕ И ПРИ САХАРНОМ ДИАБЕТЕ В ЭКСПЕРИМЕНТЕ // Современные проблемы науки и образования. 2013. № 1. ;URL: https://science-education.ru/ru/article/view?id=8297 (дата обращения: 09.06.2026).



