Мужское бесплодие и нарушение отцовского генома – актуальная проблема современной репродуктивной медицины. Причинами бесплодия могут быть патологические состояния, возникающие при инфекционно-воспалительных процессах, нарушениях эндокринной и нервной регуляции активности гонад. Действие патогенных факторов может проявляться как на макроскопическом уровне, так и на уровне генома половых клеток. В последнее десятилетие интенсивно исследуется одна из недавно открытых причин мужского бесплодия и отцовского эффекта нарушений раннего эмбрионального развития – фрагментация ДНК созревающих мужских половых клеток и сперматозоидов.
Функциональная активность мужских гонад и, в частности, течение сперматогенеза находятся под контролем эндокринной, нервной и иммунной систем организма. Помимо гипоталамо-гипофизарной системы в настоящее время определено участие эпифиза в становлении репродуктивной функции и регуляции суточной активности семенников. Известно, что эпифизарная недостаточность приводит к преждевременному половому созреванию [4], а в период репродуктивной активности – к росту пролиферативной активности сперматогоний и рассогласованию течения сперматогенеза со свето-темновым циклом [2]. Однако качественные показатели сперматогенных клеток и, в частности, состояние ДНК созревающих половых клеток при данной патологии остаются до настоящего времени неисследованными.
Процесс пролиферации и дифференцировки половых клеток сопровождается удалением части клеток на каждой стадии созревания сперматозоидов [7]. Несомненно, такой процесс, как апоптоз, который сопровождается синтезом белков de novo и имеет многочисленные регуляторные механизмы, должен быть согласован с общей ритмической структурой функции. В предыдущих работах нами был показан циркадианный ритм пролиферативной активности сперматогоний и его нарушение после эпифизэктомии [2]. В связи с этим естественно предполагать наличие циркадианного ритма и процесса апоптоза созревающих половых клеток.
Целью настоящей работы явилось изучение уровня активности ферментов – индукторов апоптоза в сперматогенных клетках на протяжении суток у интактных животных и животных после эпифизэктомии.
Материалы и методы. Опыт выполнен на 48 самцах беспородных белых крыс массой 160–200 г. Животные в течение 20 дней адаптировались к 12 часовому режиму освещенности (освещение с 6 до 18 ч). На всем протяжении опыта доступ к пище и воде был свободным. Для изучения хроноструктуры активности ферментов индукторов апоптоза в сперматогенных клетках и влияния эпифизэктомии на данный процесс по истечении адаптационного периода крысы были разделены на две экспериментальные группы: интактные контрольные (n = 24) и эпифизэктомированные (n = 24). ![]()
![]() Эпифизэктомия проводилась по оригинальной методике [1]. Все эксперименты, уход и содержание животных осуществлялись в соответствии с Директивой №63 от 22.09.10 г. Президиума и Парламента Европы «О защите животных, используемых для научных исследований» и приказом Минздрава РФ №267 от 19.06.2003 «Об утверждении правил лабораторной практики». Наркоз осуществлялся путем внутрибрюшинного введения тиопентала натрия в дозе 50 мг/кг. Выживаемость животных после операции составила 68 %. Эпифизэктомированных животных продолжали содержать при режиме освещенность/темнота равном 12/12 (освещение с 6 до 18 ч). Животных с неудовлетворительным состоянием, выражающемся в нарушении координации движений, уменьшении веса, нарушениях функций кишечника, с воспалительными процессами, в эксперименте в дальнейшем не использовали.
Эпифизэктомия проводилась по оригинальной методике [1]. Все эксперименты, уход и содержание животных осуществлялись в соответствии с Директивой №63 от 22.09.10 г. Президиума и Парламента Европы «О защите животных, используемых для научных исследований» и приказом Минздрава РФ №267 от 19.06.2003 «Об утверждении правил лабораторной практики». Наркоз осуществлялся путем внутрибрюшинного введения тиопентала натрия в дозе 50 мг/кг. Выживаемость животных после операции составила 68 %. Эпифизэктомированных животных продолжали содержать при режиме освещенность/темнота равном 12/12 (освещение с 6 до 18 ч). Животных с неудовлетворительным состоянием, выражающемся в нарушении координации движений, уменьшении веса, нарушениях функций кишечника, с воспалительными процессами, в эксперименте в дальнейшем не использовали.
Выведение животных из эксперимента производили под эфирным наркозом на 40 – 41-й день после эпифизэктомии в 1 ч (темное время) и 13 ч (светлое время) в течение двух суток, что обеспечивало исследование активности ферментов на протяжении двух периодов циркадианного ритма. В каждую временную точку эксперимента входило по 6 животных контрольной и опытной групп.
Семенники фиксировали в забуференном формалине, и по стандартной гистологической методике изготавливали парафиновые поперечные срезы толщиной 5 мкм. Об уровне апоптоза созревающих сперматогенных клеток судили по активности ферментов, участвующих в индукции апоптоза (прокаспаза 3) и в посттрансляционной репарации ДНК (PARP-1). Белки-ферменты выявлялись иммуногистохимически на парафиновых срезах в патологоанатомической лаборатории Республиканской клинической больницы г. Казани. Оценку активности ферментов проводили в сперматоцитах на стадии метафазы мейоза и сперматидах 7–8 этапа развития, используя показатель оптической плотности окрашивания ядер (программа денситофотометрии Мекос-С1).
Для микроскопирования применяли микроскоп Axiostar Plus (Carl Zeiss) при увеличении х1000 (окуляр х10, объектив х100). Измерения производились с помощью медицинской компьютерной видеосистемы, состоящей из микроскопа Axiostar Plus (Carl Zeiss), цифровой фотокамеры Nikon COOLPIX 995, персонального компьютера Рentium-IV и программы автоматизированной обработки изображений Месоs C-1. Статистическую обработку результатов проводили с использованием метода Фишера – Стьюдента. Уровень значимости был принят P<0,05.
Результаты и их обсуждение
У интактных животных наблюдался циркадианный ритм уровня содержания PARP-1 (p116/25) и прокаспазы-3 в созревающих половых клетках, о чем судили по оптической плотности комплексов белок-АТ (рис. 1), определяемых в темное и светлое время суток в течение эксперимента.
а) 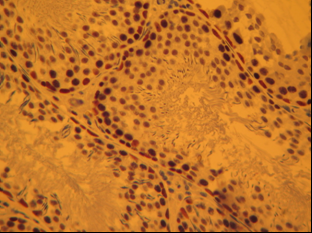 б)
б) 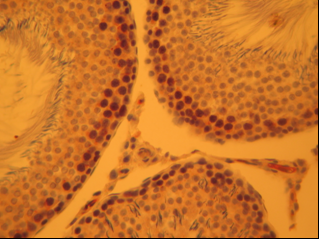
Рис. 1. Сперматогенная и эндокринная ткань семенников интактных животных. Иммуногистохимическое окрашивание на PARP-1 (p116/25) – А и прокаспазу 3 – Б, доокрашивание гематоксилином. Увеличение х400
Уровень содержания прокаспазы 3 в сперматоцитах на этапе мейоза и сперматидах 7–8 этапа развития, определяемый по удельной оптической плотности иммуногистохимически окрашиваемого комплекса прокаспаза 3 – первичные АТ (прокаспаза 3) – DAB-chromogen имел закономерные различия при определении в темновую и световую фазу эксперимента.
Таблица 1
Суточная динамика оптической плотности комплексов белок-АТ в сперматогенных клетках интактных белых крыс (M±m), опт. ед.
|
Этап развития половых клеток |
PARP-1 |
Прокаспаза 3 |
||
|
Светлое время |
Темное время |
Светлое время |
Темное время |
|
|
Ядра сперматид 7–8 этапов развития |
0,399±0,025 |
0,567±0,018 |
0,257±0,031 |
0,417±0,037 |
|
Цитоплазма сперматоцитов на этапе мейоза |
0,172±0,036 |
0,398±0,029 |
0,103±0,022 |
0,290±0,026 |
Содержание прокаспазы 3 как в сперматоцитах, так и в сперматидах было значительно выше в темновую фазу эксперимента (табл.1). Известно, что при стимуляции ткани каким-либо митогеном, ее клетки переходят в состояние повышенной митотической активности, которое сопровождается активацией апоптоза [5]. В случае сперматогенеза повышение уровня пролиферативных процессов в темновую фазу эксперимента [2] приводит к тому, что уровень ферментов-индукторов апоптоза также повышается в темновую фазу цикла.
Помимо концентрации прокаспазы 3 в сперматогенных клетках нами определялась удельная оптическая плотность иммуногистохимического комплекса PARP-1 – первичные АТ(PARP-1) - DAB-chromogen (рис.1, табл.1). Высокая каталитическая активность фермента проявляется только при повреждении ДНК. Независимо от пути, по которому протекает апоптоз, его конечным итогом является разрушение ДНК с последующей активацией полимеразы 1 поли(АДФ-рибозы) (PARP-1) [8]. Активность PARP-1 возрастает в 500 раз и более при связывании с участками разрыва ДНК. В целом у интактных животных динамика активности PARP-1 соответствовала изменениям уровня прокаспазы-3 в сперматоцитах и сперматидах при спермиации и на этапе мейоза. Также определялись различия концентрации данного фермента в темновую и световую фазу в течение двух суток эксперимента, что свидетельствует о циркадианном ритме его активности. Повышение уровня PARP-1 наблюдалось в темное время эксперимента, как и рост пролиферативной активности сперматогоний и сперматоцитов.
Таким образом, у интактных животных наблюдался циркадианный ритм физиологической дегенерации части созревающих половых клеток. Выявленный ритм обнаруживал зависимость от свето-темнового цикла. Так, процессы размножения клеток и активация ферментов, участвующих в удалении поврежденных половых клеток, наиболее активно происходили в темную фазу суток, а процесс спермиации (отделения созревших сперматозоидов от сустентоцитов) наблюдался преимущественно в светлую фазу суток.
Несмотря на повышенную митотическую активность сперматогоний, масса семенников после эпифизэктомии не изменилась. По свидетельству Рузен-Ранге [6], количество возможно образовавшихся сперматозоидов из одной стволовой сперматогонии для данного вида животных всегда постоянно и не зависит от каких-либо регуляторных влияний. Число образующихся сперматозоидов определяется количеством делений стволовой сперматогонии в процессе дифференцировки. Однако оно всегда ниже, чем можно предположить путем простого умножения. Данное снижение обеспечивается процессами физиологической дегенерации, которым подвергается часть дифференцирующихся половых клеток, благодаря чему в организме достигается биологическое равновесие между процессами пролиферации сперматогоний и выходом зрелых сперматозоидов [3]. Вероятно, после эпифизэктомии происходит как увеличение пролиферативной активности сперматогоний, так и повышение процента дегенерирующих клеток, что в целом не отражается на массе органа у полиэстричных животных.
С целью подтверждения данного предположения нами исследовался уровень содержания некоторых ферментов в извитых семенных канальцах, участвующих в процессах апоптоза созревающих половых клеток (прокаспаза-3, PARP-1) у эпифизэктомированных крыс (рис.2). После удаления эпифиза произошло достоверное повышение уровня данных ферментов, с утратой различий экспрессии в темное и светлое время суток (табл. 2).
а) 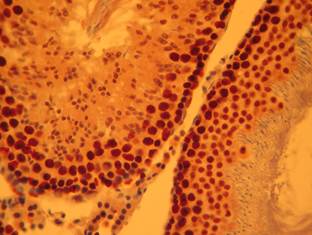 б)
б) 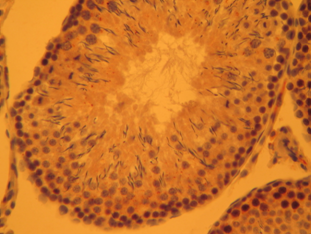
Рис. 2. Сперматогенная и эндокринная ткань семенников эпифизэктомированных животных. Иммуногистохимическое окрашивание на PARP-1 (p116/25) – а и прокаспазу 3 – б, доокрашивание гематоксилином. Увеличение х400
Данный факт свидетельствует о том, что с ростом пролиферативной активности сперматогоний после эпифизэктомии увеличивается и количество «поломок» в структуре ДНК, а соответственно и большее количество созревающих половых клеток удаляется из дальнейшей дифференцировки.
Таблица 2
Суточная динамика оптической плотности комплексов белок-АТ в сперматогенных клетках эпифизэктомированных белых крыс (M±m), опт. ед.
|
Этап развития сперматогенных клеток |
PARP-1 |
Прокаспаза 3 |
||
|
Светлое время |
Темное время |
Светлое время |
Темное время |
|
|
Ядра сперматид 7–8 этапов развития |
0,615±0,027 |
0,603±0,018 |
0,428±0,052 |
0,467±0,071 |
|
Цитоплазма сперматоцитов на этапе мейоза |
0,384±0,042 |
0,440±0,056 |
0,183±0,031 |
0,243±0,058 |
Эти положения согласуются с общепринятым понятием об апоптозе как фундаментальном биологическом процессе, занимающем ведущее место в поддержании гомеостаза и сохранении клеточного баланса в многоклеточном организме. Хорошо известны свойства одного из гормонов эпифиза – мелатонина, как протектора ДНК и сильного антиоксиданта [9]. Вероятно, в отсутствие биоактивных веществ эпифиза и при повышении пролиферативной активности сперматогоний уровень нарушений в структуре ДНК созревающих половых клеток значительно увеличивается, что приводит к активации белков-ферментов, запускающих программу апоптоза.
Заключение. Таким образом, апоптоз, являющийся необходимым звеном процесса созревания мужских половых клеток, характеризуется циркадианным ритмом, который утрачивается после эпифизэктомии. В то же время удаление эпифиза приводит к значительному росту не только пролиферативной активности сперматогоний, но и росту среднего уровня активности ферментов – индукторов апоптоза. Данный факт свидетельствует о повышении количества созревающих половых клеток, несущих в себе структурные патологии и, в первую очередь, нарушения в структуре их ДНК.
Работа выполнена в рамках госзадания Минобрнауки России.
Рецензенты:
Ильина Наталья Анатольевна, доктор биологических наук, профессор, проректор по науке
ФГБОУ ВПО «Ульяновский государственный педагогический университет им. И. Н. Ульянова», г. Ульяновск.
Перфильева Наталья Петровна, доктор биологических наук, профессор кафедры анатомии, физиологии и гигиены человека и животных ФГБОУ ВПО «Ульяновский государственный педагогический университет им. И. Н. Ульянова», г. Ульяновск.
Библиографическая ссылка
Слесарева Е.В., Слесарев С.М., Арав В.И., Ляпейкова О.В., Гальчин А.В. ЦИРКАДИАННЫЙ РИТМ АПОПТОЗА СПЕРМАТОГЕННЫХ КЛЕТОК ИНТАКТНЫХ БЕЛЫХ КРЫС И ЕГО НАРУШЕНИЯ ПОСЛЕ ЭПИФИЗЭКТОМИИ. // Современные проблемы науки и образования. 2013. № 1. ;URL: https://science-education.ru/ru/article/view?id=8251 (дата обращения: 05.05.2026).



