Введение. Считается, что угроза прерывания беременности может быть одновременно причиной плацентарной недостаточности и ее следствием [1; 2; 4; 5]. Дискуссионным остается вопрос, какое из этих осложнений формируется первично. Для определения группы риска по развитию плацентарной недостаточности у беременных с угрожающим прерыванием беременности в качестве ранних тестов должен быть исследован комплекс гормонов и ферментов, вырабатываемых в фето-плацентарном комплексе, так как определение только одного из показателей не может служить основанием для заключения о патологическом развитии ФПК.
Цель исследования – разработка алгоритма ранней диагностики дисфункций плаценты при угрожающем прерывании беременности.
Материал и методы. Для достижения поставленной цели были обследованы 50 здоровых беременных (контрольная группа) и 97 женщин с угрожающим абортом, у 56 из которых дальнейшее течение беременности осложнилось развитием плацентарной недостаточности (ПН) в сроки беременности от 5 до 22 недель. По возрасту, соматическому и акушерско-гинекологическому анамнезу обследованные группы были сопоставимы.
Уровень ТБГ (мг/л) капиллярной крови и β-субъединицы ХГ определяли иммуноферментным методом. Эстриол мочи (мкмоль/л) исследовали методом Brown a Coyle, прегнандиол (нмоль/л) методом Клоппера; фермента ТЩФ – методом Боданского.
Полученные результаты подвергались статистической обработке с помощью интегрированных программ «Облегченные способы статистического анализа в клинической медицине» (Бенсман В.М., 2002) и Microsoft Excel 2000.
Результаты исследования. Диагностическим критерием хориальной и плацентарной дисфункций считают уменьшение экскреции эстриола (Е3) с мочой. Определение эстриола в моче имеет целый ряд существенных преимуществ, таких как: неинвазивность, отсутствие зависимости от циркадных колебаний гормонов в крови, которые часто бывают значительными, а также возможность суммарного учета суточной экскреции гормона.
При исследовании этого показателя у здоровых беременных установлено, что экскреция эстриола с мочой до 12 недель беременности составляла 3,32±0,55 мкмоль/л (табл. 1). С увеличением срока беременности содержание эстриола в моче увеличивается в сроки 13 – 16 недель на 70,0% (Р≤0,001), а после 17 недель в 2 раза относительно предыдущего показателя и в 7 раз по сравнению с его экскрецией в первом триместре беременности. У беременных с угрожающим абортом уровень эстриола не отличался от показателя при аналогичных сроках нормального гестационного процесса, однако с прогрессированием беременности нарастание Е3 в моче было не столь значительным. В 13–16 недель этот прирост составлял 46% (Р≤0,01), а после 17 недель – в 3,7 раза по сравнению с ранними сроками беременности, что было ниже нормального показателя в 1,5 раза. При беременности, осложненной угрозой прерывания и плацентарной недостаточностью, в ранние сроки беременности содержание эстриола в моче не отличалось от уровня показателя в предыдущих группах. Однако в момент наиболее активного формирования плаценты (в 13–16 недель беременности) отмечалась гипоэстриолурия в 2,5 раза относительно показателя при аналогичных сроках нормально развивающейся беременности, и в 2 раза – по сравнению с его уровнем при угрожающем аборте. По окончании формирования плаценты количество эстриола в моче у беременных этой группы повышалось в 3,4 раза, однако уровень его все-таки оставался ниже, чем при нормальной гестации на 37,8% (Р≤0,05).
При исследовании динамики экскреции хорионического гонадотропина выявлено нарастающее снижение его содержания на 50% и более, что свидетельствовало о формировании плацентарной недостаточности. Как правило, снижение уровня ХГЧ коррелировало со снижением уровня эстрогенов, секреция которых, как известно, находится под контролем ХГЧ.
Результаты исследований показали, что при физиологической беременности до 16 недель уровень ХГЧ достоверно не изменялся и составлял 69633±18812 МЕ/л до 12 недель беременности и 77325±1552 МЕ/л в 13–16 недель. После 17 недель уровень этого гормона снижался на 48,2% (Р≤0,01) по отношению к ранним срокам беременности. При угрожающем прерывании беременности в первом триместре содержание ХГЧ достоверно не отличалось от нормативных показателей. Но с увеличением гестационного срока происходило падение уровня гормона на 171,0% (Р≤0,01) в 13–16 недель и почти в 2,5 раза – после 17 недель относительно начального показателя. При формировании плацентарной недостаточности на фоне угрожающего аборта изначально, с ранних сроков беременности, отмечалось снижение уровня ХГЧ на 101,7 (Р≤0,01) по сравнению с нормальным уровнем в аналогичные сроки. Резкое падение содержания гормона, в 1,8 раза относительно исходного показателя, происходило в 13–16 недель беременности. После 17 недель у этого контингента беременных уровень ХГЧ оставался низким и был в 2 раза меньше нормативного.
Другим тестом, применяемым для лабораторной диагностики ПН в различные сроки беременности, является количественное определение трофобластического b1-гликопротеина (ТБГ) в сыворотке материнской крови [5]. Синтез его происходит в клетках синцитиотрофобласта, а локализация в незрелой плаценте в цитоплазме цитотрофобластов и синцитиотрофобластов хориона [3]. Уровень ТБГ до 12 недель нормально развивающейся беременности составлял 29,80±2,77 мг/л. Прогрессирование беременности сопровождалось значительным ростом уровня трофобластического β1-гликопротеина в 13–16 недель на 54,8% (Р≤0,01), а после 17 недель в 5,5 раза.
У беременных с угрожающим абортом уровень ТБГ в ранние сроки оказался на 42,8% (Р≤0,01) выше, чем при физиологической беременности, что происходило за счет деструкции трофобласта и массивного поступления ТБГ в материнский кровоток из разрушенных клеток хориона в процессе отслойки плодного яйца. К 13–16 неделям уровень протеина снижался на 22,7% (Р≤0,05), а после 17 недель – возрастал на 14,7% (Р≤0,05), но был в 2,5 раза ниже аналогичного показателя при нормальной гестации.
При сочетании угрожающего аборта с плацентарной недостаточностью зафиксировано снижение уровня ТБГ в первом триместре беременности почти на 1/3 по сравнению с нормой. Дальнейшее развитие беременности у этих женщин сопровождалось прогрессивным повышением содержания в крови ТБГ: на 19,1% (Р≤0,05) – в 13-16 недель беременности и 65,0% (Р≤0,05) – после 17 недель. Представленные факты позволяют полагать, что достаточно низкое содержание ТБГ у этих пациенток можно объяснить снижением интенсивности биосинтеза белков (в том числе и ТБГ) в синцитиотрофобласте.
Исследование экскреции прегнандиола с мочой при физиологической беременности показало, что уровень этого гормона до 12 недель составлял 6,95±0,39 нмоль/л. В сроки 13–16 недель произошло повышение показателя на 23,1% (Р≤0,05) при сохранении его на том же уровне до конца беременности. При угрожающем аборте начальный уровень экскреции прегнандиола не отличался от нормального и составлял 6,15±2,06 нмоль/л, однако к 13–16 неделям содержание его в моче снизилось на 51,4% (Р≤0,05), по сравнению с нормой. В дальнейшем, после 17 недель, уровень прегнандиола возрастал на 34,9% (Р≤0,05) по сравнению с исходным и достигал значений при физиологической беременности (рис. 1).
Следует отметить, что при угрожающем аборте, сочетающемся с плацентарной недостаточностью, уровень прегнандиола в первом триместре в моче был повышен на 21,6% (Р≤0,05), однако в 13–16 недель наблюдалось снижение его экскреции на 86,1% (Р≤0,01) по сравнению с исходным значением и на 89,9% (Р≤0,05) относительно уровня при нормальной гестации. В более поздние сроки происходило дальнейшее снижение прегнандиола, в результате уровень его стал ниже нормативного значения в 2,3 раза.
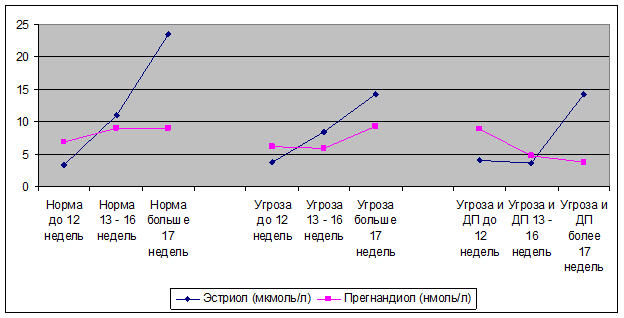
Рис. 1. Динамика экскреции эстриола и прегнандиола в норме и при угрожающем аборте.
При проведении корреляционного анализа между экскрецией эстриола и прегнандиола до 12 недель нормальной беременности статистически значимой связи не было. При сроках беременности 13–16 недель установлена умеренная обратная корреляция (r= -0,439; р<0,01), а после 17 недель эта связь становилась прямой – (r=0,408; р<0,01). При угрожающем прерывании беременности в сроки до 12 недель выявлялась высокая прямая корреляция со значением коэффициента 0,815 (р<0,01), однако с увеличением срока беременности эта связь уменьшалась: к 13–16 неделям r=0,317 (р<0,05), т.е. оказалась умеренной, а после 17 недель практически исчезала. При угрожающем аборте, сопровождающемся дисфункцией плаценты, только после 17 недель была отмечена заметная прямая корреляционная связь со значением r=0,593 (р<0,01).
Определение дегидроэпиандростерона является одним из ведущих маркеров функции фето-плацентарного комплекса. В норме до 12 недель уровень экскреции ДЭА составлял 0,365±0,029 нмоль/л и достоверно не изменялся до 16 недель. После 17 недель значение ДЭА увеличивалось на 30,2% (Р≤0,05). Угрожающее прерывание беременности сопровождалось повышением экскреции ДЭА практически в 1,5 раза до 16 недель беременности. После 17 недель не происходило достоверного изменения этого гормона относительно исходных значений, но отмечена тенденция к его повышению относительно нормы. Присоединение дисфункции плаценты происходило на фоне повышения уровня ДЭА до 12 недель беременности на 24,0% (Р≤0,05) по сравнению с нормативными показателями. К 13–16 неделям его значение увеличивалось на 46,7% (Р≤0,01) по сравнению с нормой, а после 17 недель происходило снижение экскреции ДЭА на 85,5% (Р≤0,05) по сравнению с физиологической беременностью.
Еще одним индикатором ранней диагностики дисфункций плаценты можно считать уровень в крови термостабильной щелочной фосфатазы (ТЩФ). Лабораторно диагностированное появление ее в крови произошло после 17 недель беременности, при этом содержание изофермента составило 0,33±0,03 мкмоль/ч·л. Активность ТЩФ до 16 недель беременности, осложненной угрожающим абортом, была на уровне этого показателя, но раннее появление ее в крови, можно объяснить (как и повышение ТБГ) деструкцией трофобласта при локальной отслойке плодного яйца. В более поздние сроки происходил рост активности ТЩФ в 3 раза. Для плацентарной недостаточности также было характерно раннее появление термостабильного изофермента в крови. Но повышение его активности на 41,1% (Р≤0,05) проявилось уже к 13–16 неделе, а после 17 недель содержание ТЩФ снижалось и оказалось ниже первоначального уровня на 37,0% (Р≤0,05). По данным одних авторов [7], эстрогены, одни или в сочетании с андрогенами, понижают активность ЩФ; согласно другим источникам, эстрогены и андрогены увеличивают сывороточную активность ЩФ [6]. Изменения активности ТЩФ происходили на фоне стабильной высокой активности общей щелочной фосфатазы при осложненном течении беременности и при прогрессивном повышении со сроком беременности активности общей ЩФ, которое, однако, в норме было в 2 раза ниже, чем у женщин с угрожающим абортом в обеих подгруппах.
Проведенный анализ исследования позволяет выделить биохимические маркеры прогнозирования плацентарной недостаточности при угрожающем прерывании беременности:
Ø снижение содержания эстриола в моче ниже 4,5 мкмоль/л в 13–16 недель беременности;
Ø снижение ХГЧ ниже 35000МЕ/л до 12 недель беременности;
Ø снижение ТБГ в крови ниже 25,00 мг/л;
Ø повышение уровня экскреции прегнандиола с мочой в ранние сроки беременности на 20% с дальнейшим прогрессивным снижением его уровня в 2 раза;
Ø снижение уровня ДЭА после 17 недель беременности на 85%;
Ø раннее (до 12 недель) появление в крови ТЩФ с быстрым повышением и последующим быстрым снижением активности изофермента.
Использование перечисленных показателей в комплексном обследовании беременных с угрожающим абортом позволит более объективно оценивать их метаболический статус и своевременно диагностировать возникновение плацентарной недостаточности.
Таблица 1 – Гормональные и ферментные показатели функции фето-плацентарного комплекса у беременных с угрожающим абортом (M±m)
|
Группа
Показатель |
Контрольная группа |
Угрожающий аборт |
Угрожаюший аборт с ПН |
||||||
|
До 12 недель |
13-16 недель |
17 недель и более |
До 12 недель |
13-16 недель |
17 недель и более |
До 12 недель |
13-16 недель |
17 недель и более |
|
|
Эстриол мочи (мкмоль/л) |
3,32±0,55 |
11,05±2,612 |
23,46±8,823 |
3,87±0,26 |
8,41±0,321,2 |
14,25±3,431,3 |
4,11±0,72 |
3,65±0,921,4 |
14,32±2,681,3 |
|
ХГ (МЕ/л) |
69633±18812
|
77325±1552 |
45853±122823 |
89606±41711 |
32986±124291,2 |
26171±51381,3 |
34526±13891,4 |
18871±45821,2,4 |
20676±33921 |
|
ТБГ (мг/л) |
29,80±2,77
|
66,00±6,212 |
162,75±16,813 |
52,13±1,941 |
42,50±2,891,2 |
61,14±6,221,3 |
23,15±2,371,4 |
28,63±1,521,2,4 |
41,25±2,181,3,4 |
|
Прегнан- диол (нмоль/л) |
6,95±0,39 |
9,04±2,292 |
9,04±2,08 |
6,148±2,06 |
5,97±1,421 |
9,30±1,973 |
8,86±1,43 |
4,76±1,581,2 |
3,86±0,141 |
|
ДЭА (нмоль/л) |
0,365± 0,029 |
0,333±0,026 |
0,523±0,0933 |
0,609±0,0681 |
0,659±0,0571 |
0,671±0,046 |
0,480±0,0411 |
0,625±0,0141,2 |
0,282±0,0321,3 |
|
Общая ЩФ (мкмоль/ч·л) |
0,292±0,08 |
0,468±0,062 |
0,69±0,21 |
1,56±0,191 |
1,30±0,041,2 |
1,89±0,411 |
1,71±0,071 |
1,67±0,061,4 |
1,79±0,191 |
|
ТЩФ (мкмоль/ч·л) |
- |
- |
0,33±0,033 |
0,39±0,061 |
0,35±0,011 |
0,95±0,161,3 |
0,33±0,081 |
0,56±0,061,2,4 |
0,62±0,051,4 |
1 – Р ≤0,05 между одноименными показателями подгрупп относительно нормы.
2 – Р ≤0,05 между подгруппами до 12 недель и 13–16 недель одной группы.
3 – Р ≤0,05 между подгруппами 13–16 недель и 17 и более недель одной группы.
4 – Р ≤0,05 между одноименными подгруппами при угрожающем аборте и при угрожающем аборте с плацентарной недостаточностью.
Рецензенты:
Герасименко Алексей Валентинович, доктор медицинских наук, профессор, директор ГБУЗ РМ «Мордовский республиканский клинический перинатальный центр», г. Саранск.
Балыкова Лариса Александровна, доктор медицинских наук, профессор, зав. кафедрой педиатрии Медицинского института ФГБОУ ВПО «Мордовский государственный университет им. Н.П. Огарева», г. Саранск.
Библиографическая ссылка
Ляличкина Н.А., Пешев Л.П., Щукина Л.П. ПРОГНОСТИЧЕСКИЕ МАРКЕРЫ ПЛАЦЕНТАРНОЙ НЕДОСТАТОЧНОСТИ ПРИ УГРОЖАЮЩЕМ АБОРТЕ // Современные проблемы науки и образования. 2012. № 6. ;URL: https://science-education.ru/ru/article/view?id=7495 (дата обращения: 27.05.2026).



