Разработка гибкой энерго- и ресурсосберегающей технологии концентрированных фосфатов натрия [2-4] с обеспечением регулирования размеров и габитуса получаемых кристаллов вещества и фильтрующих свойств кристаллов.
Экспериментальная часть
Для исследования свойств растворов фосфатов натрия получали нейтрализацией 73%-ной фосфорной кислоты едким натром до достижения нейтрализации первого, второго или третьего иона водорода. Полученные растворы разбавляли до достижения необходимой концентрации. Кристаллизацию проводили в реакторе, охлаждаемом водой. Скорость охлаждения раствора регулировали в пределах 1-12 град/час изменением температуры (5-28 °С) и интенсивности подачи охлаждающей воды. Выпавшие кристаллы отделяли на воронке Бюхнера, сушили, определяли грансостав (рассеиванием), анализировали на содержание пентаоксида фосфора фотоколориметрически [5]. Величину пересыщения определяли по разности концентраций раствора в момент осаждения первых кристаллов соли и в момент исчезновения кристаллов при нагреве системы. Вязкость растворов определяли термостатированным вискозиметром ВПЖ-2.
Результаты и их обсуждения
Результаты исследования представлены на рисунках 1-3. На рисунке 1 номер линии пересыщения соответствует скорости охлаждения раствора (град/час).
Как видно из рисунка 1, величина пересыщения в растворах фосфатов определяется как скоростью охлаждения растворов, так и степенью замещения ионов водорода в фосфате ионом натрия. В растворах мононатрийфосфата (МНФ), насыщенных безводной солью, величина пересыщений в растворе максимальна и равна 0,8-2,6% масс. С увеличением скорости охлаждения с 1 до 5 град/час величина пересыщения в растворе, насыщенном МНФ, возрастает в 1,95-2 раза. При этом с уменьшением концентрации насыщенного раствора в ходе политермической кристаллизации безводного МНФ по мере движения фигуративной точки равновесной жидкой фазы от перитектики d2 к d1 величина пересыщения раствора возрастает в 1,7-1,75 раза одновременно с ухудшением условий диффузии ионов в растворе по мере роста вязкости насыщенных растворов (рис. 2).
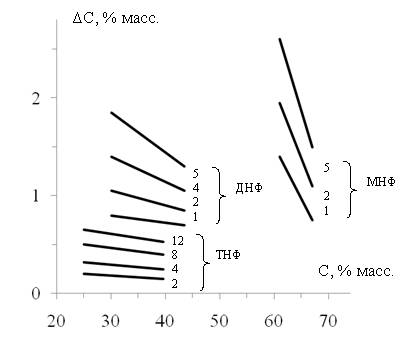
Рис. 1. Влияние концентрации насыщенных растворов (С, % масс.) на пересыщение (ΔС, % масс.).
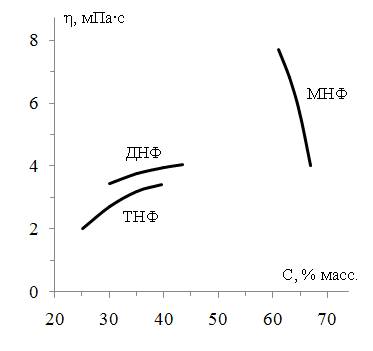
Рис. 2. Влияние концентрации насыщенных растворов (С, % масс.) на их вязкость (η, мПа·с).
В этом случае ухудшению диффузии способствует одновременно снижение температуры, рост вязкости растворов и уменьшение концентрации раствора. Поэтому для растворов, насыщенных безводным мононатрийфосфатом, из-за относительно меньшей скорости зародышеобразования диаметр получаемых кристаллов относительно больше, чем у динатрийфосфата или тринатрийфосфата (рис. 3).
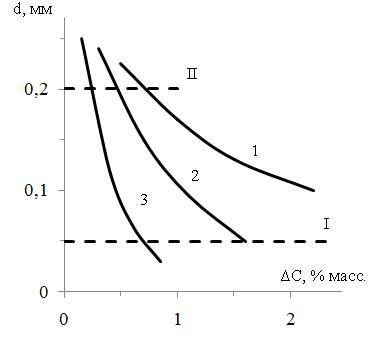
Рис. 3. Влияние пересыщений раствора (ΔС, % масс.) на средний диаметр кристаллов (d, мм) при кристаллизации: 1 - безводного МНФ; 2 - семиводного ДНФ; 3 - десятиводного ТНФ.
В растворах двузамещенного фосфата натрия (ДНФ) достигаемые пересыщения в ходе политермической кристаллизации семиводного динатрийфосфата ниже (0,8-1,85% масс.), чем в растворах МНФ, но выше, чем при осаждении трехзамещенного фосфата (ТНФ) (0,15-0,6% масс.). В растворах ДНФ с увеличением скорости охлаждения раствора с 1 до 5 град/час величина пересыщения в растворе возрастает в 1,8-2,3 раза.
По мере осаждения соли при политермической кристаллизации семиводного динатрийфосфата вязкость раствора понижается. Это способствует уменьшению значений пересыщений в растворах по сравнению с растворами, насыщенными мононатрийфосфатом. Поэтому при равных значениях пересыщений, как видно из рисунка 3, средний диаметр выпавших кристаллов семиводного динатрийфосфата имеет меньшие значения, чем диаметр кристаллов мононатрийфосфата.
В растворах, насыщенных десятиводным тринатрийфосфатом, достигаемые пересыщения значительно ниже. Этому способствует более интенсивное снижение вязкости растворов от начала процесса до завершения кристаллизации и одновременное повышение доли свободной воды в менее концентрированных растворах тринатрийфосфата. Величина пересыщения составляет 0,14-0,63% масс. при скорости охлаждения растворов 1-12 град/час. В результате при равных пересыщениях средний диаметр образующихся кристаллов десятиводного тринатрийфосфата меньше, чем у семиводного динатрийфосфата и безводного мононатрийфосфата.
Как показано Тодесом О.М. [6], изменение условий в системе по мере охлаждения раствора способствует волнообразному изменению пересыщения с амплитудой от 0 до максимально достигаемой величины и частотой, определяемой преимущественно вязкостью раствора. Условия кристаллизации разбивают на три области [6]:
- область активного роста зародышей до достижения размеров устойчивости (30-50 мкм);
- область активной коагуляции зародышей с образованием стабильных кристаллов (100-200 мкм);
- область роста кристаллов.
На рисунке 3 эти области отграничиваются линиями I и II.
При кристаллизации безводного мононатрийфосфата практически весь интервал изменения концентрации раствора в жидкой фазе приходится на область формирования кристаллов стабильного размера. При этом область оптимума скоростей охлаждения приходится на 1,5-3 град/час.
При осаждении семиводного динатрийфосфата область формирования кристаллов стабильного размера также охватывает практически весь интервал изменения концентрации раствора, насыщенного данным кристаллогидратом. Но при скоростях охлаждения 3 и более град/час в конце процесса появляется возможность образования новых зародышей кристаллов, которые из-за дефицита времени для их роста (200-300 с) не достигают размера частиц коагуляции (100 мкм). Поэтому в выделяемом продукте появляется относительно мелкая фракция кристаллов (< 50 мкм). При кристаллизации динатрийфосфата скорость охлаждения раствора целесообразно ограничить в пределах 2-3 град/час.
При выпадении в осадок кристаллов десятиводного тринатрийфосфата область оптимума скорости охлаждения раствора значительно шире и составляет до 8 град/час.
Заключение
Оптимальными скоростями охлаждения являются для выделения: безводного мононатрийфосфата 1,5-3 град/час; семиводного динатрийфосфата 2-3 град/час; десятиводного тринатрийфосфата до 8 град/час.
По результатам исследования разработана гибкая энерго- и ресурсосберегающая технология фосфатов натрия различной замещенности и гидратности с использованитем рецикла маточных растворов.
Рецензенты:
Луконин В.П., д.техн.н., профессор, генеральный директор Федерального государственного унитарного предприятия «Научно-исследовательский институт химии и технологии полимеров им. акад. В.А. Каргина с опытным заводом» (ФГУП «НИИ Полимеров»), г. Дзержинск.
Ширшин К.В., д.хим.н., профессор, заместитель директора Федерального государственного унитарного предприятия «Научно-исследовательский институт химии и технологии полимеров им. акад. В.А. Каргина с опытным заводом» (ФГУП «НИИ Полимеров») по научной работе, г. Дзержинск.
Библиографическая ссылка
Никандров М.И., Никандров И.С. ПЕРЕСЫЩЕНИЕ В РАСТВОРАХ ПРИ КРИСТАЛЛИЗАЦИИ ФОСФАТОВ НАТРИЯ // Современные проблемы науки и образования. 2012. № 4. ;URL: https://science-education.ru/ru/article/view?id=6507 (дата обращения: 01.05.2026).



