Индолиленаминокарбонильные соединения используются в качестве исходных в реакции циклизации для получения трициклических гетероароматических структур - пирролохинолинов с различным сочленением колец [1,2].
Однако было сообщено [3], что енаминокетоны, образованные из 2,5-диметил-, 1,2,3-триметил-, 5-метил-2-фенил-, 1,5-диметил-2-фенил-6-аминоиндолов и β-дикетонов, ни в кислой среде, ни термически не превращаются в соответствующие пирролохинолины.
Целью настоящей работы является дополнительное исследование поведения (2,5-диметилиндолил-6-), (1,2,5-триметилиндолил-6-), (5-метил-2-фенилиндолил-6-), (1,5-диметил-2-фенилиндолил-6-)енаминокетонов в различных кислотных, термических условиях и выяснение причин их аномального поведения.
Материалы и методы исследования
Спектры ЯМР 1Н в трифторуксусной кислоте записаны на приборе JNM-ECX400. Квантово-химические расчеты эффективных зарядов на атомах молекул 1-16 проведены ограниченным методом Хартри-Фока в параметризации полуэмпирического метода РМ3 из пакета прикладных программ GAMESS. Контроль за ходом реакции осуществляли с помощью ТСХ на пластинках Silufol UV-254 в системах бензол-этилацетат, этилацетат-метанол в различных соотношениях.
Общая методика попыток циклизации в присутствии хлорида цинка (А)
Смесь енаминокетона и хлорида цинка (в десятикратном избытке) нагревают в течение 0,5 часа и более длительное время при температуре 140-145 ◦С. После этого реакционную массу обрабатывают разбавленным (10-12 %) водным аммиаком. Осадок отфильтровывают, промывают теплой водой и подвергают хроматографическому анализу с помощью ТСХ.
Общая методика попыток циклизации в трифторуксусной и серной кислотах (Б)
Енаминокетон нагревают в десятикратном избытке кипящей трифторуксусной или в концентрированной серной (80-100оС) кислоте в течение 1 часа и более длительное время. После этого охлажденную реакционную смесь выливают в 12 % водный аммиак со льдом. Осадок отфильтровывают, промывают водой и подвергают хроматографическому анализу с помощью ТСХ.
Общая методика попыток термической циклизации (В)
Енаминокетон нагревают в кипящем дифениле в течение 0,5 часа или более длительное время. После этого еще теплую реакционную смесь выливают в петролейный эфир. Осадок отфильтровывают, многократно промывают горячим петролейным эфиром и подвергают хроматографическому анализу с помощью ТСХ.
Результаты и их обсуждение
Ранее нами было сообщено, что енаминокетоны, полученные из замещенных 6-аминоиндолов со свободным положением С(3) индола не удается превратить в пирролохинолины [3].

При проведении дополнительных исследований по поведению енаминокетонов 1-8 в реакции циклизации под действием различных кислотных агентов (CF3COOH, H2SO4, ZnCl2), а также термически кипячением в дифениле, нами не зафиксировано образование (даже следовых количеств) пирролохинолинов не только для N-Ме замещенных енаминов 1-4, но и для соединений 5-8. В реакционной смеси после проведения реакции обнаруживаются лишь исходные соединения и продукты их распада, а в случае использования хлорида цинка в качестве циклизующего агента - окрашенные полимерообразные продукты (не идентифицировались).
Возможную циклизацию молекул соединений 1-8 можно рассматривать как электрофильную атаку атома С(13) по атому С(7). Однако в условиях проводимой циклизации молекулы 1-8 в результате протонирования могут иметь иную пространственную и электронную структуру. На рисунке 1 приведены возможные системы, имеющиеся или образующиеся в выше приведенных условиях в реакционной смеси.
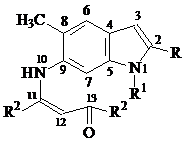
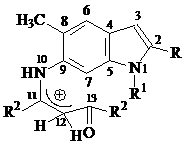
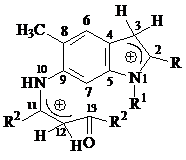
а б в
Рисунок 1
Реакция циклизации должна протекать под зарядовым контролем и определяется величинами эффективных зарядов на взаимодействующих атомах.
В таблицах 1-6 представлены результаты расчета эффективных зарядов (в ат. ед.) на атомах молекул различно протонированных соединений 1-16 (системы а, б, в, г, д, е).
Таблица 1. Значения величин эффективных зарядов на отдельных атомах в системе а
|
Соедин. |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
|
С(3) |
-0,154 |
-0,141 |
-0,157 |
-0,144 |
-0,148 |
-0,136 |
-0,147 |
-0,135 |
|
С(7) |
-0,129 |
-0,133 |
-0,135 |
-0,139 |
-0,129 |
-0,131 |
-0,131 |
-0,135 |
|
С(12) |
-0,207 |
-0,206 |
-0,211 |
-0,211 |
-0,206 |
-0,205 |
-0,209 |
-0,209 |
|
С(13) |
0,339 |
0,339 |
0,390 |
0,390 |
0,338 |
0,338 |
0,389 |
0,389 |
Как видно из данных таблицы 1, атом С(7) в молекулах соединений 1-8 (система а) имеет отрицательный эффективный заряд, величина которого меняется в интервале 0,129-0,135 в зависимости от заместителя R.
Атом С(13) в тех же молекулах имеет положительный эффективный заряд, величина которого меняется в интервале 0,339-0,389.
Таким образом, существуют достаточные зарядовые предпосылки для протекания реакции циклизации в рамках электрофильной атаки. Однако экспериментально установлено, что в рассмотренных молекулах, несмотря на благоприятное зарядовое распределение на взаимодействующих атомах, реакция кислотной циклизации не реализуется.
Для объяснения имеющихся экспериментальных данных, учитывая, что реакция циклизации исследовалась в кислой среде, рассмотрена возможность протонирования атома С(12), который имеет, как следует из данных таблицы 1, самый значительный отрицательный эффективный заряд. На рисунке 1 также представлены рассмотренные монопротонированные формы молекул соединений 1-8 (система б).
Таблица 2. Значения величин эффективных зарядов на отдельных атомах в системе б
|
Соедин. |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
|
С(3) |
-0,174 |
-0,173 |
-0,170 |
-0,170 |
-0,167 |
-0,167 |
-0,165 |
-0,165 |
|
С(7) |
-0,034 |
-0,033 |
-0042 |
-0,042 |
-0,034 |
-0,032 |
-0,043 |
-0,047 |
|
С(12) |
-0,177 |
-0,176 |
-0,199 |
-0,195 |
-0,178 |
-0,177 |
-0,197 |
-0,196 |
|
С(13) |
0,293 |
0,293 |
0,350 |
0,353 |
0,293 |
0,293 |
0,353 |
0,357 |
Как видно из данных таблицы 2, на атоме С(7) протонированных по С(12) молекул происходит значительное уменьшение величины отрицательного эффективного заряда. Интервал изменений заряда в зависимости от заместителей R равен 0,032-0,047. В тоже время наблюдается не только уменьшение, а даже некоторое увеличение величин эффективного отрицательного заряда на атоме С(3). Интервал изменения величин заряда в зависимости от заместителей составляет 0,165-0,174 ат. ед. Такое значительное различие в величинах эффективных зарядов на атомах С(7) и С(3) открывает возможность дополнительного протонирования пиррольного кольца по атому С(3) в кислотной среде исследуемой реакции, но не электрофильного замыкания пиридинового цикла с участием атомов С(7) , С(13). Следует отметить, что величины положительного эффективного заряда на атоме С(13) молекул незначительно отличаются от аналогичных величин в соответствующих непротонированных молекулах. На рисунке 1 также представлены дважды протонированные формы молекул соединений 1-8 (система в).
Таблица 3. Значения величин эффективных зарядов на отдельных атомах в системе в
|
Соедин. |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
|
С(3) |
-0,067 |
0,072 |
-0,064 |
-0,068 |
-0,070 |
-0,063 |
-0,065 |
-0,060 |
|
С(7) |
0,007 |
-0,014 |
-0,002 |
-0,020 |
0,014 |
-0,011 |
0,004 |
-0,010 |
|
С(12) |
-0,199 |
-0,197 |
-0,215 |
-0,211 |
-0,200 |
-0,198 |
-0,213 |
-0,209 |
|
С(13) |
0,305 |
0,303 |
0,365 |
0,365 |
0,306 |
0,304 |
0,368 |
0,369 |
Как видно из данных таблицы 3, происходит дальнейшее уменьшение величины отрицательного эффективного заряда на атоме С(7) молекул. Двойное протонирование исходных молекул незначительно изменяет величину положительного эффективного заряда на атоме С(13).
Нами также рассмотрено протонирование карбонильного кислорода в рассматриваемых молекулах. На рисунке 2 представлены такие дважды протонированные формы рассматриваемых молекул (система г).
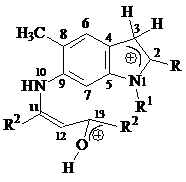

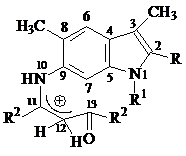
г д (9-16) е (9-16)
Рисунок 2
Таблица 4. Значения величин эффективных зарядов на отдельных атомах в системе г
|
Соедин. |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
|
С(3) |
-0,063 |
-0,068 |
-0,060 |
-0,065 |
-0,066 |
-0,060 |
-0,061 |
-0,057 |
|
С(7) |
0,013 |
-0,006 |
0,004 |
-0,016 |
0,015 |
-0,006 |
0,004 |
-0,008 |
|
С(12) |
-0,377 |
-0,375 |
-0,405 |
-0,402 |
-0,382 |
-0,378 |
-0,407 |
-0,401 |
|
С(13) |
0,240 |
0,234 |
0,307 |
0,298 |
0,231 |
0,224 |
0,302 |
0,303 |
Как видно из данных таблицы 4, эффективные заряды на атоме С(7) молекул соединений 1-8 (система г) либо практически не имеют отрицательного заряда, либо приобретают небольшой положительный заряд, по аналогии с дважды С(3) и С(12) протонированными формами.
Таким образом, проведение циклизации по механизму электрофильной атаки молекул соединений 1-8 в трифторуксусной и серной кислотах приводит к протонированию атомов С(3) и енаминного фрагмента, что существенно уменьшает величину отрицательного эффективного заряда на атоме С(7) и делает протекание циклизации по механизму электрофильной атаки маловероятным. О двойном протонировании индолиленаминокетонов свидетельствуют и спектры ЯМР 1Н соединений 1-8 в трифторуксусной кислоте, в которых отсутствует характерный сигнал Н-С(3) в области 6 м.д. и резкое уменьшение интегральной интенсивности сигнала винильного протона в области 5,2 м.д. Блокирование возможности протонирования атома С(3) путем введения в данное положение заместителя, например, метильной группы, обеспечивает протекание циклизации с образованием соответствующих пирролохинолинов [2]. Нами проведены также квантово-химические расчеты молекул енаминокетонов 9-16 (рисунок 2, система д) с метилированным бета-положением пиррольного кольца (радикалы R,R1,R2 такие же, как и в соединениях 1-8 ).
Как видно из таблицы 5, введение метильной группы в положение С(3) енаминокетона (система д) приводит к существенному уменьшению величин отрицательного эффективного заряда на атоме С(3), при этом величины эффективных зарядов на атомах С(7), С(12) практически остаются без изменения. Следовательно, первичное протонирование структур 9-16 реализуется, как и аналогов без метильной группы 1-8, с участием енаминокетонного фрагмента (система е).
Таблица 5. Значения величин эффективных зарядов на отдельных атомах в системе д
|
Соедин. |
9 |
10 |
11 |
12 |
13 |
14 |
15 |
16 |
|
С(3) |
-0,131 |
-0,111 |
-0,1338 |
-0,112 |
-0,123 |
-0,104 |
-0,123 |
-0,102 |
|
С(7) |
-0,129 |
-0,134 |
-0,135 |
-0,140 |
-0,129 |
-0,133 |
-0,131 |
-0,136 |
|
С(12) |
-0,207 |
-0,207 |
-0,210 |
-0,211 |
-0,206 |
-0,205 |
-0,209 |
-0,209 |
|
С(13) |
0,339 |
0,339 |
0,389 |
0,390 |
0,338 |
0,338 |
0,389 |
0,389 |
Таблица 6. Значения величин эффективных зарядов на отдельных атомах в системе е
|
Соедин. |
9 |
10 |
11 |
12 |
13 |
14 |
15 |
16 |
|
С(3) |
-0,140 |
-0,132 |
-0,137 |
-0,130 |
-0,136 |
-0,127 |
-0,136 |
-0,125 |
|
С(7) |
-0,036 |
-0,036 |
-0,044 |
-0,046 |
-0,035 |
-0,036 |
-0,043 |
-0,050 |
|
С(12) |
-0,177 |
-0,176 |
-0,198 |
-0,195 |
-0,178 |
-0,177 |
-0,196 |
-0,196 |
|
С(13) |
0,293 |
0,293 |
0,350 |
0,352 |
0,293 |
0,294 |
0,353 |
0,357 |
Из таблицы 6 видно, что в результате протонирования значительно уменьшаются величины эффективного заряда на атоме С(3) и наблюдается незначительное увеличение величин эффективного заряда на атоме С(7). В связи с этим, а также учитывая пространственный фактор метильной группы, возможности последующего протонирования по атому С(3) снижаются и реализуется конкурирующая реакция циклизации с образованием пиридинового цикла.
Что касается условий циклизации с использованием в качестве катализатора хлорида цинка, то, по-видимому, в этом случае электрофильная атака активированного атома углерода карбонильной группы енаминокетонного фрагмента реализуется по положению с наибольшим отрицательным эффективным зарядом С(3) другой молекулы индолиленаминокетона с образованием окрашенных полимерообразных продуктов. В случае термолиза электрофильная активность С(13) недостаточна для замыкания пиридинового цикла и никакого электрофильного превращения не происходит, а протекает лишь разложение енамина.
Выводы
Из результатов проведенных исследований следует, что (2,5-диметилиндолил-6-), (1,2,5-триметилиндолил-6-), (5-метил-2-фенилиндолил-6-), (1,5-диметил-2-фенилиндолил-6-)енаминокетоны не могут быть использованы для получения соответствующих пирролохинолинов. Дано объяснение аномального поведения изученных индолиленаминокетонов в условиях электрофильной реакции с использованием в качестве катализатора хлорида цинка, трифторуксусной и серной кислот.
Работа выполнена в рамках реализации ФЦП «Научные и научно-педагогические кадры инновационной России», (ГК П840).
Рецензенты:
- Климов Е.С., д.х.н., профессор, зав. кафедрой «Химия» ФГБОУ ВПО «Ульяновский государственный технический университет», г. Ульяновск.
- Пржевальский Н.М., д.х.н., профессор кафедры физической и органической химии Российского государственного аграрного университета - МСХА имени К. А. Тимирязева, г. Москва.
Библиографическая ссылка
Ямашкин С.А., Томилин О.Б., Бояркина О.В., Позднякова О.В. ИССЛЕДОВАНИЕ (2,5-ДИМЕТИЛ-, 1,2,5-ТРИМЕТИЛ-, 5-МЕТИЛ-2-ФЕНИЛ-, 1,5-ДИМЕТИЛ-2-ФЕНИЛИНДОЛИЛ-6-)ЕНАМИНОКЕТОНОВ В РЕАКЦИЯХ ЦИКЛИЗАЦИИ // Современные проблемы науки и образования. 2012. № 1. ;URL: https://science-education.ru/ru/article/view?id=5404 (дата обращения: 21.05.2026).



