Предметом пристального изучения, после открытия их специфического биологического действия, стали некоторые сахарозаменители (неусваиваемые), имеющие особую ценность для здоровья человека. Было установлено, что они являются пребиотиками - веществами, которые не гидролизуются и не всасываются в верхней части желудочно-кишечного тракта, а поступают в нижние его отделы и способствуют развитию полезных бактерий, обитающих в толстом кишечнике. Как все пребиотики, эти вещества регулируют кишечную микрофлору, индуцируют полезные эффекты как на уровне желудочно-кишечного тракта, так и организма в целом, способствуя поддержанию иммунной системы человека [4,8].
Одно из таких веществ - изомальтулоза (6-О-α-D-глюкопиранозид-D-фруктоза), известная как натуральный заменитель сахара, присутствующий в меде, соке сахарного тростника. За рубежом этот углевод рекомендуют использовать в рационе питания людей, страдающих сердечно-сосудистыми заболеваниями, ожирением, атеросклерозом, а также при диабете.
Сотрудниками кафедры микробиологии и биохимии ФГБОУВПО «ВГТА» была разработана биотехнология изомальтулозы с применением иммобилизованных высокоактивных бактерий Erwinia rhapontici, основанная на реакции биотрансформации сахарозы в изомальтулозу, катализируемой ферментом этого продуцента - изомальтулозосинтазой [6].
В литературе отсутствуют конкретные данные о способности бифидобактерий развиваться на средах с изомальтулозой, однако имеются сведения о ее пребиотических свойствах.
Как известно, бифидобактерии относятся к наиболее значимым представителям нормобиоценоза [3], поэтому в качестве объекта исследования был использован типовой вид рода - Bifidobacterium bifidum: анаэробные микроорганизмы, морфологически представляющие собой крупные грамположительные неспорообразующие палочки с раздвоенными концами, способные к полиморфизму. Среди неусваиваемых углеводов инулин и трегалоза являются известными пребиотиками.
Цель настоящего исследования состояла в изучении роста и развития бифидобактерий на средах, содержащих изомальтулозу, полученную в результате биотрансформации сахарозы с применением иммобилизованных бактериальных клеток рода Erwinia в условиях in vitro и типа взаимодействия бифидобактерий с основным представителем микрофлоры желудочно-кишечного тракта - кишечной палочкой.
Материал и методы исследования
Объектом для иммобилизации служили факультативно-анаэробные бактерии Erwinia rhapontici штамм В-9292 (ВКПМ, г. Москва). Для поддержания и выращивания E. rhapontici использовали мясо-пептонный агар. Культивирование бактерий проводили на среде следующего состава (г/дм3): пептон - 10; дрожжевой экстракт - 5; NaCl - 10; сахароза - 40. Культуру выращивали в периодических условиях в течение 3 суток при температуре 28-30 °С при рНисх 7,0±0,1. Клетки осаждали центрифугированием при 8000 g в течение 15 минут, промывали трис-HCl буфером 0,05 М, рН 6,0. Об активности фермента судили по изменению концентрации изомальтулозы, полученной в результате трансформации сахарозы и выражали в Ед/см3. Количество изомальтулозы определяли по методу Сомоджи-Нельсона. Иммобилизацию живых бактериальных клеток проводили, как описано в [2]. Раствор, содержащий изомальтулозу, получали путем биотрансформации сахарозы с последующим концентрированием и выделением.
Для подтверждения пребиотических свойств изомальтулозы осуществляли культивирование бактерий Bifidobacterium bifidum in vitro на средах с различными источниками углерода. В опытах использовались бакпрепараты B. bifidum. Препарат «Бифидобактерин сухой» предварительно растворяли в питательной среде и активизировали при температуре 37 - 38 °С в течение 24 ч. Затем данный препарат вносили в подготовленные для культивирования питательные среды из расчета 5 доз на 1 л среды. Выращивание микроорганизмов проводили в анаэробных условиях на модифицированной среде Блаурокка. Для определения эффективности действия различных углеводов на рост микроорганизмов B. bifidum в питательную среду поочередно включали изомальтулозу, лактозу, инулин, фруктозу, трегалозу. Углеводы вносили в количестве 10 % по углероду в среду следующего состава: пептон - 10; NaCl - 5; агар-агар - 0,75; цистеин солянокислый - 0,1; печеночный отвар, рН 7,5. Подсчет клеток бифидобактерий проводили на фиксированных окрашенных мазках по методу Виноградского-Шульгиной-Брига [7].
Микроскопирование культур проводили с помощью светового микроскопа Микмед - 1 (ОАО «Ломо» Россия). Фотографии получены с использованием цифровой камеры - окуляра DCM-130 (1300K pixels, USB 2) для микроскопа, программное обеспечение «ScopePhoto».
Опыты проводили в 3 кратной биологической повторности. В таблицах и на рисунках приведены данные типичных опытов, где каждое значение есть среднее арифметическое. При математической обработке использовали статистический критерий Стьюдента.
Результаты исследования и их обсуждение
Изучение влияния изомальтулозы на рост и развитие бифидобактерий в сравнении с другими углеводами.
Данные по динамике роста B. bifidum на различных источниках углерода показали, что микроорганизмы способны к росту на всех испытанных вариантах сред. Максимальное накопление биомассы наблюдалось к 48 ч процесса культивирования бактерий. Однако внесение того или иного источника углерода оказывало различное влияние на скорость и интенсивность роста бифидобактерий. Наибольшая физиологическая активность культуры проявлялась при внесении в среду изомальтулозы и лактозы (рис.1).
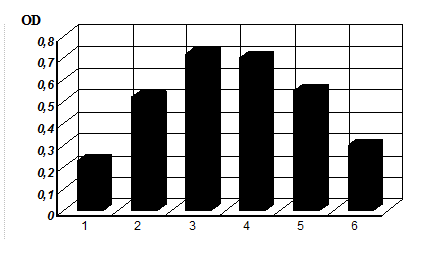
Рис. 1. Нефелометрическое определение биомассы B. bifidum на различных углеводных средах (24 ч). 1 - без углевода, 2 - инулин, 3 - изомальтулоза, 4 - лактоза, 5 - трегалоза, 6 - фруктоза. OD - показатель оптической плотности
Так, к 24 ч культивирования микроорганизмов количество биомассы на среде с изомальтулозой было в 2 раза больше по сравнению с инулинсодержащей средой и в 3 раза больше по сравнению с биомассой в контроле (среда без углевода). Это не противоречит литературным данным, которые указывают, что бифидобактерии потребляют глюкозу, галактозу, большое число олигосахаридов, в том числе фруктоолигосахариды, а из полисахаридов только инулин [5]. Анализ результатов по подсчету клеток B. bifidum на фиксированных препаратах также указывал на интенсификацию роста и развития бифидокультуры на среде с содержанием изомальтулозы и лактозы (табл. 1).
Таблица 1. Изменение биомассы бифидобактерий в зависимости от источника углерода (по количеству клеток на фиксированных препаратах)
|
τ, ч |
Вносимые углеводы |
|||||
|
без углевода |
изомальтулоза |
лактоза |
трегалоза |
инулин |
фруктоза |
|
|
6 |
2·105 |
6·109 |
6·109 |
4·108 |
3·108 |
4·107 |
|
12 |
8 ·105 |
2·1010 |
2·1010 |
6·109 |
7·108 |
8·107 |
|
24 |
2·106 |
3·1011 |
2·1011 |
1·1010 |
9·109 |
4·108 |
|
36 |
3·107 |
7·1011 |
7·1011 |
8·1010 |
5·1010 |
1·109 |
|
48 |
7·107 |
9·1011 |
9·1011 |
2·1011 |
8·1010 |
5·1010 |
Как известно, бифидобактерии обладают способностью проявлять полиморфизм, при этом степень полиморфности зависит от условий выращивания культуры, в чистых культурах они более полиморфны. Так, в неблагоприятных условиях (неподходящая кислотность среды, недостаток питательных компонентов среды, присутствие кислорода) они способны образовывать разбухшие инволюционные, шаровидные формы. В связи с этим, представляло интерес изучить изменение морфологических признаков исследуемых бактерий при росте на средах с различными углеводами.
Как видно на рис. 2, B. bifidum представляют собой в динамике роста неспорообразующие палочки, зернистые, проявляющие тенденцию к образованию цепочек на всех средах. В контроле (а) появляется много гранулированных форм, которые можно принять за кокки. Шаровидные клетки, появляющиеся в результате отсутствия в среде компонентов, необходимых для нормального синтеза бактериальных клеточных стенок, не образуются, однако происходит ветвление, что свидетельствует о неполноценности состава питательной среды.



а) б) в)
Рис. 2. Интенсивность роста B. bifidum на средах с различными углеводами (увеличение 1350 раз);
а) среда без углевода; б) среда с инулином; в) среда с изомальтулозой
Наиболее интенсивное развитие типичных форм отмечено на среде с изомальтулозой (в). Установлено, что на средах с этими углеводами бактерии имели четкую форму палочек, соединенных в цепочки или палочек с раздвоением на концах. На среде, содержащей инулин, клетки микроорганизма имели форму палочек, соединенных в более длинные и тонкие цепочки.
Интенсивность метаболических процессов у бифидобактерий контролировали по изменению рН среды, что служит показателем трансформации сахаров в органические кислоты как конечные продукты метаболизма. Установлено, что изменение величины рН коррелирует с ростом и развитием культуры бактерий (рис. 3).
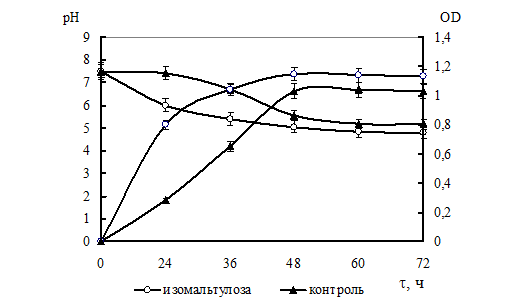
Рис. 3. Динамика изменения рН среды культивирования и интенсивности роста B. bifidum на среде с изомальтулозой. OD - показатель оптической плотности, τ - продолжительность процесса
Отмечено, что наиболее интенсивное снижение рН (до 6,0, 6,3 и 6,5) наблюдалось при сбраживании изомальтулозы, лактозы и трегалозы, соответственно, к 24 ч процесса культивирования. На среде с инулином, фруктозой и в контроле к этому времени значение рН изменилось незначительно. Максимальное снижение рН среды (4,8 - 5,8) наблюдалось на всех вариантах сред к 48 - 60 ч культивирования.
Изучение типа взаимодействий Bifidobacterium bifidum с Escherichia coli.
Как известно, микроорганизмы, составляющие основу микрофлоры толстого кишечника здорового человека, представлены полезными бифидобактериями и лактобактериями, а также условно-патогенными микробами - кишечной палочкой с нормальными ферментативными свойствами. Именно эти микроорганизмы обеспечивают устойчивость колонии и предотвращают заселение толстого кишечника посторонними микробами.
Однако вопрос о диагностической ценности исследований микрофлоры толстого кишечника в настоящее время широко дискутируется. В России большинство лабораторий при диагностике дисбактериоза руководствуется МР № 10-11/31 «Применение бактерийных биологических препаратов в практике лечения больных кишечными инфекциями. Диагностика и лечение дисбактериоза кишечника» (Москва, 1986). Количество нормируемых групп микроорганизмов кишечника человека варьируется в разных документах от 10 до 22. Наибольшей детализации подвергается кишечная палочка - Escherichia coli. Рекомендуется определять общее количество эшерихий, с четко выраженной ферментативной активностью, со сниженной ферментативной активностью, лактозонегативные, гемолитические, неподвижные, индолнегативные, маннитнегативные и т.д. Согласно диагностическим критериям, приведенным в МР 10-11/31, содержание бифидобактерий в норме должно составлять 108-1010 кл/г, кишечных палочек с нормальной ферментативной активностью 107-108 кл/г (табл. 2.4). Такой симбиоз микроорганизмов достаточно стабилен и не допускает развития в толстом кишечнике других микроорганизмов.
В связи с этим были проведены исследования по изучению симбиотических отношений следующих микроорганизмов: B. bifidum - основного представителя нормобиоценоза кишечника человека и E. coli - представителя условно-патогенной микрофлоры на средах с различными источниками углевода (изомальтулоза, глюкоза, фруктоза, трегалоза).
Углеводы вносили в полужидкую среду Блаурокка в качестве единственного источника углевода, в контрольной пробе углевод отсутствовал. Среды инокулировали чистыми культурами B. bifidum и E. сoli в количестве, соответствующем показателю нормы. Культивирование микроорганизмов проводили при 37 ° С в течение 48-72 ч.
Как показали исследования, на средах с изомальтулозой и глюкозой обе культуры проявляли максимальную способность к росту (табл.2).
Таблица 2. Интенсивность роста B. bifidum и E. сoli на средах с различными углеводами
|
τ, ч |
Вносимые углеводы |
|||||
|
изомальтулоза |
глюкоза |
фруктоза |
||||
|
B. bifidum |
E. сoli |
B. bifidum |
E. сoli |
B. bifidum |
E. сoli |
|
|
6 |
6·108 |
4·107 |
6·108 |
3·107 |
4·107 |
2·106 |
|
12 |
2·109 |
6·108 |
2·109 |
7·107 |
8·107 |
8·106 |
|
24 |
3·1010 |
1·109 |
4·109 |
9·108 |
4·108 |
2·107 |
|
36 |
7·1010 |
8·109 |
9·109 |
5·109 |
1·109 |
7·107 |
|
48 |
4·1011 |
2·1010 |
9·1010 |
8·109 |
5·1010 |
9·107 |
Однако на средах с трегаллозой, фруктозой плотность популяций снижалась в процессе культивирования, что свидетельствует об ухудшении симбиотических взаимоотношений микроорганизмов в этих вариантах опыта.
Заключение
В результате проведенных исследования установлено, что культивирование бифидобактерий B. bifidum в условиях in vitro на среде с содержанием изомальтулозы отличается высокой активностью их роста, уровнем накопления биомассы, продукцией органических кислот. Выявлено, что при совместном культивировании бифидобактерий B. bifidum и кишечной палочки E. сoli соотношение микроорганизмов соответствует принятым нормам и является достаточно стабильным. Таким образом, изомальтулоза обладает пребиотическими свойствами, что косвенно позволяет рассматривать ее как потенциальный иммуномодулятор организма человека.
Работа выполнялась в рамках федеральной целевой программы «Научные и научно-педагогические кадры инновационной России» на 2009 - 2013 годы, государственный контракт № П1333 от 11.06.2010 г.
Рецензенты:
- Тертычная Т.Н., д.с.-х.н., профессор, профессор кафедры технологии переработки растениеводческой продукци, ФГОУ ВПО «Воронежский государственный аграрный университет» Министерства образования и науки РФ, г. Воронеж.
- Грабович М.Ю., д.б.н., доцент, профессор кафедры биохимии и физиологии клетки, ФГОУ ВПО «Воронежский государственный аграрный университет» Министерства образования и науки РФ, г. Воронеж.
Работа получена 11.11.2011.
nbsp;Библиографическая ссылка
Божко О.Ю., Шуваева Г.П., Корнеева О.С. ИЗУЧЕНИЕ ПРЕБИОТИЧЕСКИХ СВОЙСТВ ЗАМЕНИТЕЛЯ САХАРА ИЗОМАЛЬТУЛОЗЫ В УСЛОВИЯХ IN VITRO // Современные проблемы науки и образования. 2011. № 5. ;URL: https://science-education.ru/ru/article/view?id=4920 (дата обращения: 14.05.2026).



