Введение
Тотальное эндопротезирование тазобедренного сустава (ТЭТС) по праву считается одним из величайших достижений травматологии и ортопедии XX в. – операцией, которая значительно улучшает качество жизни пациентов [1, 2]. Ежегодно выполняется более миллиона таких вмешательств, и прогнозы указывают на неуклонный рост: только в Соединенных Штатах Америки ожидается увеличение числа первичных артропластик на 176% к 2040 г. и на 659% к 2060 г.[3, 4]. Параллельно с этим закономерно возрастает и количество ревизионных вмешательств: согласно данным Национального регистра Великобритании, общий уровень ревизий после первичного эндопротезирования тазобедренного сустава через 13 лет составит 6,8% [5].
Одной из причин увеличения количества ревизионных вмешательств считается перипротезная инфекция (ППИ), которая представляет собой серьезное осложнение после артропластики тазобедренного сустава, частота которой, несмотря на совершенствование профилактических мер, остается стабильной на протяжении последних десятилетий. ППИ входит в тройку основных причин отрицательных результатов после первичного эндопротезирования тазобедренного сустава и главной причиной ранних ревизий (в течение первых двух лет после операции) [6, 7]. При ревизионном эндопротезировании инфекция уже выходит на первое место, составляя 30,2% всех повторных вмешательств, и прогнозируется, что в ближайшие 15 лет эта доля может достигнуть 60%[8, 9].
В целом распространенность ППИ колеблется в пределах 0,5–2,3% [8]. По данным программы VINCat (Каталония, Испания), включающей анализ 189063 операций за 15 лет (2008–2022), частота ППИ после первичного тотального эндопротезирования тазобедренного сустава (ТЭТС) составляет 0,9–1,2% и не демонстрирует значимой тенденции к снижению[10]. Даже при стабильно низкой частоте абсолютное число пациентов с ППИ растет пропорционально увеличению количества выполняемых артропластик [11].
Масштаб экономического бремени впечатляет: лечение ППИ обходится в 3–5,6 раза дороже первичной артропластики [12]. По оценкам европейских исследователей, только за 2019 г. в 30 странах Европы было зарегистрировано 20416 случаев ППИ после первичного эндопротезирования тазобедренного и коленного суставов, что обошлось системам здравоохранения в сумму более 346млн евро. При этом львиная доля затрат (142млн евро) пришлась на двухэтапные ревизионные вмешательства по поводу ППИ [13]. Стоимость одного страхового случая лечения ППИ в США может достигать 40000–160000 долл. [14].
Современная диагностика ППИ, несмотря на появление новых классификаций (MSIS, ICG, EBJIS, WAIOT), демонстрирующих высокую согласованность между собой (до 90%), все еще оставляет «серую зону» – примерно 5% пациентов с вялотекущими инфекциями, которые трудно верифицировать [15].
Лечение же требует не просто грамотно подобранной хирургической тактики, а глубокого понимания процессов формирования биопленки и дифференцированного подхода: от дебридмента с сохранением имплантата до одно- и двухэтапных ревизионных вмешательств [16]. Таким образом, ППИ представляет собой мультидисциплинарную проблему, требующую консолидации ортопедов, клинических фармакологов и организаторов здравоохранения.
Цель исследования – на основе анализа современных литературных данных, включая последние рекомендации профильных обществ и данные мировых регистров, представить всесторонний взгляд на эпидемиологию, факторы риска, диагностику и современные алгоритмы лечения перипротезной инфекции тазобедренного сустава.
Материал и методы исследования
Поиск актуальной литературы проводился в базах данных Scopus, PubMed, Web of Science. Применялись следующие ключевые слова и их комбинации: hip, hip joint, arthroplasty, Periprosthetic joint infection (PJI), epidemiology PJI, risk factors PJI, diagnostic PJI, Infection management, Treatment periprosthetic joint infection, DAIR, Revision hip arthroplasty, Single-stage revision hip arthroplasty, Two-stage revision hip arthroplasty.
На начальном этапе было проанализировано 167 источников литературы. По результатам анализа полнотекстовых статей, проверки их релевантности задачам данного обзора, в окончательный вариант вошло 49 работ, наиболее точно отвечавших на вопросы эпидемиологии, факторов риска, а также лечения перипротезной инфекции. Временной диапазон поиска литературы – 2007–2025 гг. Публикации старше пяти лет включались в обзор при условии сохранения методологической, клинической значимости и использовались для сопоставления с современными результатами.
Результаты исследования и их обсуждение
Факторы риска развития перипротезной инфекции
Понимание факторов риска ППИ имеет критическое значение для стратификации пациентов, оптимизации предоперационной подготовки и разработки эффективных профилактических стратегий. За последние годы опубликован ряд крупных исследований и метаанализов, позволивших систематизировать знания о предикторах этого осложнения. В обзоре представлен анализ модифицируемых (ИМТ, влияние лекарственных препаратов), немодифицируемых (пол, возраст, коморбидность), а также ряд интраоперационных и микробиологических факторов.
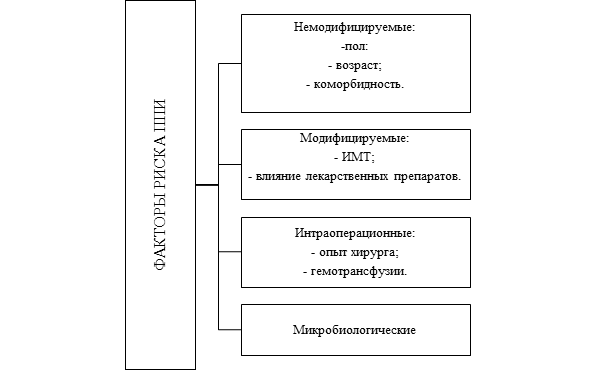
Факторы риска перипротезной инфекции.
Примечание: составлена авторами на основе приведенных источников литературы
Пол и возраст. Мужской пол ожидаемо ассоциируется с повышенным риском развития ППИ. Анализ данных Германского регистра эндопротезирования, включивший 300998 случаев артропластики коленного сустава, продемонстрировал, что мужской пол является независимым фактором риска септических осложнений (отношение рисков [HR] 1,84) [17]. Аналогичная тенденция прослеживается и при эндопротезировании тазобедренного сустава: в исследовании Sumi и соавт. (2024), включавшем 1619 пациентов после гемиартропластики по поводу перелома шейки бедра, доля мужчин в группе ППИ была закономерно выше [18]. Несмотря на вполне очевидный риск развития ППИ у пациентов старшей возрастной группы, в упомянутом исследовании средний возраст пациентов с ППИ был даже несколько ниже (80,4 года), чем в группе сравнения (82,1 года), что может отражать роль других, более значимых факторов, таких как ИМТ, коморбидность, сопутствующие заболевания.
Ожирение. Индекс массы тела (ИМТ)>35 кг/м² является доказанным фактором риска развития ППИ.Предикторами развития инфекции при ожирении считаются технические сложности операции, большая травматизация тканей, увеличение продолжительности операции и нарушение микроциркуляции в подкожно-жировой клетчатке [19]. В исследование Rubin и соавт. были включены 10 работ, охватывающих 46080 операций по эндопротезированию тазобедренного сустава. Было установлено, что у пациентов с патологическим ожирением значительно выше частота перипротезных инфекций по сравнению с пациентами без такового (отношение шансов = 4,332, 95% доверительный интервал [ДИ], 2,943–6,375) [20].
Коморбидный статус. Значение коморбидности в целом подтверждается данными Германского регистра: повышенный индекс коморбидности по Эликсхаузеру (Elixhauser score) ассоциировался с увеличением риска ППИ (HR от 1,18 до 1,56 в зависимости от степени тяжести), тогда как низкие значения этого индекса выступали протективным фактором (HR 0,80)[17].
Системные заболевания и сопутствующие состояния играют ключевую роль в предрасположенности к ППИ. Анализ научной литературы, проведенный Сиваконь и соавт., выделяет целый ряд факторов риска, включаяхроническую сердечную недостаточность, хронические заболевания легких, предоперационную анемию, депрессию, заболевания почек, нарушения легочного кровообращения, психотические расстройства, метастатические опухоли, а также заболевания периферических сосудов и клапанов сердца [21].
Исследование Chang и соавт. подтверждает увеличение частоты развития ППИ у пациентов с сахарным диабетомизаболеваниями периферических сосудов. Данный риск ассоциирован с атеросклеротическим поражением сосудов, что, в свою очередь, ухудшает перфузию тканей в области операционной раны и замедляет заживление [22].
Ревматоидный артрит (РА) является классическим фактором риска инфекционных осложнений. Метаанализ Li и соавт., посвященный риску ППИ, продемонстрировал, что наличие РА увеличивает шансы развития инфекции (ОШ) 2,38 (95% ДИ 1,06–5,38; p=0,04). Это связано как с самой иммуновоспалительной природой заболевания, так и с применяемой иммуносупрессивной терапией [23].
Влияние лекарственных препаратов. Применение системных глюкокортикостероидов закономерно повышает риск развития инфекционных осложнений [24].Исследования George с соавт. показали, что у пациентов, принимавших глюкокортикоиды в дозе более 10мг в день, риск инфекции после артропластики почти вдвое выше, чем у тех, кто не принимал стероиды [25].
Неожиданным, но клинически важным наблюдением Sumi и соавт. стала пролонгация введенияантикоагулянтовв группе ППИ[18]. Авторы связывают это с более высокой частотой послеоперационныхгематом(40% в группе ППИ), которые создают благоприятную среду для бактериальной колонизации. Гематома, по-видимому, выступает промежуточным звеном между приемом антикоагулянтов и развитием инфекции.
Уникальные данные получены при анализе реестра Michigan Arthroplasty Registry Collaborative Quality Initiative (MARCQI), включившего 82110 эндопротезирований тазобедренного сустава. Впервые в литературепредоперационное использование опиоидовбыло идентифицировано как предиктор инфекции после первичного эндопротезирования[26]. Авторы подчеркивают модифицируемый характер этого фактора и возможность его коррекции на этапе предоперационной подготовки.
Интраоперационные факторы. Данные уже озвученного ранее Германского регистра убедительно демонстрируют зависимость исходов оперативного лечения от опыта хирургической бригады. Низкий годовой объем выполняемых операций (менее 25 артропластик в год) ассоциировался с двукратным повышением риска септических осложнений (HR 2,15)[17]. Анализ MARCQI также подтверждает, что годовой объем операций менее 100 случаев является фактором рискаразвития последующей ППИ [26].
Периоперационная гемотрансфузия. Частота гемотрансфузий в группе пациентов с ППИ после артропластики составила 50% против 23,8% в группе без инфекции. Трансфузия может как выступать маркером интраоперационной кровопотери и сложности вмешательства, так и оказывать самостоятельное иммуномодулирующее действие, повышая восприимчивость к инфекции [18].
Микробиологические факторы. За последние два десятилетия произошли существенные изменения в структуре возбудителей ППИ. По данным ретроспективного анализа, стафилококки остаются доминирующими возбудителями (60,6%), однако отмечается неуклонный рост ряда других микроорганизмов: полимикробные инфекции– увеличение доли до 40%, энтерококки– до 7,8%, грамотрицательная флора– 4,7%, культурально-негативные инфекции – 10,6% [27].
Наиболее тревожным трендом является рост инфекций, вызванный микроорганизмами, трудно поддающимися лечению (difficult-to-treat microorganisms). В структуре резистентных форм преобладает метициллин-резистентныйStaphylococcus aureus(MRSA) Наличие MRSA как возбудителя ППИ является мощнейшим предиктором неблагоприятных исходов [28].
Важно также различать микробный пейзаж ППИ после тотального эндопротезирования тазобедренного сустава и после гемиартропластики. В последней группе достоверно чаще выявляются полимикробные ассоциации (53%) и микроорганизмы с множественной лекарственной устойчивостью (41%), что ставит под сомнение эффективность стандартной антибиотикопрофилактики для данной категории пациентов [29].
Таблица1
Значимость факторов риска развития перипротезной инфекции
|
Фактор риска |
Авторы (год) |
Показатель |
Комментарий |
|
Мужской пол |
Szymski et al. (Германский регистр, 2024) |
HR 1,84 |
Независимый фактор риска септических ревизий при артропластике |
|
Ожирение (ИМТ>35 кг/м²) |
Rubin et al. (2025) |
OR 4,332 (2,943–6,375) |
Метаанализ 10 исследований (46080 операций ТБС) |
|
Высокий индекс коморбидности Elixhauser |
Szymski et al. (2024) |
HR 1,18–1,56 (в зависимости от тяжести) |
По сравнению с нулевым индексом (протективный HR 0,80) |
|
Ревматоидный артрит |
Li et al. (2025) |
OR 2,38 (1,06–5,38); p=0,04 |
Метаанализ риска метахронной ППИ |
|
Прием системных глюкокортикостероидов (> 10 мг/день) |
George et al. (2019) |
Риск почти вдвое выше |
Цитируется по Mahase (2019) и George et al. |
|
Предоперационное использование опиоидов |
Gerow et al. (MARCQI, 2024) |
Впервые идентифицировано как предиктор |
Анализ 82110 эндопротезирований ТБС |
|
Прием антикоагулянтов |
Sumi et al. (2024) |
Частота гематом 40% в группе ППИ против низкой в контроле |
Косвенный фактор образования гематом |
|
Периоперационная гемотрансфузия |
Sumi et al. (2024) |
Качественная оценка 50% в группе ППИ против 23,8% в контроле |
Может быть маркером кровопотери или иммуномодулятором |
|
Низкий годовой объем операций (<25 артропластик/год) |
Szymski et al. (2024) |
HR 2,15 |
По данным Германского регистра |
|
Годовой объем операций <100 |
Gerow et al. (MARCQI, 2024) |
Фактор риска |
Подтверждение из американского регистра |
|
Микробиологические: полимикробные инфекции |
Hu et al. (2021) |
Доля выросла до 40% |
Ретроспективный анализ 2392 случаев (2001–2022) |
|
Микробиологические: MRSA |
Egerci et al. (2024) |
Мощный предиктор неблагоприятных исходов |
Преобладает в структуре резистентных форм |
|
Гемиартропластика (по сравнению с ТЭТС) |
Lewis et al. (2025) |
Чаще полимикробные (53%) и с множественной устойчивостью (41%) |
Особая категория пациентов с переломами шейки бедра |
Примечание: составлена авторами на основе приведенных источников литературы
Диагностика перипротезной инфекции: современные стандарты
Диагностика перипротезной инфекции остается одной из наиболее сложных задач в ортопедии. Отсутствие единого стандарта заставляет клиницистов опираться на комбинацию клинических, лабораторных, микробиологических и гистологических признаков [30]. За последние годы произошел значительный прогресс в этой области: от уточнения диагностических критериев ведущими профессиональными обществами до внедрения новых биомаркеров и технологий молекулярной диагностики.
Важной особенностью современного этапа является сосуществование нескольких систем диагностических критериев, что создает определенные сложности как в клинической практике, так и при интерпретации научных данных. Исследование Streck и соавт. наглядно продемонстрировало, что частота диагностируемой ППИ при ревизионном эндопротезировании значимо варьирует в зависимости от применяемой методики [31].
В клинической практике наиболее широко используются критерии следующих организаций:
- Musculoskeletal Infection Society (MSIS)– классические критерии, пересмотренные в 2018 г. с включением альфа-дефенсина и лейкоцитарной эстеразы в качестве минорных критериев[32].
- European Bone and Joint Infection Society (EBJIS)– отличаются более высокой чувствительностью при сохранении специфичности, что особенно важно для диагностики вялотекущих инфекций[33].
Предоперационная диагностика. Важнейшим этапом диагностики является пункция сустава, которая должна выполняться в строго асептических условиях [34]. В рекомендациях CRIOGO, представленные во Франции в 2025 г., подробно описано, как обращаться с полученным материалом: пунктат разделяют на две части – одну помещают во флакон для анаэробных гемокультур, другую – в стерильную пробирку для посева на плотные среды. Такое разделение связано с разной чувствительностью методов: флаконы с гемокультурами позволяют выявить патогены чаще, чем агаровые среды, однако дляCutibacterium acnesлучше подходят тиогликолевая среда и агар Шедлера. Образцы необходимо доставить в лабораторию не позже чем через 2 ч; если это невозможно, допустимо хранить их при 4 °C, но не дольше 24 ч.Если при пункции получить жидкость не удается («сухая» пункция), не стоит вводить в сустав физиологический раствор для разведения, так как это исказит подсчет клеток и снизит концентрацию биомаркеров.В таких случаях прибегают к чрескожной биопсии (tru-cut); ее выполняют, когда пункция неинформативна или выпот отсутствует [35].
Цитологическое исследование синовиальной жидкости. Цитологический анализ синовиальной жидкости остается важным методом диагностики. В современных рекомендациях предложены следующие пороговые значения (табл. 2).
Таблица2
Диагностические пороги цитологического исследования синовиальной жидкости
|
Параметр |
EBJIS |
MSIS |
Острая инфекция |
|
Лейкоциты (клеток/мкл) |
> 1500 |
> 3000/мм³ |
> 10 000/мм³ |
|
Нейтрофилы (%) |
> 65% |
> 80% |
> 90% |
Примечание: составлена авторами на основе источников [32, 33, 36]
Сывороточные маркеры. СРБ и СОЭ – это стандартные скрининговые тесты, однако их специфичность невысока, поэтому исследователи ищут более точные сочетаниямаркеров [37]. В ретроспективном исследовании, включившем 177 пациентов с ППИ и 60 пациентов контрольной группы, сравнили диагностическую ценность нескольких серологических и синовиальных маркеров [36]:
- сывороточный СРБ показал наивысшую площадь под ROC‑кривой (AUC 0,912) при пороге 16,15 мг/дл (чувствительность 79,6%, специфичность 97,8%);
- для лейкоцитов синовиальной жидкости пороговое значение составило 5,75 клеток/мкл (AUC 0,803), для соотношения нейтрофилов к лимфоцитам (NLR) – 3,659 (AUC 0,803);
- комбинация трех показателей – сывороточного СРБ, количества лейкоцитов в синовиальной жидкости и NLR – дала наилучшие результаты: AUC 0,946, чувствительность 93%, специфичность 90,9%.
Такая комбинация удобна для клинического применения, так как не требует дополнительных расходов или специального оснащения.
Интраоперационная диагностика. Культуральное исследование остается краеугольным камнем диагностики ППИ, поскольку позволяет не только идентифицировать возбудителя, но и определить его чувствительность к антибиотикам [33]. Ключевые принципы, согласно рекомендациям CRIOGO, звучат следующим образом:
1. Забор 4–6 глубоких образцов тканей(предпочтительно из области контакта с имплантатом и синовиальной жидкости) с последующим микробиологическим и гистологическим исследованием.
2. Забор материала до начала антибиотикотерапии(за исключением пациентов с сепсисом).
3. Отказ от поверхностных мазковиз ран и свищей – их корреляция с истинной микрофлорой недостоверна.
4. Использование транспортных сред– флаконы с гемокультурами предпочтительнее, чем сухие пробирки.
5. Пролонгированная инкубация– не менее 14 дней для выявления медленнорастущих микроорганизмов [35].
Ограничениями культуральной диагностики считаются ложноотрицательные результаты при возможной предшествующей антибиотикотерапии, низкая чувствительность при низкой бактериальной нагрузке, трудности выявления микроорганизмов, интегрированных в биопленку, а также длительное время ожидания результатов [33].
Молекулярные методы диагностики. Обзорная статья по молекулярной диагностике Indelliи соавт. 2025 г. подтверждает, что эти методы становятся чрезвычайно ценными инструментами в процессе принятия решений при лечении ППИ[38].
Различные форматы ПЦР-анализа используются для выявления бактериальной ДНК непосредственно из клинических образцов. Исследование Bémer и соавт. продемонстрировало чувствительность и специфичность ПЦР гена 16S рРНК при диагностике ППИ: Количественная ПЦР (qPCR) определяет бактериальную нагрузку, а мультиплексная ПЦРпозволяет одновременное выявление множества патогенов (панели включают наиболее частые возбудители и гены резистентности) [35].
Обзор Sandu и соавт. подчеркивает, что точность современных биомаркеров может быть дополнительно повышена за счет разработки новых технологий детекции, таких как метагеномное секвенирование нового поколения (mNGS). Данный метод позволяет идентифицировать все микроорганизмы в образце без предварительного знания конкретного патогена, выявлять труднокультивируемые и медленнорастущие бактерии, определять профили генов резистентности [30].
Критически важно понимать, что ни один тест не обладает 100% точностью, и диагноз ППИ всегда должен основываться на совокупности клинических, лабораторных, микробиологических и гистологических данных. Диагностический алгоритм должен быть гибким и адаптироваться к конкретной клинической ситуации, доступным ресурсам и характеристикам пациента [39].
Лечение: стратегии и показания
Лечение ППИ преследует три основные цели: эрадикацию инфекции, сохранение функции конечности и минимизацию риска рецидива. Достижение этих целей требует мультидисциплинарного подхода с участием травматолога-ортопеда, клинического фармаколога, микробиолога. Выбор тактики лечения определяется временными критериями, стабильностью имплантата, состоянием мягких тканей, характеристиками возбудителя и соматическим статусом пациента [40].
Дебридмент с сохранением имплантата (DAIR). DAIR представляет собой органосохраняющую операцию, включающую открытый дебридмент, замену модульных компонентов (головки и вкладыша), обильное промывание и целенаправленную антибактериальную терапию [41]. В 2025 г. Европейское общество костно-суставных инфекций (EBJIS) опубликовало протокол, который систематизирует показания, противопоказания и факторы риска DAIR. Согласно рекомендациям EBJIS, DAIR следует рассматривать у пациентов, отвечающих следующим критериям:
1. Стабильный, правильно позиционированный и функционирующий имплантат– отсутствие рентгенологических признаков нестабильности компонентов.
2. Острая инфекция:
ранняя острая(≤4 недель после первичной артропластики);
поздняя острая (длительность симптомов <3 недель при изначально благополучном послеоперационном периоде (> 4 недель после операции)).
3. Удовлетворительное состояние мягких тканей(отсутствие свища, возможность первичного закрытия раны) [40].
Противопоказания к проведению DAIR: нестабильность имплантата, срок после операции более 12 недель, длительность симптомов свыше 3 недель, наличие свища или невозможность первичного закрытия раны [42].
Хирургическая техника включает открытый дебридмент, обязательную замену модульных компонентов с целью профилактики образования биопленки, забор 4–6 образцов тканей и обильное промывание антисептиками [43].
После операции антибактериальная терапия продолжается 12 недель, из них первая неделя – внутривенное введение (индукционный период). При отсутствии сепсиса или септического шока антибиотики назначают после того, как взяты интраоперационные пробы. Режим подбирают по результатам антибиотикограммы: при стафилококковой инфекции применяют комбинацию фторхинолонов с рифампицином, при грамотрицательной – фторхинолоны [40].
При строгом соблюдении критериев отбора частота благоприятного исхода DAIR достигает 70–80%. Попытка применить этот метод у пациентов, не отвечающих рекомендованным критериям, резко снижает его эффективность [44].
Ревизионное эндопротезирование. Если DAIR противопоказан или предшествующее лечение оказалось неэффективным, показано удаление компонентов эндопротеза. Вопрос о том, выполнять ревизию в один или два этапа, остается предметом дискуссий [45].
Двухэтапное ревизионное эндопротезирование. Традиционно двухэтапное ревизионное эндопротезирование считается методом выбора при лечении хронической ППИ. Частота успеха данного метода составляет более 80% [46].
Однако в исследовании Tubin и соавт., проведенном в специализированном ортопедическом центре, реальные результаты оказались скромнее. При использовании критериев Musculoskeletal Infection Society Outcome Reporting Tool (MSIS ORT) успешное лечение с реимплантацией достигнуто у58,2%пациентов. При применении Delphi-критериев этот показатель составил 86,6%. Авторы обращают внимание, что отсутствие единого стандартизированного подхода к оценке исходов затрудняет сравнение данных. Кроме того, сохранение спейсера и отказ от второго этапа (реимплантации) «размывают» картину и снижают долю действительно благоприятных исходов [47].
Вопрос о роли антибиотиков после реимплантации изучали Ryan и соавт. Согласно их данным, короткий курс пероральных антибиотиков (до 2 недель) снижает риск повторной инфекции на 62% (HR 0,38; p=0,01). Это свидетельствует о потенциальной пользе короткого курса после второго этапа двухэтапного ревизионного эндопротезирования [48].
Одноэтапное ревизионное эндопротезирование. Одноэтапное ревизионное эндопротезирование включает удаление импланта, радикальную хирургическую обработку и имплантацию нового эндопротеза. В последние годы этот вариант набирает обороты, поскольку позволяет сократить количество операций, сроки госпитализации и экономические затраты [49].
Kushwaha и соавт. провели ретроспективное сравнение двух методов у 60 пациентов (по 30 в каждой группе). Через 24 месяца частота реинфекции в обеих группах составила 0%. Функциональные исходы по шкале Harris Hip Score (HHS) были сопоставимы. При этом в группе одноэтапных ревизий болевой синдром (по ВАШ) оказался менее выражен через 3, 6 и 12 месяцев. Как и ожидалось, двухэтапные ревизии сопровождались более длительной госпитализацией и большими экономическими затратами.
Авторы делают вывод, что оба метода обеспечивают сопоставимые результаты при лечении хронической ППИ. Вместе с тем одноэтапное вмешательство может способствовать более быстрому купированию боли и снижению финансовой нагрузки [45].
Заключение
Перипротезная инфекция после эндопротезирования тазобедренного сустава по‑прежнему остается серьезным осложнением, требующим участия специалистов разного профиля. Современные эпидемиологические данные подтверждают, что доля ППИ остается стабильной, но при этом настораживает рост резистентных и полимикробных форм инфекции.
В диагностике важно опираться на строго стандартизированные подходы, которые объединяют клинические, лабораторные, микробиологические и гистологические методы. На предоперационном этапе центральное место занимает пункция сустава: ее выполняют в асептических условиях, а полученный материал разделяют для цитологии и микробиологии. Во время операции обязательно берут 4–6 глубоких образцов тканей. Новые технологии постепенно ускоряют идентификацию возбудителей и определение их резистентности, что помогает быстрее подобрать эффективную терапию.
Лечение ППИ строится с учетом ряда факторов: сроков развития инфекции, стабильности имплантата, состояния мягких тканей и характеристиках возбудителя. При острой инфекции (длительность симптомов до 3 недель) со стабильным, правильно позиционированным имплантатом и интактными мягкими тканями методом выбора является дебридмент с сохранением имплантата. При четком соблюдении показателей эффективность такого метода достигает 70–80%.
При хронической перипротезной инфекции показано ревизионное эндопротезирование тазобедренного сустава. Результаты одноэтапных ревизий представляют сопоставимые результаты с двухэтапными, при этом уменьшают количество операций, сокращают сроки восстановления и снижают экономические затраты. Двухэтапное ревизионное эндопротезирование долгое время считалось «золотым стандартом», однако в реальной клинической практике его успех во многом зависит от того, как именно оценивать исходы.
Ключевым условием успешного лечения остается тесная работа междисциплинарной команды: травматолога-ортопеда, клинического фармаколога, микробиолога.Только совместное взаимодействие специалистов позволяет правильно интерпретировать результаты диагностики, выбрать оптимальную тактику с учетом индивидуальных особенностей пациента и назначить адекватную антибактериальную терапию. Индивидуальный подход, который опирается на оценку факторов риска, микробиологический профиль и функциональный статус пациента, во многом определяет, насколько успешным будет лечение перипротезной инфекции.
Конфликт интересов
Финансирование
Библиографическая ссылка
Глазков И.Р. СОВРЕМЕННЫЙ ВЗГЛЯД НА ПЕРИПРОТЕЗНУЮ ИНФЕКЦИЮ ПОСЛЕ ЭНДОПРОТЕЗИРОВАНИЯ ТАЗОБЕДРЕННОГО СУСТАВА: ФАКТОРЫ РИСКА, ДИАГНОСТИКА И АЛГОРИТМЫ ЛЕЧЕНИЯ // Современные проблемы науки и образования. 2026. № 4. ;URL: https://science-education.ru/ru/article/view?id=34584 (дата обращения: 13.05.2026).
DOI: https://doi.org/10.17513/spno.34584



