Введение
Нейроэндокринные опухоли (НЭО) – гетерогенная группа злокачественных опухолей, исходящих из диффузной нейроэндокринной системы в различных органах. За последние четыре десятилетия заболеваемость данной патологией существенно возросла и демонстрирует устойчивую тенденцию к ежегодному приросту. НЭО тонкой кишки, среди всех НЭО, занимают второе место по частоте встречаемости, составляя 1,41 случая на 100000 населения, уступая лишь локализации в лёгких [1]. Следует отметить, что НЭО тонкой кишки (ТК), в литературе прошлых лет именуемые карциноидами, являются наиболее частой формой злокачественных опухолей данной локализации [2], что подчёркивает важность и актуальность изучения данной патологии.
НЭО ТК характеризуется ранним и активным метастазированием, как регионарным, так и отдаленным. Более чем у половины пациентов к моменту первичной диагностики выявляются регионарные метастазы в брыжейке тонкой кишки. В 1961 году Moertel и соавторы [3] выявили корреляцию между размером первичной опухоли и частотой метастазирования в регионарные лимфатические узлы. Так, при опухолях размером более 2 см частота поражения регионарных лимфатических узлов достигает 80%, что подтверждается современными данными [4; 5]. Характерной особенностью является то, что метастатические узлы в брыжейке, как правило, превосходят по размерам первичную опухоль. Также на момент постановки диагноза у 50-80% пациентов имеются отдаленные метастазы, преимущественно в печени [6-8].
Стандартно принятой практикой в лечении пациентов с НЭО тонкой кишки и метастазами в брыжейке является выполнение радикального хирургического лечения, включающего резекцию сегмента кишки вместе с конгломератом пораженных лимфатических узлов. При наличии отдаленных метастазов вопрос о целесообразности удаления первичного очага остается объектом дискуссий. В литературе приводятся данные об увеличении выживаемости, купировании карциноидного синдрома и профилактике ургентных состояний, связанных с ростом первичной опухоли и метастазов в брыжейке, при удалении первичного опухолевого очага [9-11]. В противовес данному подходу часть авторов заявляет об отсутствии преимуществ при выполнении таких вмешательств [12; 13].
Радикальное удаление метастатических лимфоузлов из брыжейки тонкой кишки является технически непростой задачей. В 2000 году Ohrvall и соавторы из клиники Уппсала, Швеция, разработали четырёхуровневую классификацию поражения брыжейки при тонкокишечных карциноидах [14].
Опираясь на предложенную классификацию и интегрируя накопленный клинический опыт, авторы разработали собственные хирургические подходы, ориентированные на разнообразные локализации конгломератов в брыжейке тонкой кишки.
Цель исследования
Оптимизировать и систематизировать хирургический подход у пациентов с нейроэндокринными опухолями тонкой кишки и конгломератами пораженных лимфатических узлов брыжейки.
Материалы и методы исследования
Исследование представляет собой ретроспективный анализ результатов хирургического лечения 73 пациентов с нейроэндокринными опухолями тонкой кишки на базе Национального медицинского исследовательского центра онкологии имени Н. Н. Блохина в период с 2000 по 2024 год.
Критериями включения являлись: морфологически верифицированный диагноз нейроэндокринных опухолей тонкой кишки, наличие конгломератов метастатических лимфоузлов в брыжейке. Критерии исключения – пациенты, не подвергшиеся хирургическому лечению, а также больные с отсутствием конгломератов пораженных лимфатических узлов в брыжейке. Все пациенты были комплексно обследованы до начала лечения. Хирургическое лечение при местнораспространенном процессе включало радикальное удаление первичной опухоли с резекцией пораженных участков брыжейки. В контексте метастатического заболевания хирургическое лечение проводилось в следующих объёмах: удаление первичной опухоли с конгломератом в брыжейке; радикальное удаление первичной опухоли с регионарными и отдаленными метастазами; удаление первичной опухоли и регионарных метастазов с циторедукцией метастазов в печени; паллиативные резекции тонкой кишки без удаления конгломерата в брыжейке и отдаленных метастазов.
Основным исследуемым параметром являлись непосредственные результаты хирургического лечения – радикальность оперативного вмешательства, послеоперационные осложнения и смертность.
Результаты исследования и их обсуждение
В период с 2000 по 2024 год было выполнено хирургическое лечение 73 больным с НЭО ТК. В анализ включены только пациенты с поражением регионарных лимфоузлов. У 21 больного (29%) выявлен местнораспространённый процесс (стадия T1-4N+M0), у 52 пациентов (71%) на момент постановки диагноза имелись отдалённые метастазы (стадия T1-4N+M1). Клинико-морфологическая характеристика пациентов представлена в таблице 1.
У 3 больных из группы местнораспространенного заболевания проводилась предоперационная терапия аналогами соматостатина. 23 пациента с отдаленными метастазами НЭО ТК получили предоперационную терапию в одном из следующих вариантов: 13 пациентов – аналоги соматостатина (АС), 1 больной получал АС в комбинации с таргетной терапией, 2 пациента – АС + химиотерапию, 5 – АС + трансартериальную эмболизацию печеночных артерий, 1 – АС + иммунотерапию интерфероном-альфа, 1 пациент – АС + полихимиотерапию в сочетании с бевацизумабом.
Всем 73 больным выполнены хирургические вмешательства. Объем операции зависел от выделенных типов поражения брыжейки. Соответственно выполнялись: резекция тощей кишки у 12 пациентов (16,4%); резекция подвздошной кишки - у 38 (52%); илеоцекальная резекция - у 3 больных (4,1%); гемиколэктомия справа – у 13 (17,8%), гемиколэктомия справа с расширенной резекцией подвздошной кишки - у 7 пациентов (9,6%).
Средняя длина резецированной части тонкой кишки составила 47 см, диапазон варьировал от 12 до 200 см.
Таблица 1
Клинико-морфологические характеристики пациентов
|
Всего пациентов |
73 |
|
Пол |
Мужчины – 30 (41%) Женщины – 43 (59%) |
|
Средний возраст |
53 |
|
Стадия заболевания
|
IIIA – 11 (15%) IIIB – 10 (13,7%) IV – 52 (71,2%) |
|
Средний размер брыжеечных метастазов, диапазон |
3,6 см (1,3–10 см) |
|
Локализация первичной опухоли |
Тощая кишка – 12 (16,3%) Подвздошная кишка – 61 (83,6%) |
|
Степень дифференцировки опухоли (Grade)
|
G1 – 29 (40%) G2 – 42 (57,5%) G3 – 2 (2,7%) |
|
Мультифокальный рост первичной опухоли |
16 (22%) |
|
Среднее количество опухолей при мультифокальном росте |
5 (2–26) |
|
Карциноидный синдром/ карциноидная болезнь сердца |
54 (80%)/3 (4%) |
Составлено авторами на основе полученных данных в ходе исследования.
У 17 (81%) пациентов с местнораспространенным заболеванием выполнено радикальное оперативное вмешательство (табл. 2). В 4 случаях выполнены R1/2 операции: двум пациентам была выполнена паллиативная резекция кишки без удаления метастазов из брыжейки, у 2 больных гистологически выявлен положительный край резекции.
Таблица 2
Результаты хирургического лечения у пациентов с T1-4N+M0
|
Объёмы операции |
R0 (17) |
R2 (4) |
|
Резекция тощей кишки – 4 |
3 |
1 |
|
Резекция подвздошной кишки – 11 |
8 |
3 |
|
Илеоцекальная резекция - 1 |
1 |
0 |
|
Гемиколэктомия справа – 2 |
2 |
0 |
|
Гемиколэктомия справа с расширенной резекцией подвздошной кишки – 3 |
3 |
0 |
Примечание: R0 – радикальное хирургическое вмешательство с отсутствием в краях резекции опухолевых клеток; R2 – неудаленные конгломераты пораженных лимфатических узлов в брыжейке тонкой кишки. Цифрами указано количество пациентов.
Составлено авторами на основе полученных данных в ходе исследования.
Радикальность вмешательств у больных IV стадией заболевания: 21 (40,3%) пациенту выполнено радикальное хирургическое лечение в объёме R0, включающее резекцию кишки и печени (табл. 3). Остальным больным выполнены R2 резекции, в числе которых были операции с остаточной опухолью в локорегионарной зоне или только в печени. Нерадикальное удаление первичной опухоли или регионарных метастазов было выполнено в связи с инвазией опухоли в двенадцатиперстную кишку и поджелудочную железу (1 случай), циркулярной инфильтрацией верхней брыжеечной вены (ВБВ) (3 случая).
Таблица 3
Результаты хирургического лечения пациентов с НЭО тонкой кишки cT1-4 N+M1
|
Объёмы операции
|
R0 (21)
|
R2 (31) |
|
|
R2 (4) в локорегионарной зоне |
R2 (27) отдаленные метастазы |
||
|
Резекция тощей кишки – 8 |
5 |
1 |
2 |
|
Резекция подвздошной кишки – 27 |
9 |
3 |
15 |
|
Илеоцекальная резекция - 2 |
2 |
0 |
0 |
|
Гемиколэктомия справа – 11 |
3 |
0 |
8 |
|
Гемиколэктомия справа с расширенной резекцией подвздошной кишки – 4 |
2 |
0 |
2 |
Примечание: R0 – радикальное хирургическое вмешательство, включающее как удаление первичного опухолевого очага с метастазами в брыжейке и отдаленных метастазов, с отсутствием в краях резекции опухолевых клеток; R2 – неудаленные конгломераты пораженных лимфатических узлов в брыжейке тонкой кишки или отдаленные метастазы. Цифрами указано количество пациентов. Составлено авторами на основе полученных данных в ходе исследования.
Послеоперационные осложнения возникли у 8 пациентов (10,9%). По классификации Clavien Dindo осложнение I степени возникло у 1 больного, II степени – у 3, IIIA степени – у 3, IIIB степени – у 1 пациента. Послеоперационной летальности не зафиксировано.
В послеоперационном периоде синдром короткой кишки возник у 7 пациентов. Средняя длина резецированной тонкой кишки, при которой возник синдром, составила 144 см (диапазон от 104 до 200 см). При анализе данных основными причинами расширенной резекции тонкой кишки, приведшими к синдрому короткой кишки, являлись: множественные первичные опухоли (n = 1); множественные конгломераты метастатических узлов (n = 3); особенности артериального кровоснабжения брыжейки толстой кишки (n = 1); объемное образование брыжейки (>6 см) и мультифокальный рост первичной опухоли (n = 2).
Хирургические подходы в зависимости от локализации брыжеечных метастазов
Механизмы развития и распространения метастазов в брыжейку представляют собой сложное клиническое явление, значительно влияющее на выбор хирургической тактики и проведение радикальных вмешательств. В рамках данного исследования выделены 5 наиболее типичных вариантов локализации конгломератов, каждый из которых требует четко выверенной хирургической тактики, основанной на степени вовлеченности сосудистых структур и степени распространения опухолевого процесса. Схематическое представление локализации метастазов по отношению к сосудам брыжейки и КТ-снимок соответствующего распространения опухоли представлены на рисунках 1-6.
Первый тип - локализация конгломерата вблизи стенки кишки с поражением только прямых сосудов, что соответствует концепции I уровня по классификации Ohrvall. В данном случае целесообразно выполнение перевязки прямых сосудов с пересечением аркады по границе поражения и единичных радиальных сосудов выше метастатического узла и резекции вовлечённой части тонкой кишки с клиновидной резекцией брыжейки (рис. 1).
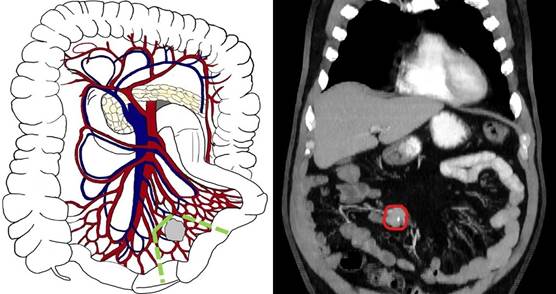
Рис. 1. Первый тип (уровень I) - локализация конгломерата пораженных лимфатических узлов в непосредственной близости к кишечнику с вовлечением терминальных сосудистых ветвей
Второй тип (уровень II по Ohrvall) - локализация конгломерата в зоне отхождения a. et v. Ileocolica. Такая картина часто наблюдается при локализации опухоли в терминальном отделе подвздошной кишки. При этом типе выполняется перевязка этих сосудов у их основания с сохранением ствола верхней брыжеечной артерии (ВБА) и верхней брыжеечной вены (ВБВ) ниже. Такой подход предполагает выполнение илеоцекальной резекции или гемиколэктомии справа в зависимости от локализации первичной опухоли и возможности сохранения правых толстокишечных сосудов (рис. 2).

Рис. 2. Второй тип (уровень II) - поражение подвздошно-ободочной артерии или вены
Третий А тип (уровень III по Ohrvall) - распространение опухолевого конгломерата вдоль ВБА и ВБВ, на уровне или ниже a. Ileocolica (рис. 3). Погранично-резектабельный. В данном случае возможно выделение и перевязка вовлеченных радиальных ветвей первого порядка. В подобных случаях, как правило, возникает необходимость выполнять обширные резекции тонкой кишки. Необходимо четко оценить планируемый и возможный объем операции, длину резецируемой и остающейся тонкой кишки и возможность развития синдрома короткой кишки после операции.
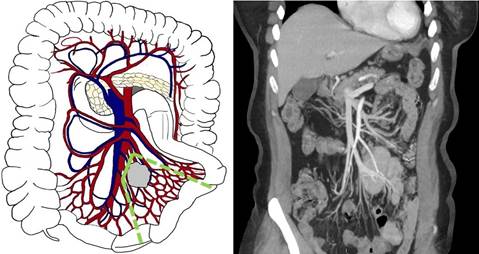
Рис. 3. Третий А тип (уровень III) - локализация брыжеечных метастазов на уровне или дистальнее отхождения a. et v. ileocolica, без вовлечения ствола ВБА/ВБВ
Третий В тип (уровень III по Ohrvall) - вовлечение стволов ВБА и/или ВБВ дистальнее ветвления a. et v. ileocolica. В подобных случаях выполняем резекцию подвздошной кишки с перевязкой соответствующих стволов ВБА и ВБВ выше уровня поражения, с сохранением a. et v. Ileocolica, что позволяет не резецировать восходящий отдел толстой кишки (рис. 4). При этом перевязываются не менее трёх радиальных ветвей ВБА первого порядка, что приводит к протяженной резекции кишки.
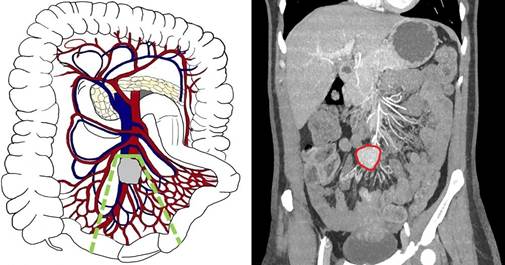
Рис. 4. Третий В тип (уровень III) - вовлечение стволов и ветвей ВБА/ВБВ дистальнее ветвления a. et v. ileocolica
Четвертый тип (уровень III по Ohrvall) - характеризуется наличием массивных конгломератов в брыжейке, располагающихся проксимальней подвздошно-ободочных сосудов, вовлекая их в патологический процесс, а также правые ободочные сосуды и ствол ВБА/ВБВ без циркулярного роста. В подобных случаях возможна перевязка a. et v. ileocolica, a. et v. colica dextra и выполнение гемиколэктомии справа с расширенной резекцией подвздошной кишки и сохранением стволов ВБА и ВБВ (рис. 5). Такой тип поражения брыжейки относится к погранично-резектабельному.
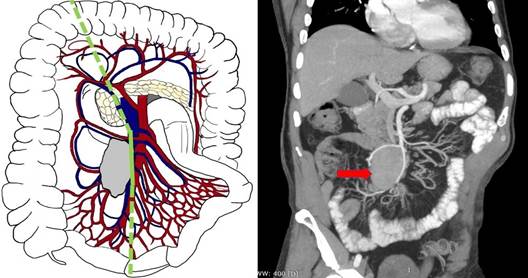
Рис. 5. Четвертый тип (уровень III) - массивный метастатический конгломерат в брыжейке, располагающийся проксимальней подвздошно-ободочных сосудов, с вовлечением стволов ВБА/ВБВ без циркулярного охвата
Пятый тип (уровень IV по Ohrvall) - конгломерат метастатических узлов циркулярно охватывает ствол ВБА или ВБВ под нижним краем поджелудочной железы, нередко инвазируя последнюю и двенадцатиперстную кишку, распространяясь также забрюшинно. При данной распространенности процесс, как правило, нерезектабельный или требует выполнения реконструкции ВБА/ВБВ (рис. 6).

Рис. 6. Пятый тип (уровень IV) - конгломерат компримирует корень брыжейки с циркулярным ростом вокруг ВБА или ВБВ
Нейроэндокринные опухоли тонкой кишки отличаются ранним и активным метастазированием в регионарные лимфатические узлы и отдалённые органы, преимущественно в печень [4; 5]. Несмотря на агрессивный характер заболевания, более половины пациентов переживают 10-летний срок наблюдения [15]. В отсутствие отдалённых метастазов хирургическое лечение остаётся основным радикальным методом, способным обеспечить длительную ремиссию и потенциальное излечение [16]. При распространённом заболевании терапевтический подход становится более предпочтительным и включает в себя использование аналогов соматостатина в сочетании с химио- и таргетной терапией, либо как самостоятельное лечение. Аналоги соматостатина не только эффективно купируют карциноидный синдром, но и обладают доказанной антипролиферативной активностью, что подтверждается клиническими данными из исследований CLARINET и PROMID [17; 18].
В литературе существуют данные, говорящие о целесообразности хирургических вмешательств у больных как местнораспространенным, так и метастатическим процессом [9; 19; 20]. При IV стадии заболевания хирургические подходы могут варьироваться от удаления первичной опухоли до радикальной операции. Вопрос эффективности удаления первичного очага остаётся предметом активного исследования. Большинство работ, посвящённых анализу результатов данного метода, свидетельствуют об увеличении выживаемости пациентов, подвергшихся хирургическому лечению, по сравнению с пациентами без операции, даже при наличии нерезектабельных метастазов в печени [9–11]. Авторы подчёркивают, что удаление первичной опухоли не только способствует контролю карциноидного синдрома, но и замедляет прогрессирование заболевания [9]. В то же время в мировой литературе приводятся данные об отсутствии преимуществ при таком подходе [12; 13].
Основной тактической и технической задачей при поражении регионарных лимфоузлов является оценка степени поражения брыжейки кишки, вовлечения ветвей верхних брыжеечных сосудов, объёма предполагаемой резекции кишки с учетом послеоперационных функциональных результатов.
Характерной особенностью НЭО ТК является развитие десмопластической реакции брыжейки вследствие избыточной продукции серотонина и тахикинина и других биологически активных веществ, приводящей к развитию фиброза, что существенно затрудняет хирургическое вмешательство [21; 22]. В брюшной полости десмопластическая реакция проявляется втяжением стенки кишки к метастатическому конгломерату в брыжейке и формированием спаечного процесса, что нередко вызывает нарушение кишечной проходимости. Кроме того, циркулярный рост метастатического опухолевого узла вокруг ВБА и ВБВ может вызывать ишемические изменения в тонкой кишке.
Руководствуясь необходимостью объективной оценки резектабельности первичной опухоли и регионарных метастазов, в 2000 году Ohrvall и соавторы разработали оригинальную классификацию поражения брыжейки, которая основана на анатомическом расположении опухолевых конгломератов относительно ВБА и ВБВ [14]. Позднее, в 2017 году, Partelli et al. внедрили аналогичную трёхуровневую систему классификации, где тип A предполагает резектабельное поражение, тип B - погранично резектабельное, а тип C - нерезектабельное [23]. Несмотря на то, что ценность предложенных классификаций трудно переоценить, в клинической практике отсутствует детальное описание специализированных хирургических подходов, адаптированных под конкретное расположение конгломератов, что ограничивает их практическое применение в контексте персонализированного хирургического планирования.
В связи с этим предпринята попытка более детального описания типичных вариантов поражения брыжейки кишки с подробным описанием соответствующих объёмов хирургических вмешательств, которые могут быть выполнены. Тщательный анализ ситуации, распространенности опухоли, локализации метастатических конгломератов по отношению к брыжеечным сосудам позволяет, как правило, укладывать ситуацию в один из типичных вариантов и планировать хирургическое вмешательство на предоперационном этапе. Особое внимание заслуживают типы 3 и 4, которые нередко требуют проведения расширенных резекций тонкой кишки. Такие обширные операции сопряжены с высоким риском развития синдрома короткой кишки, что значительно ухудшает функциональный статус пациентов, проявляясь хронической диареей, снижением аппетита, потерей массы тела и электролитными нарушениями. В связи с этим авторы настоятельно рекомендуют применять прецизионную технику, максимально сохраняя сосуды кишки, тщательно соблюдая при этом принципы адекватной лимфаденэктомии, чтобы достичь баланса между радикальностью лечения и сохранением качества жизни пациента.
В настоящем исследовании представлены специализированные хирургические подходы при нейроэндокринных опухолях тонкой кишки. Ключевыми факторами, определяющими возможность и объем хирургического вмешательства, являются распространенность метастатического конгломерата и инвазия в стволы ВБА и ВБВ. Предложенный подход к оценке поражений позволяет предварительно определить радикальность резекции и минимизировать риск возникновения осложнений, в частности развития синдрома короткой кишки.
Таким образом, представленная классификация поражений брыжейки и предложенные рекомендации по хирургической тактике создают базу для стандартизации подходов и повышения эффективности лечения пациентов с нейроэндокринными опухолями тонкой кишки, особенно при наличии крупных конгломератов брыжейки.
Такой подход позволяет оптимизировать объем вмешательства, повысить вероятность радикальности операции и обеспечить ее безопасность и хорошие функциональные результаты.
Заключение
В настоящем исследовании показаны специализированные хирургические подходы при нейроэндокринных опухолях тонкой кишки. Ключевыми факторами, определяющими возможность и объем хирургического вмешательства, являются распространенность метастатического конгломерата и инвазия в стволы ВБА и ВБВ. Предложенный подход к оценке поражений позволяет предварительно определить радикальность резекции и минимизировать риск возникновения осложнений, в частности развития синдрома короткой кишки.
Конфликт интересов
Финансирование
Библиографическая ссылка
Батыров К.А., Бохян В.Ю., Комаров И.Г., Гогиева Э.Х., Габрава М.М. ХИРУРГИЧЕСКАЯ ТАКТИКА У БОЛЬНЫХ С МЕСТНОРАСПРОСТРАНЕННЫМИ И МЕТАСТАТИЧЕСКИМИ НЕЙРОЭНДОКРИННЫМИ ОПУХОЛЯМИ ТОНКОЙ КИШКИ // Современные проблемы науки и образования. 2026. № 3. ;URL: https://science-education.ru/ru/article/view?id=34496 (дата обращения: 10.06.2026).
DOI: https://doi.org/10.17513/spno.34496



