Введение
Травмы крестообразных связок представляют собой одну из наиболее распространенных категорий спортивных травм во всем мире. В Соединенных Штатах ежегодно около 250 000 человек получают разрывы передней крестообразной связки (ПКС), причем почти в 50% этих случаев требуется реконструктивное хирургическое вмешательство [1; 2]. Хотя травмы задней крестообразной связки (ЗКС) встречаются реже, структурные повреждения ЗКС выявляются у 38% пациентов с травмами колена, и такие травмы связаны со значительными долгосрочными неблагоприятными последствиями для функции коленного сустава [3; 4]. Актуальных данных по эпидемиологии повреждений крестообразных связок в Российской Федерации нет [5].
Внутренний потенциал заживления крестообразных связок ограничен из-за недостаточной васкуляризации. После травмы микроструктурные изменения, включая клеточные изменения и дезорганизацию внеклеточного матрикса, приводят к изменению механических свойств ткани связки [6]. Функциональная недостаточность крестообразных связок приводит к нестабильности коленного сустава и способствует развитию гонартроза. В клинической практике пациенты могут испытывать хроническую боль, изменение походки, гипотрофию мышц и прогрессирующее функциональное нарушение, что в конечном итоге приводит к значительному снижению физической активности и качества жизни. Эти патологические последствия можно предотвратить своевременным хирургическим вмешательством, которое обычно включает пластику или реинсерцию связки. Однако результаты хирургического лечения сильно зависят от времени вмешательства: на поздних стадиях необратимые изменения сустава существенно ограничивают эффективность операции. Следовательно, ранняя и точная диагностика повреждений крестообразных связок имеет критически важное значение, особенно у лиц, занимающихся интенсивной физической активностью.
В случаях полного разрыва крестообразных связок клинические проявления, как правило, выражены и легко подтверждаются с помощью неинвазивных методов визуализации, таких как магнитно-резонансная томография (МРТ) и ультразвуковое исследование, а также во время диагностического этапа артроскопического вмешательства [7]. Однако частичные субсиновиальные разрывы, связанные с незначительными микроструктурными изменениями, представляют собой серьезную диагностическую проблему. В таких случаях явные клинические признаки нестабильности коленного сустава могут отсутствовать, а традиционные методы визуализации, включая МРТ, демонстрируют ограниченную чувствительность для обнаружения этих повреждений [8].
Методы оптической спектроскопии, успешно применяемые в различных медицинских дисциплинах, включая общую хирургию, эндокринологию, урологию, онкологию, неврологию и нейрохирургию, предоставляют возможность объективной и количественной оценки состояния тканей [9-11].
Спектроскопия представляет собой анализ взаимодействия между материей и электромагнитным излучением. Анализ спектра поглощения или излучения позволяет определить компонентный состав, структурную организацию и некоторые физические характеристики исследуемого образца. Рамановская спектроскопия (РС) впервые была описана К. В. Раманом в 1928 году, который идентифицировал рассеянные фотоны, демонстрирующие сдвиг длины волны относительно падающего света. В РС монохроматический лазерный источник освещает образец, вызывая фотонно-молекулярные взаимодействия, которые могут приводить к потере энергии (стоксово рассеяние) или приобретению энергии (антистоксово рассеяние) рассеянными фотонами [12-14]. Обмен энергией возбуждает определенные молекулярные колебания, генерируя Рамановский спектр, в котором каждая молекула демонстрирует характерный рисунок, соответствующий ее составным функциональным группам [15]. Этот метод позволяет идентифицировать и характеризовать молекулярный состав и структуру материалов. РС чувствительна к изменениям в конформации и составе клеток, тканей, дезоксирибонуклеиновой кислоты (ДНК), белков и липидов [12].
Цель исследования
Исследовать возможность использования метода Рамановской спектроскопии для оценки состояния крестообразных связок коленного сустава.
Материалы и методы исследования
Для отбора пациентов к участию в исследовании проводили скрининг среди совершеннолетних пациентов, имевших показания к тотальному эндопротезированию коленного сустава. Всем пациентам в предоперационном периоде была выполнена МРТ, на основании которой диагностированы повреждения хотя бы одной крестообразной связки коленного сустава, соответствующее 1-2 типам по шкале остеоартрита передней крестообразной связки (ACLOAS). Пациентов с полным разрывом, а также с отсутствием патологии крестообразных связок, по данным МРТ, не включали в исследование.
В ходе операции проводили анализ состояния крестообразных связок, оценивая их по классификации американской ассоциации хирургов-ортопедов (AAOS) до их эксцизии. При выполнении операции тотального эндопротезирования коленного сустава осуществляли забор эксплантов ПКС и ЗКС, которые впоследствии подвергали спектроскопическому исследованию. Образцы крестообразных связок изымали единым блоком совместно с костными точками прикрепления для сохранения структурной целостности и обеспечения оптической оценки областей прикрепления. После каждого оперативного вмешательства экспланты тщательно осматривались на предмет ятрогенных повреждений, полученных во время забора, чтобы исключить потенциальные артефакты измерения. Образцы, имеющие такие повреждения, исключались из дальнейшего анализа. Несмотря на то, что в исследование включали только тех пациентов, у которых при предоперационном МРТ-исследовании выявляли повреждения только 1 и 2 типов по классификации ACLOAS, все же в некоторых случаях интраоперационно, используя классификацию AAOS, выявляли повреждения и III степени, то есть полный разрыв. В общей сложности в окончательный анализ были включены 30 эксплантов передней и задней крестообразных связок, полученных от 24 пациентов.

Рис. 1. Экспланты ПКС: слева - 1-я степень повреждения (AAOS), справа - 3-я степень повреждения (AAOS).
Примечание: составлено авторами в ходе исследования
Извлеченные экспланты связок тщательно промывали в стерильном контейнере физиологическим раствором хлорида натрия (NaCl – 0,9%) для удаления остаточных следов крови и синовиальной жидкости, которые могли бы помешать получению спектров. Для предотвращения дегидратации биологических образцов в контейнер добавляли 150 мл фосфатно-буферного раствора (PBS).
Для анализа методом Рамановской спектроскопии на каждом экспланте выделили девять репрезентативных точек (рис. 2).
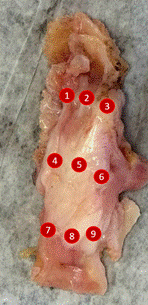
Рис. 2. Точки получения спектров на примере экспланта ПКС. Примечание: составлено авторами в ходе исследования
Каждое измерение повторяли два-три раза, в результате чего получили набор данных, включающий 270 исследованных участков крестообразных связок.
Основные полосы Рамановского рассеяния для молекул, содержащихся в связках, известны и описаны в литературе [16].
Основные полосы Рамановского рассеяния для молекул, содержащихся в связках
|
Пик (см-1) |
Молекулярное колебание |
Молекулярный компонент |
Ткань сустава |
|
850-880 |
C-C |
Коллаген |
Хрящ, синовиальная жидкость, сухожилие, связка, мениск |
|
1001-1004 |
Ароматическое |
Белки |
Хрящ, синовиальная жидкость, сухожилие, связка, мениск |
|
1240 |
C-N |
Дефектный коллаген |
Хрящ, синовиальная жидкость, сухожилие, связка, мениск, субхондральная кость, кость |
|
1270 |
Функциональный коллаген |
||
|
1441-1460 |
CH2 |
Липиды и белки |
Хрящ, сухожилие, связка, мениск, субхондральная кость, кость |
|
1630-1690 |
C=O |
Коллаген и другие белки |
Хрящ, сухожилие, связка, мениск, субхондральная кость, кость |
Примечание: составлено авторами на основе источника [16].
Использовали источник света с длиной волны 690 нм при комнатной температуре (25±2 °C). Оптическая система использовала ряд линз и зеркал для направления падающего луча в одно из двух оптических волокон, в то время как рассеянный сигнал от образца собирался через второе волокно и передавался через коллиматор и полосовой фильтр на входную щель монохроматора. Спектры Рамановского рассеяния регистрировали в диапазоне 2600–3800 см-1 с помощью монохроматора М266 (решетка 600 штрихов/мм, SOL Instruments Ltd., Минск, Беларусь), оснащенного камерой с зарядовой связью (ПЗС-детектор) с обратной засветкой в ближнем ИК-диапазоне, глубоко обедненным слоем и термоэлектрическим охлаждением (iDus 416, Andor Technology, Белфаст, Северная Ирландия, Великобритания). Монохроматор и ПЗС-детектор работали под управлением программного обеспечения Solar Lab, разработанного компанией SOL Instruments Ltd (Минск, Беларусь). Спектры регистрировали при интенсивности лазерного излучения на поверхности ткани около 500 мВт, время измерения каждого спектра составляло 3 секунды. Ширина входной щели монохроматора составляла 100 мкм.

Рис. 1. Общий вид установки для Рамановской спектроскопии.
Примечание: составлено авторами в ходе исследования
Статистические сравнения между степенями повреждения крестообразных связок оценивали при помощи непараметрического U-критерия Манна-Уитни. Всего таким образом было проанализировано более 300 спектров Рамановской спектроскопии. Для корректировки исходных p-значений, полученных с помощью каждого отдельного U-критерия Манна-Уитни, применяли поправку Бонферрони. Для заключения о статистической значимости скорректированное p-значение должно было быть меньше установленного уровня, равного 0,05.
Результаты исследования и их обсуждение
По результатам измерений был построен график средних спектров Рамановского рассеяния в зависимости от Рамановского сдвига (рис. 4).

Рис. 4. Вариабельность интенсивности спектров Рамановского рассеяния в зависимости от степени повреждения связки по AAOS.
Примечание: составлено авторами в ходе исследования
В Рамановской спектроскопии для нивелирования аппаратных факторов и различного времени накопления принято использовать отношения интенсивностей пиков. Нормирование проводили на самые интенсивные полосы: 1270 см-1 (маркер функционального коллагена) и 1450 см-1 (маркер белков/липидов), на которые были построены диаграммы (рис. 5, 6).
При нормировании на пик 1270 см-1 обращает на себя внимание отношение дефектного коллагена к функциональному (диаграмма 1240/1270 см-1), где выявлено статистически значимое различие между I и II степенью повреждения связки по AAOS (p < 0,001). Это подтверждает, что степень дегенерации коррелирует с увеличением доли дефектного коллагена. Статистически значимое различие между II и III степенью (р < 0,01) определено только при исследовании отношений 850/1270 см-1 и 1002/1270 см-1 (рис. 5).
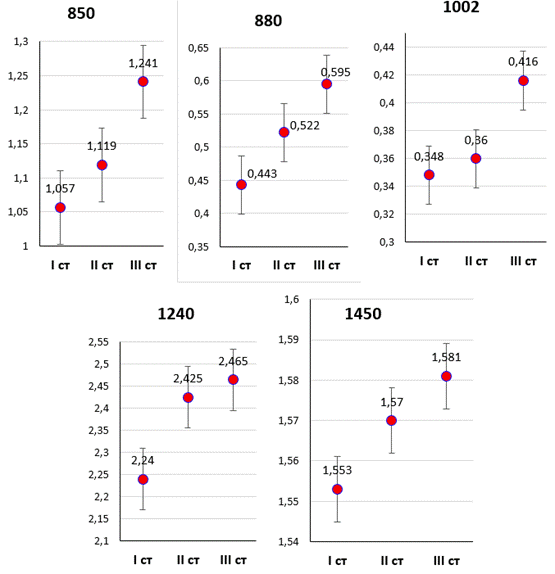
Рис. 5. Диаграммы размаха с оценкой статистической значимости различий между степенями тяжести повреждений связок по AAOS по данным РС (нормирование на пик 1270 см-1). Примечание: составлено авторами в ходе исследования
При нормировании на пик 1450 см-1 можно отметить статистически значимые различия между I и II степенью повреждения связки по AAOS на полосах Рамановского рассеяния 1240, 1270, 1650 см-1 (p < 0,001). Статистически значимы также различия между I и III степенью на всех полосах Рамановского рассеяния (р < 0,001). Однако различия между II и III степенью по AAOS при данном методе анализа были статистически незначимыми (р > 0,05) (рис. 6).
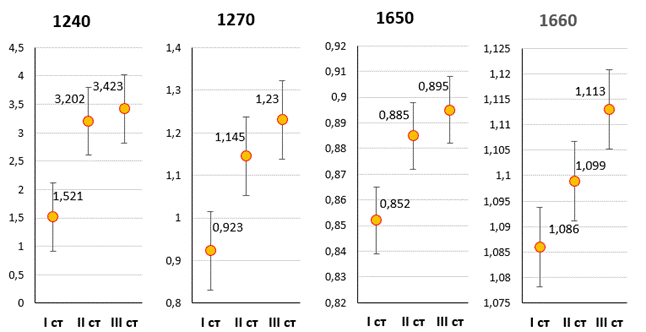
Рис.6. Диаграммы размаха с оценкой статистической значимости различий между степенями тяжести повреждений связок по AAOS по данным РС (нормирование на пик 1450 см-1). Примечание: составлено авторами в ходе исследования
Заключение
Таким образом, метод Рамановской спектроскопии позволяет эффективно дифференцировать состоятельную связку (неповрежденную или поврежденную незначительно – I степень по AAOS) от патологически измененной (II и III степени) за счет оценки отношения дефектного и функционального коллагена. В то же время разграничение между II и III степенями повреждения оказалось более сложной диагностической задачей и стало возможным лишь при анализе отношений 850/1270 см-1 и 1002/1270 см-1. С клинической точки зрения полученные результаты указывают на потенциальную значимость Рамановской спектроскопии как объективного инструмента оценки состояния крестообразных связок. В перспективе интеграция данного метода в клиническую практику может повысить объективность диагностики.
Конфликт интересов
Финансирование
Библиографическая ссылка
Лычагин А.В., Калинский Е.Б., Азаркин К.М., Гаркави А.В., Гончарук Ю.Р. ОПРЕДЕЛЕНИЕ ВОЗМОЖНОСТИ ПРИМЕНЕНИЯ МЕТОДА РАМАНОВСКОЙ СПЕКТРОСКОПИИ ДЛЯ ВЫЯВЛЕНИЯ НЕСОСТОЯТЕЛЬНОСТИ КРЕСТООБРАЗНЫХ СВЯЗОК КОЛЕННОГО СУСТАВА // Современные проблемы науки и образования. 2026. № 3. ;URL: https://science-education.ru/ru/article/view?id=34489 (дата обращения: 10.06.2026).
DOI: https://doi.org/10.17513/spno.34489



