Введение
В настоящее время острая декомпенсация хронической сердечной недостаточности (ОДСН) остается одной из наиболее актуальных и сложных проблем современной кардиологии, анестезиологии и реаниматологии [1–3]. Это состояние характеризуется высокими показателями госпитальной летальности, достигающими 4–7 %, и крайне неблагоприятным отдаленным прогнозом с годовой летальностью, превышающей 35 % [4–6]. ОДСН является ведущей причиной экстренных госпитализаций в кардиологические стационары, составляя до 50 % всех случаев [1, 7], а риск повторной госпитализации в течение двух лет после эпизода достигает 80 % [1].
Одним из известных осложнений, определяющим тяжесть состояния и тактику лечения пациента, является развитие острой дыхательной недостаточности (ОДН) на фоне кардиогенного отека легких [8–10]. Патофизиологической основой ОДН при ОДСН служит критическое повышение давления в легочных капиллярах, приводящее к транссудации жидкости в интерстиций и альвеолы. Это вызывает резкое снижение растяжимости легких, увеличение работы дыхательной мускулатуры и гипоксемию. В результате дыхательная мускулатура может потреблять до 16 % сердечного выброса, что создает дополнительную функциональную нагрузку на миокард [11, 12]. В подобных условиях инвазивная искусственная вентиляция легких (ИВЛ) становится не только методом респираторной поддержки, но и важным компонентом гемодинамической разгрузки сердца [13].
Потребность в ИВЛ является значимым прогностическим маркером, ассоциированным с госпитализацией в отделения реанимации и интенсивной терапии (ОРИТ) и увеличением длительности лечения, риском инфекционных осложнений и общей летальностью [13–15]. Несмотря на это, в настоящее время отсутствуют валидированные инструменты для стратификации риска развития ОДН, требующей инвазивной респираторной поддержки, у пациентов с ОДСН при госпитализации.
Цель исследования– разработка прогностической модели для оценки индивидуального риска развития дыхательной недостаточности, требующей проведения инвазивной искусственной вентиляции легких, у пациентов с острой декомпенсацией хронической сердечной недостаточности в ОРИТ.
Материал и методы исследования
Проведено проспективное одноцентровое когортное исследование пациентов с ОДСН в кардиологическом ОРИТ (2021–2023 гг.) для разработки модели прогнозирования потребности в ИВЛ. В исследование включались пациенты старше 18 лет с диагнозом ОДСН при наличии информированного согласия; критерии исключения не применялись для повышения репрезентативности. Проанализированы данные об этиологии ХСН, причинах декомпенсации, клинико-лабораторных показателях при поступлении и исходы госпитализации.
Количественные данные представлены в виде медианы с межквартильными интервалами (Me [Q1; Q3]), качественные показаны как абсолютные значения и проценты. Для сравнительного анализа между группами непрерывных переменных применялся критерий Манна – Уитни. Бинарные параметры анализировались с помощью точного теста Фишера. Независимые предикторы были выявлены с помощью многофакторного логистического регрессионного анализа методом обратного пошагового отбора по Вальду; в модель включались переменные со статистически значимыми межгрупповыми различиями. Непрерывные показатели предварительно бинаризировались по пороговым значениям, установленным на основе ROC-анализа по индексу Юдена.
Оценка качества прогностической модели также была проведена с помощью ROC-анализа. Дополнительно были рассчитаны чувствительность, специфичность и общая точность. Двусторонний пороговый уровень статистической значимости составил p < 0,05. Статистический анализ был проведен с помощью специализированного программного обеспечения IBM SPSS Statistics v. 27.0 и Stata v. 18.0.
Результаты исследования и их обсуждение
Характеристика пациентов
В исследование было включено 140 пациентов (рис. 1). Частота использования ИВЛ составила 7,9 % (11 пациентов).
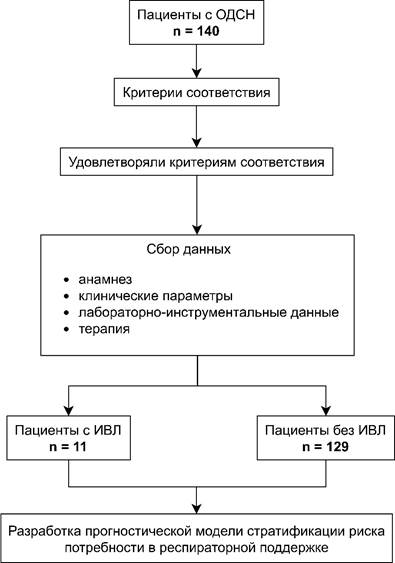
Рис. 1. Потоковая диаграмма исследования
Примечание: СН – сердечная недостаточность, составлен авторами на основе данных, полученных в ходе исследования
По результатам однофакторного анализа было показано, что пациенты, состояние которых потребовало использования ИВЛ, характеризовались большей частотой наличия хронической обструктивной болезни легких и/или бронхиальной астмы (54,5 % против 21,1 %; p = 0,022). Одновременно с этим ведущей причиной ОДСН у таких пациентов были респираторные инфекции (27,3 % против 5,4 %; p = 0,032) (табл. 1).
Таблица 1
Клинико-демографические и анамнестические данные пациентов с ОДСН
|
Параметр |
Самостоятельное дыхание (n = 129) |
ИВЛ (n = 11) |
р-значение |
|
Клинико-демографическая характеристика |
|||
|
Пол, муж. |
63 (48,8 %) |
5 (45,5 %) |
> 0,9 |
|
Возраст, лет |
76 [66; 84] |
81 [66; 84] |
0,582 |
|
ИМТ |
30,5 [26,3; 35,6] |
35,3 [27,3; 41,5] |
0,419 |
|
ИБС |
71 (55,5 %) |
5 (45,5 %) |
0,546 |
|
ПИКС |
61 (47,7 %) |
1 (9,1 %) |
0,023 |
|
Сопутствующие заболевания |
|||
|
Гипертоническая болезнь |
129 (100,0 %) |
11 (100,0 %) |
> 0,9 |
|
Сахарный диабет |
57 (44,2 %) |
4 (36,4 %) |
0,756 |
|
ХБП |
48 (37,5 %) |
1 (9,1 %) |
0,097 |
|
ХОБЛ/БА |
27 (21,1 %) |
6 (54,5 %) |
0,022 |
|
ОНМК в анамнезе |
24 (18,6 %) |
2 (18,2 %) |
> 0,9 |
|
Этиология ХСН |
|||
|
АГ |
52 (41,6 %) |
7 (63,6 %) |
0,208 |
|
ИБС |
55 (44,0 %) |
1 (9,1 %) |
0,027 |
|
Кардиомиопатия |
11 (8,8 %) |
3 (27,3 %) |
0,088 |
|
Клапанные пороки сердца |
5 (4,0 %) |
0 (0,0 %) |
> 0,9 |
|
Аритмия |
2 (1,6 %) |
0 (0,0 %) |
> 0,9 |
|
Ведущий триггер ОДСН |
|||
|
Артериальная гипертензия |
79 (61,2 %) |
4 (36,4 %) |
0,122 |
|
Аритмия |
15 (11,6 %) |
1 (9,1 %) |
> 0,9 |
|
Низкая приверженность к терапии |
12 (9,3 %) |
1 (9,1 %) |
> 0,9 |
|
Прогрессирование сопутствующего заболевания |
14 (10,9 %) |
2 (18,2 %) |
0,615 |
|
Инфекция |
7 (5,4 %) |
3 (27,3 %) |
0,032 |
|
Нарушение диеты |
2 (1,6 %) |
0 (0,0 %) |
> 0,9 |
Количественные данные представлены в виде Me [IQR], где Me – медиана, IQR – интерквартильный интервал. Качественные данные представлены в виде абсолютных и относительных частот.
Аббревиатуры: АГ – артериальная гипертензия; АКШ – аортокоронарное шунтирование; ДИ – доверительный интервал; ИБС – ишемическая болезнь сердца; ИМТ – индекс массы тела; ОДСН – острая декомпенсация сердечной недостаточности; ОНМК – острое нарушение мозгового кровообращения; ПИКС – постинфарктный кардиосклероз; ст. – степень; ХБП – хроническая болезнь почек; ХОБЛ/БА – хроническая обструктивная болезнь легких / бронхиальная астма; ХСН – хроническая сердечная недостаточность.
Примечание: составлена авторами на основе данных, полученных в ходе исследования
При изучении результатов физикального осмотра пациентов и данных инструментальных исследований было выявлено различие в частоте систолического АД менее 100 мм рт.ст.: 38,1 % среди умерших против 8,5 % среди выживших (p = 0,001). Другие показатели были сопоставимы между группами (табл. 2).
Таблица 2
Результаты инструментального и физикального обследования пациентов с ОДСН
|
Параметр |
Самостоятельное дыхание (n = 129) |
ИВЛ (n = 11) |
р-значение |
|
|
Физикальный осмотр |
||||
|
САД, мм рт. ст. |
132 [109; 156] |
134 [102; 140] |
0,520 |
|
|
ЧСС, уд/мин |
92 [77; 110] |
99 [86; 120] |
0,206 |
|
|
ЧДД, кол-во/мин |
23 [20; 25] |
23 [21; 25] |
0,759 |
|
|
Акроцианоз |
41 (32,0 %) |
9 (81,8 %) |
0,002 |
|
|
Асцит |
19 (14,8 %) |
3 (27,3 %) |
0,380 |
|
|
Ортопноэ |
124 (96,1 %) |
10 (91 %) |
0,369 |
|
|
Инструментальные исследования |
||||
|
SpO2, % |
94 [91; 96] |
94 [89; 96] |
0,569 |
|
|
ФВ ЛЖ, % |
48 [29; 55] |
45 [35; 46] |
0,254 |
|
|
СДЛА, мм рт. ст. |
55 [37; 64] |
56 [47; 61] |
0,822 |
|
|
Диаметр НПВ, см |
2,4 [2,1; 2,6] |
2,3 [2,3; 2,4] |
0,704 |
|
Количественные данные представлены в виде Me [IQR], где Me – медиана, IQR – интерквартильный интервал. Качественные данные представлены в виде абсолютных и относительных частот.
Аббревиатуры: САД – систолическое артериальное давление; ЧСС – частота сердечных сокращений; SpO2 – насыщение кислородом крови (сатурация (пульсоксиметр)); НПВ – нижняя полая вена; СДЛА – среднее давление в легочной артерии; ФВ ЛЖ – фракция выброса левого желудочка.
Примечание: составлена авторами на основе данных, полученных в ходе исследования
Анализ лабораторных данных показал, что концентрация общего белка (59,5 г/л против 67,8 г/л; p = 0,002) и общего билирубина (11,4 мкмоль/л против 17,7 мкмоль/л; p = 0,011) были статистически значимо ниже у пациентов, которым потребовалось проведение ИВЛ при сопоставимости других показателей (табл. 3).
Таблица 3
Лабораторные параметры пациентов с ОДСН при поступлении в ОРИТ
|
Параметр
|
Самостоятельное дыхание (n = 129) |
ИВЛ (n = 11) |
р-значение |
|
Эритроциты, 1012/л |
4,26 [3,82; 4,85] |
3,98 [3,11; 4,86] |
0,234 |
|
Гемоглобин, г/л |
121 [107; 138] |
123 [98; 152] |
0,898 |
|
Гематокрит, % |
36,7 [32,6; 41,0] |
35,3 [29,8; 45,1] |
0,791 |
|
Лейкоциты, 1012/л |
9,26 [6,79; 12,95] |
9,49 [7,10; 20,30] |
0,532 |
|
Креатинин, мкмоль/л |
113,2 [90,9; 149,5] |
139,3 [103,0; 186,0] |
0,187 |
|
Мочевина, ммоль/л |
10,6 [7,4; 13,8] |
12,4 [6,2; 15,7] |
0,749 |
|
СКФ, мл/мин/1,73 м2 |
43,88 [33,65; 60,53] |
36,74 [21,53; 57,59] |
0,330 |
|
Калий, ммоль/л |
4,33 [3,89; 4,72] |
3,94 [3,35; 4,58] |
0,278 |
|
Натрий, ммоль/л |
141,00 [136,61; 144,00] |
142,00 [139,39; 146,85] |
0,199 |
|
Общий билирубин, мкмоль/л |
17,68 [10,26; 29,86] |
11,40 [7,78; 12,33] |
0,011 |
|
Прямой билирубин, мкмоль/л |
4,38 [2,35; 9,08] |
2,53 [1,85; 3,60] |
0,066 |
|
АЛТ, Е/л |
19,9 [12,7; 39,9] |
34,2 [22,4; 132,4] |
0,081 |
|
АСТ, Е/л |
25,7 [19,9; 47,6] |
42,5 [23,2; 127,0] |
0,081 |
|
ЛДГ, Е/л |
278 [222; 368] |
375 [211; 565] |
0,267 |
|
Щелочная фосфатаза, Е/л |
98,7 [79,7; 125,0] |
91,2 [75,9; 113,1] |
0,554 |
|
СРБ, мг/л |
20,86 [9,15; 59,90] |
30,77 [3,88; 124,00] |
0,683 |
|
Общий белок, г/л |
67,81 [61,98; 71,94] |
59,54 [57,21; 65,97] |
0,002 |
|
Альбумин, г/л |
32,47 [29,11; 36,53] |
31,42 [28,30; 36,43] |
0,649 |
|
Глюкоза, ммоль/л, |
6,66 [5,60; 9,26] |
7,53 [6,80; 12,07] |
0,145 |
|
Холестерин, ммоль/л |
3,56 [2,87; 4,50] |
3,61 [2,75; 5,00] |
0,806 |
|
Железо, мкмоль/л |
4,7 [3,0; 7,7] |
6,7 [5,0; 8,0] |
0,400 |
|
Тропонин I, нг/мл |
0,044 [0,02; 0,115] |
0,071 [0,037; 0,113] |
0,257 |
|
NT-proBNP, пг/мл |
1095,6 [265,6; 1747,5] |
656,8 [62,2; 1409,1] |
0,441 |
|
Д-димер, нг/мл |
621 [315; 1698] |
1331 [438; 2754] |
0,240 |
|
МНО, МЕ/мл |
1,38 [1,20; 1,69] |
1,30 [1,25; 1,45] |
0,357 |
Количественные данные представлены в виде Me [IQR], где Me – медиана, IQR – интерквартильный интервал. Качественные данные представлены в виде абсолютных и относительных частот.
Аббревиатуры: NT-proBNP – натрийуретический пептид (N-terminal pro-B-type natriuretic peptide); АЛТ – аланинаминотрансфераза; АСТ – аспартатаминотрансфераза; ЛДГ – лактатдегидрогеназа; МНО – международное нормализованное отношение; СКФ – скорость клубочковой фильтрации; СРБ – С-реактивный белок.
Примечание: составлена авторами на основе данных, полученных в ходе исследования
Частота развития потребности в гемодинамической поддержке (использования вазопрессоров и/или инотропов с целью поддержания среднего АД более 65 мм рт. ст.) была статистически значимо выше в группе с использованием ИВЛ (45,5 % против 15,5 %; р = 0,027). Летальность также была более высокой в группе пациентов с потребностью в ИВЛ (45,5 % против 13,2 %; р = 0,015). Медиана длительности госпитализации в стационаре и в ОРИТ были сопоставимы между группами (табл. 4).
Таблица 4
Исходы госпитализации пациентов с ОДСН
|
Параметр
|
Самостоятельное дыхание (n = 129) |
ИВЛ (n = 11) |
р-значение |
|
Длительность пребывания в ОРИТ, дни |
3 [2; 4] |
6 [2; 6] |
0,055 |
|
Длительность госпитализации в стационаре, дни |
9 [7; 12] |
11 [6; 14] |
0,619 |
|
Гемодинамическая поддержка |
20 (15,5 %) |
5 (45,5 %) |
0,027 |
|
Смерть от любых причин |
17 (13,2 %) |
5 (45,5 %) |
0,015 |
Количественные данные представлены в виде Me [IQR], где Me – медиана, IQR – интерквантильный интервал. Качественные данные представлены в виде абсолютных и относительных частот.
Аббревиатуры: ОРИТ – отделение реанимации и интенсивной терапии.
Примечание: составлена авторами на основе данных, полученных в ходе исследования
По результатам многофакторного регрессионного анализа был выявлен один независимый фактор риска потребности в ИВЛ у пациентов с ОДСН в ОРИТ: акроцианоз при поступлении (ОШ = 8,25; p = 0,016). Дополнительно выявлены два протективных фактора: наличие теплого/сухого фенотипа сердечной недостаточности (ОШ = 0,12; p = 0,008) и общий билирубин более 12,4 (ОШ = 0,11; р = 0,013). На основании полученных данных была построена номограмма прогнозирования потребности в ИВЛ (рис. 2).
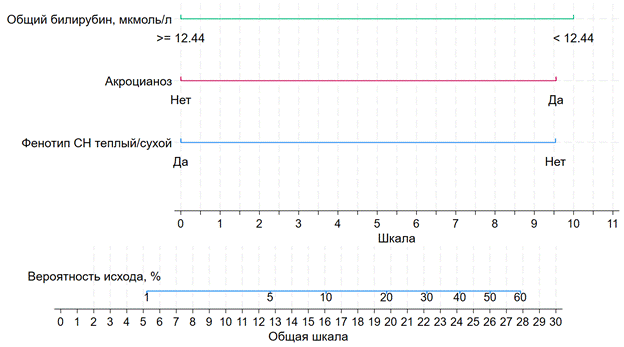
Рис. 2. Номограмма прогнозирования потребности в ИВЛ у пациентов с ОДСН в ОРИТ. Аббревиатуры: СН – сердечная недостаточность.
Примечание: составлен авторами на основе данных, полученных в ходе исследования
Показатель AUROC составил 0,88 (95 % ДИ 0,76–0,99) при оптимальной точке отсечения – 16 баллов. Номограмма продемонстрировала чувствительность 80 %, специфичность 84 % и общую точность 84 %. Отношение шансов составило 21,0 (4,2; 106,3).
Ключевые результаты
Проведено проспективное исследование 140 пациентов с ОДСН в ОРИТ, из них 7,9 % потребовали ИВЛ. По результатам многофакторного анализа, акроцианоз при поступлении был независимым предиктором потребности в ИВЛ (ОШ = 8,25). Протективными факторами являлись фенотип «теплый/сухой» (ОШ = 0,12) и уровень билирубина > 12,4 мкмоль/л (ОШ = 0,11). Созданная прогностическая номограмма показала хорошую дискриминационную способность относительно потребности в ИВЛ (AUROC 0,80; 95 % ДИ 0,76–0,99).
Связь с предыдущими исследованиями
В настоящее время существует ограниченное число работ, посвященных прогнозированию потребности в ИВЛ именно у пациентов с ОДСН, что делает прямое сравнение затруднительным. Наиболее релевантным для сопоставления является исследование Li et al. (2024), разработавших модель машинного обучения для прогноза пролонгированной ИВЛ у пациентов с ХСН [16]. Обе модели демонстрируют сопоставимую и высокую дискриминационную способность (AUROC 0,88 в данном исследовании против AUROC 0,817 в исследовании Li et al.).
Ключевое отличие заключается в характере значимых предикторов, что отражает разницу в дизайне исследований. Модель Li et al. акцентирует объективные маркеры тяжести состояния и полиорганной дисфункции (NT-proBNP, GCS, сепсис, AKI), оцениваемые в течение первых суток в ОРИТ. В противоположность этому представленная авторами номограмма идентифицирует в качестве независимых факторов риска клинические параметры, доступные непосредственно при поступлении: акроцианоз и фенотип ХСН. Это позволяет использовать ее для сверхранней стратификации риска в приемном отделении.
Важно отметить, что выявленные предикторы имеют четкое патофизиологическое обоснование. Акроцианоз является прямым клиническим коррелятом низкого сердечного выброса и периферической вазоконстрикции, что усугубляет тканевую гипоксию и повышает нагрузку на дыхательную мускулатуру. «Теплый/сухой» фенотип ХСН, в свою очередь, отражает более благоприятный гемодинамический профиль с сохраненной периферической перфузией, что снижает вероятность быстрой декомпенсации дыхательной функции. Таким образом, представленная авторами модель не только обладает статистической точностью, но и интегрирует ключевые элементы клинической патофизиологии ОДСН, что усиливает ее обоснованность и потенциальную воспроизводимость в реальной клинической практике.
Клиническая значимость результата
Результаты работы подтверждают практическую ценность созданной номограммы для раннего прогнозирования необходимости респираторной поддержки у больных с острой декомпенсацией сердечной недостаточности в отделении реанимации. Предлагаемый инструмент основан на комплексной оценке, объединяющей клинический признак (акроцианоз), фенотипическую характеристику сердечной недостаточности и стандартный лабораторный маркер (концентрация билирубина).
Использование данной модели при госпитализации позволяет выделить группу высокого риска по развитию дыхательной недостаточности, требующей проведения ИВЛ. Это способствует оптимизации тактики ведения пациентов в условиях ОРИТ, включая своевременное начало интенсивного мониторинга дыхательной функции и планирование методов респираторной поддержки. Инструмент, использующий три легко определяемых параметра, может быть эффективно интегрирован в клинический алгоритм для принятия обоснованных решений в реальном времени.
Сильные и слабые стороны исследования
Сильной стороной работы является ее проспективный характер, включение однородной группы критических пациентов и сторонний сбор данных, охватывающий клинические, анамнестические, лабораторные и инструментальные показатели, что повышает достоверность сделанных выводов.
К ограничениям следует отнести проведение исследования на базе одного центра и ограниченный объем выборки. Это может влиять на мощность статистического анализа и ограничивает возможности для широкой генерализации результатов. Для подтверждения эффективности и воспроизводимости предложенная прогностическая модель нуждается в дальнейшей валидации на независимых, более многочисленных и многоцентровых когортах.
Заключение
В рамках проведенного исследования была создана номограмма для оценки риска развития необходимости в искусственной вентиляции легких у пациентов с ОДСН, госпитализированных в ОРИТ. Модель, учитывающая наличие акроцианоза, фенотип сердечной недостаточности и уровень общего билирубина, показала высокую дискриминационную способность.
Конфликт интересов
Библиографическая ссылка
Вацик-Городецкая М.В., Малюк Д.И., Берикашвили Л.Б., Короленок Е.М. ПРОГНОЗИРОВАНИЕ ПОТРЕБНОСТИ В ИСКУССТВЕННОЙ ВЕНТИЛЯЦИИ ЛЕГКИХ У ПАЦИЕНТОВ С ОСТРОЙ ДЕКОМПЕНСАЦИЕЙ СЕРДЕЧНОЙ НЕДОСТАТОЧНОСТИ // Современные проблемы науки и образования. 2025. № 6. ;URL: https://science-education.ru/ru/article/view?id=34390 (дата обращения: 20.05.2026).
DOI: https://doi.org/10.17513/spno.34390



