Введение
Псориаз – рецидивирующее воспалительное заболевание кожи, сопровождающееся различными сопутствующими осложнениями. Заболевание в значительной степени распространенное. Так, по состоянию на 2019 г. по всему миру было зарегистрировано более 4,5 млн случаев заболевания псориазом. При этом наиболее высокий уровень заболеваемости регистрируется в странах с высоким уровнем социально-экономического развития (112,6 на 100 тыс. чел., 95 % доверительный интервал (ДИ) 108,9–116,1), частота выявления зависит также от возраста и географического региона, его численность выше в странах, расположенных дальше от экватора [1, 2].
В структуре системных поражений выделяют несколько клинических форм псориаза. Медицинские возможности в лечении пациентов с псориазом существенно расширились, однако существующие методы лечения лишь облегчают симптомы, но не излечивают болезнь у значительной части пациентов.
Псориаз связан с другими серьезными заболеваниями, такими как сердечно-сосудистые, злокачественные заболевания эндокринные патологии, психоневрологические состояния. Наиболее распространенным осложнением является псориатический артрит [3, 4]. Псориаз заметное негативное влияние оказывает на качество жизни пациентов [5]. Кроме того, псориаз добавляет весомую долю к учету смертности населения от всех причин [6]. Наибольшее число случаев приходится на вульгарный или бляшечный псориаз – порядка 90 % от всех случаев. Эта форма также связана с рядом сопутствующих заболеваний, включая псориатический артрит, кардиометаболические заболевания и депрессию [7].
Глубокое понимание патогенеза псориаза помогает находить новые терапевтические мишени и разрабатывать эффективные инновационные методы лечения, поэтому оно имеет важное клиническое значение.
Генно-инженерные биологические препараты являются препаратами для лечения при неэффективности традиционных методов. Моноклональные антитела (мАт) используются при разработке методов иммунотерапии, направленных на борьбу с различными заболеваниями, такими как аутоиммунные патологии, включая псориаз и его среднетяжелые и тяжелые формы. Использование биологических препаратов произвело революцию в лечении пациентов с псориазом, но выбор правильного препарата может оказаться сложной задачей. В настоящее время существует множество биологических препаратов, каждый из которых имеет свои преимущества и недостатки [8].
Для пациентов с легким псориазом наружная терапия остается основой лечения, и она включает кортикостероиды для дерматологического применения, аналоги витамина D, ингибиторы кальциневрина и кератолитики. Биологические препараты рекомендуются для лечения средней и тяжелой степени течения псориаза. Эта группа препаратов эффективна и имеет высокий профиль безопасности.
Псориаз характеризуется чрезвычайно сложным иммунологическим патогенезом, затрагивающим как врожденную, так и адаптивную иммунную систему (рис. 1).
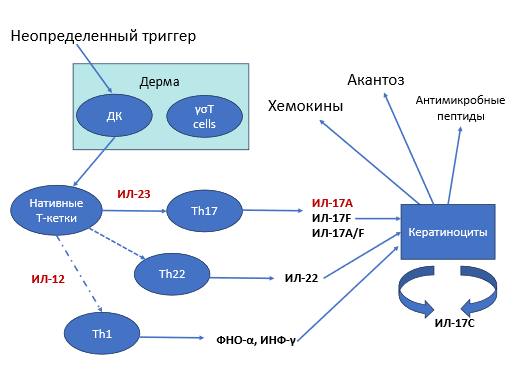
Рис. 1. Патогенез псориаза: ДК – дермальные клетки, ИЛ – интерлейкин, Th1 – Т-хелперы 1-го типа, Th17 – Т-хелперы 17-го типа, Th22 – Т-хелперы 22-го типа, ФНО-α – фактор некроза опухоли α, ИНФ-γ – интерферон-гамма.
Примечание: составлен авторами на основе источника [9]
Нарушение активности Т-клеток приводит к гиперпролиферации и аномальной дифференцировке кератиноцитов, которые привлекают дендритные клетки, высвобождающие интерлейкин (ИЛ)-12 и 23. ИЛ-22 и ИЛ-23 активируют два типа Т-клеток: Т-хелперы 1 (Th1) и Т-хелперы 17 (Th17), которые высвобождают псориатические цитокины ИЛ-17, интерферон (ИФН)-γ, фактор некроза опухоли (ФНО)-α и ИЛ-22. Ключевую роль в патогенезе псориаза играет цитокиновый каскад. Первым пусковым цитокином является ФНО-α. Блокирование этого цитокина является эффективным методом лечения псориаза. Группа ингибиторов ФНО-α включают этанерцепт, адалимумаб, цертолизумаб и инфликсимаб [10].
Альтернативные биологические препараты нацелены на ингибирование интерлейков: устекинумаб блокирует субъединицы p40 ИЛ-12 и ИЛ-13, секукинумаб, иксекизумаб, бимекизумаб и бродалумаб нацелены на ИЛ-17; гуселькумаб, тилдракизумаб, рисанкизумаб и мирикизумаб направлены на ингибирование субъединицы p19 ИЛ-23. Для лечения пациентов с псориатическим артритом одобрены также биологические препараты, которые ингибируют ФНО-α, p40ИЛ-12/23 и ИЛ-17.
В состав пероральных лекарственных средств для лечения псориаза включают традиционные препараты, такие как ацитретин, метотрексат, циклоспорин и модифицированные ингибитор фосфодиэстеразы 4 – апремиласт.
Для изменения физиологических процессов в коже с целью достижения ремиссии кожных заболеваний в составе фототерапии используется многократное контролируемое воздействие ультрафиолетового (УФ) излучения. Наиболее часто назначаемая фототерапия, используемая для лечения бляшечного псориаза, – это узкополосная УФ-В-фототерапия (UVB) с длиной волны от 280 до 320 нм [11]. Сочетание фототерапии в режиме узкополосного В-излучения с режимом А (UVA) с длиной волны от 320 до 400 нм и псораленом (природное соединение из группы линейных фуранокумаринов) хорошо зарекомендовало себя как метод лечения псориаза [12].
Фактор некроза опухоли α (ФНО-α) – провоспалительный цитокин, играет важную роль в патогенезе псориаза. У пациентов с псориазом повышенные уровни ФНО-α в коже и сыворотке крови, которые значимо коррелируют с тяжестью заболевания. После успешного лечения псориаза уровни ФНО-α снижаются до нормальных значений [13, 14].
Адалимумаб представляет собой рекомбинантное, полностью человеческое, моноклональное антитело против ФНО-α. Он с высокой специфичностью связывается с ФНО-α и блокирует его взаимодействие с рецепторами p55, так и с p75, нейтрализуя биологическую активность. Адалимумаб хорошо зарекомендовал себя для лечения хронического псориаза средней и тяжелой степени у взрослых и совсем недавно был одобрен в Европейском союзе для применения у детей с тяжелым хроническим бляшечным псориазом.
Иксекизумаб представляет собой гуманизированное моноклональное антитело к интерлейкину 17А (ИЛ-17А и ИЛ-17A/F), относящемуся к подклассу иммуноглобулинов G4 (IgG4), продемонстрировал эффективность и безопасность при лечении бляшечного псориаза средней и тяжелой степени. Препарат проявляет иммунодепрессивное влияние, эффективно взаимодействует с мишенью ИЛ17A, нейтрализуя его, снижая воспаление и его патологические последствия. Иксекизумаб одобрен к применению в Российской Федерации и в Европейском союзе. Препарат назначают взрослым пациентам с бляшечным псориазом средней и тяжелой степени в активной фазе, которым назначена комплексная терапия или фототерапия, а также его применяют для лечения пациентов с активным псориатическим артритом [15].
Цель исследования – определение безопасности применения адалимумаба и иксекизумаба в лечении пациентов с псориазом.
Материал и методы исследования
В исследовании приняли участие 140 пациентов, из них 87 (62,14 %) мужчин и 53 (37,86 %) женщины в возрасте 18–60 лет (средний возраст 38,2±11,7 лет). У всех участников исследования был подтвержден диагноз бляшечного (вульгарного) псориаза. Все участники исследования получили информацию о предстоящем исследовании, в соответствии с принятым порядком дали письменное согласие на участие в нем.
Пациенты были разделены на две равные группы по 70 чел. методом случайных чисел. Первой группе пациентов была назначена терапия препаратом адалимумаб, второй группе – препаратом иксекизумаб. Оценку эффективности лечения проводили через 4, 8, 12, 56 недель лечения и через 2 года.
Все участники исследования проходили медицинское обследование согласно Российским клиническим рекомендациям по диагностике и лечению пациентов с псориазом. Были проведены клинический и биохимический анализ крови, клинический анализ мочи, наличие антител на инфекции (вирусные гепатиты, вирус иммунодефицита человека (ВИЧ), сифилис). Общеклинические анализы проводились один раз в две недели.
Результаты исследования и их обсуждение
Участники исследования обеих групп переносили терапию хорошо. В каждой группе исследования наблюдалось по одному сердечно-сосудистому осложнению: в группе применения иксекизумаба была установлена синусовая аритмия, в группе применения адалимумаба – тахикардия. Осложнения были купированы самостоятельно и не требовали назначения специального лечения или отмены препарата.
В первой группе у двоих пациентов также был установлен стоматит. Во второй группе стоматит ни у кого не регистрировали. Тромбоцитопения была установлена только у одного пациента первой группы, во второй группе тромбоцитопении выявлено не было. В обеих группах не отмечено других нежелательных реакций и осложнений, которые требовали бы отмены препарата (рис. 2).
В группе пациентов, получавших адалимумаб, было выявлено больше побочных реакций, чем в группе иксекизумаб (2,9 % против 0,7 % соответственно).
Таким образом, в группе, получавшей адалимумаб, количество побочных эффектов и нежелательных явлений было выше, чем в группе пациентов, получавших иксекизумаб. Можно сделать вывод о хорошей клинической переносимости обоих препаратов. Побочные эффекты от проводимой терапии в обеих группах имели легкое течение и не требовали отмены препаратов, часто регрессировали самостоятельно даже без отмены препаратов.
Полученные результаты демонстрируют некоторое сходство с опубликованными другими исследователями данными.
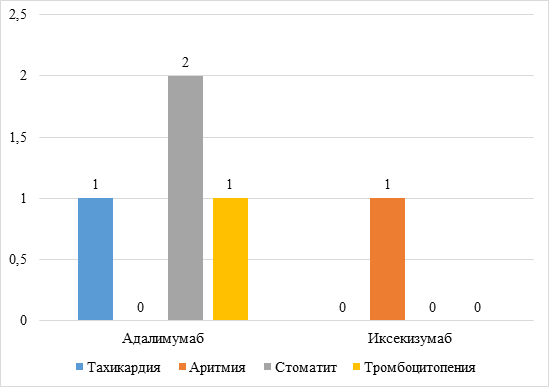
Рис. 2. Побочные эффекты от терапии в обеих группах пациентов с псориазом.
Примечание: составлен авторами на основе собственных исследований
W.M. Wang с соавт. (2020) провели исследование с целью сравнения безопасности биологической терапии в лечении пациентов с псориазом. Пациенты с вульгарным псориазом, получавшие биологические препараты, продемонстрировали выраженный положительный эффект от проводимого лечения. Авторы пришли к мнению, что ингибиторы ФНО-α являются наиболее доступными биологическими препаратами для лечения пустулезного псориаза, а ингибиторы ИЛ-12/23 и ИЛ-17A могут рассматриваться в качестве терапии первой или второй линии при лечении вульгарного псориаза средней и тяжелой степени, рефрактерного к лечению [16].
S.K. Mahil с соавт. (2020) сравнили безопасность и переносимость биологических препаратов пациентами с псориазом. Все биологические препараты были эффективнее по сравнению с плацебо или метотрексатом через 10–16 недель. Анализ показал, что адалимумаб, бродалумаб, цертолизумаб, гуселькумаб, рисанкизумаб, секукинумаб, тилдракизумаб и устекинумаб были сопоставимы в отношении высокой краткосрочной эффективности и переносимости. Инфликсимаб и иксекизумаб авторы отнесли к препаратам с высокой краткосрочной эффективностью, но относительно более низкой переносимостью, чем другие препараты, хотя количество случаев отмены препарата в ходе исследования было низким, поэтому к этим результатам следует относиться с осторожностью [17]. Авторы установили, что большинство биологических препаратов объединяются в группы по кратковременной эффективности. Эти данные необходимо интерпретировать в контексте долгосрочной эффективности, данных об эффективности, безопасности, дозировки и затрат на приобретение лекарств при принятии решений о лечении.
В исследовании A. Blauvelt с соавт. (2020) с включением 646 пациентов с псориазом, принимавших иксекизумаб, и 3668 пациентов, принимавших адалимумаб, наблюдение вели в среднем 14,0 и 16,5 месяцев соответственно. Применение иксекизумаба было связано со снижением рисков отсутствия персистенции на 19 % по сравнению с адалимумабом, (отношение рисков [ОР] = 0,81, 95 % доверительный интервал [ДИ]: 0,69–0,95), 26 % снижением риска прекращения лечения (ОР = 0,74, 95 %ДИ: 0,62–0,88) и 28 % снижением риска перехода на другой препарат (ОР = 0,72, 95 % ДИ: 0,57–0,91). Тем самым пациенты с псориазом, получавшие иксекизумаб, демонстрировали более длительную ремиссию, более высокую приверженность лечению и меньшую вероятность прекращения лечения или перехода на другой препарат по сравнению с пациентами, получавшими адалимумаб. При этом, по сравнению с пациентами, получающими адалимумаб, у пациентов с псориазом, начавших лечение иксекизумабом, как правило, было хуже общее состояние здоровья и они чаще не реагировали на предыдущие биологические препараты [18].
Таким образом, биологические препараты являются эффективными и безопасными методами лечения псориаза средней тяжести и тяжелого течения, резистентного к стандартным традиционным методам лечения. Генно-инженерные биологические препараты относительно безопасны в лечении псориаза. Однако в процессе накопления данных об эффективности и безопасности имеются определенные противоречия, которые необходимо устранять путем дополнительных сравнительных исследований.
Заключение
Проведенное исследование показало, что оба исследованных генно-инженерных биологических препарата – адалимумаб и иксекизумаб – обладают высоким профилем безопасности и хорошей переносимостью при лечении пациентов с псориазом средней и тяжелой степени. Наиболее часто при терапии генно-инженерными препаратами возникали нарушения сердечного ритма, тромбоцитопения и стоматит. Несмотря на небольшие различия в частоте неблагоприятных явлений, оба препарата не потребовали отмены терапии. Таким образом, генетически-инженерные биологические препараты представляют собой эффективную и безопасную альтернативу традиционным методам терапии псориаза. Данное исследование будет способствовать расширению понимания возможностей терапии пациентов с псориазом генно-инженерными препаратами и совершенствованию медицинской помощи таким больным.
Конфликт интересов
Библиографическая ссылка
Сарсур Ш.Х., Руднева Н.С. АНАЛИЗ РИСКОВ И НЕЖЕЛАТЕЛЬНЫХ ЯВЛЕНИЙ ИНГИБИТОРОВ TNF-Α И IL-17A ПРИ ПСОРИАЗЕ // Современные проблемы науки и образования. 2025. № 5. ;URL: https://science-education.ru/ru/article/view?id=34328 (дата обращения: 31.05.2026).
DOI: https://doi.org/10.17513/spno.34328



