Введение
Торакотомия является традиционным методом доступа в грудную полость и остается актуальной в настоящее время, несмотря на стремительное развитие миниинвазивных методов в хирургии. Однако данный вариант доступа имеет ряд недостатков, которые могут отрицательно влиять на течение послеоперационного периода. К наиболее распространенным осложнениям торакотомии как доступа к органам грудной полости относятся развитие инфекции области хирургического вмешательства и выраженный болевой синдром в послеоперационном периоде. Выраженный болевой синдром в послеоперационном периоде способствует ограничению функции внешнего дыхания и продуктивного кашля, что может провоцировать развитие респираторных осложнений (ателектаз, пневмония, дыхательная недостаточность) [1]. Кроме того, в одном из зарубежных исследований было продемонстрировано, что выраженный болевой синдром в послеоперационном периоде способствует развитию формирования хронической постторакотомной боли [2]. Согласно данным отечественных и зарубежных исследователей, инфекция области хирургического вмешательства остается серьезной проблемой, несмотря на совершенствование хирургической техники и тщательного периоперационного ведения пациентов [3]. Разрабатываемые методики по снижению болевого синдрома и профилактике инфекции области хирургического вмешательства (ИОХВ) не обеспечивают в полной мере решения указанных проблем. Поэтому требуется поиск оптимального ведения пациентов в раннем послеоперационном периоде, которым было выполнено вмешательство на органах грудной клетки путем использования торакотомного доступа.
Целью данной работы является описание новой методики комплексного ведения торакотомной раны и ее применение на практике у пациентов с операциями на грудной полости.
Материалы и методы исследования
Работа проводилась на базе хирургического отделения торакальной онкологии ГУЗ «Областной клинический онкологический диспансер» г. Ульяновска. Методика применялась у 10 пациентов, которым была выполнена стандартная боковая торакотомия для операции на органах грудной полости (анатомическая резекция легкого в объеме лобэктомия). Все пациенты дали информированное добровольное согласие на применение методики, исследование было одобрено этическим комитетом ГУЗ ОКОД. Оценивались клинические данные исследуемых пациентов. С целью оценки эффективности метода оценивался болевой синдром по визуально-аналоговой шкале (ВАШ) [4], определялся уровень кортизола до операции, на 1 сутки и на 5 сутки после оперативного вмешательства. Проводилась оценка функции внешнего дыхания до операции, на 1 сутки и на 5 сутки после оперативного вмешательства.
Таблица 1
Клинические данные исследуемых пациентов
|
Показатели |
M ± SD/Me |
95 % ДИ / Q₁–Q₃ |
|
Возраст, M ± SD |
66,27 ± 4,22 |
63,44–69,11 |
|
Пол, абс. (%) |
Жен. |
2 (18,2) |
|
Муж. |
8 (81,8) |
|
|
Продолжительность операции (мин), M ± SD |
103,18 ± 25,33 |
86,17–120,20 |
|
Кровопотеря (мл), Me |
80,00 |
50,00–180,00 |
|
ОФВ, M ± SD (%) |
95,91 ± 11,25 |
88,35–103,46 |
|
ЖЕЛ, Me (%) |
96,00 |
87,50–98,50 |
|
ФЖЕЛ, Me (%) |
99,00 |
91,00–100,50 |
|
Индекс Чарлсона, M ± SD (баллы) |
4,36 ± 0,81 |
3,82–4,91 |
|
Уровень кортизола (нг/мл), Me |
89,00 |
87,50–102,50 |
Источник: составлено авторами на основе собственных данных.
Примечание. ОФВ – объем форсированного выдоха; ЖЕЛ – жизненная емкость легких;
ФЖЕЛ – форсированная жизненная емкость легких.
Послеоперационный период был стандартный: применялись опиоидные анальгетики: р-р трамадола 50 мг/мл – 2 мл в/м 4 раза в день, нестероидные противовоспалительные препараты (НПВП) при отсутствии эффекта обезболивания, антибактериальная терапия проводилась согласно рекомендациям СКАТ [5], непрямые антикоагулянты в стандартных дозировках (р-р эноксапарин натрия 0,4 п/к 1 раз в 24 ч).
Предлагаемый способ комплексной профилактики развития ИОХВ и снижение болевого синдрома выполняется следующим образом. После завершения оперативного пособия производится постановка первой трубки (эпидуральный катетер) в субплевральное пространство, ближе к реберно-позвоночному углу с целью воздействовать на расстоянии на 2–3 межреберья. При этом катетер заводится под «целую» плевру на глубину 4–6 см (рис. 1). Катетер выводится через латеральный край торакотомной раны и подключается к помпе с бупивакаином со скоростью 4–5 мл/ч в течение трех суток. Далее используется непрерывный полиспастный шов PDX–1–0, для сближения ребер. После этого происходит ушивание мышц грудной клетки непрерывным узловым швом на атравматичной игле викрил 2–0, и после этого на ушитые мышцы устанавливается второй катетер (рис. 2). Катетер имеет множество перфоративных отверстий на протяжении всего расположения его в ране. Второй катетер имеет роль комбинированного влияния, он устанавливается через медиальный край раны, далее производится болюсное введение в течение трех суток повидон-йод 20 мл 1 раз с интервалом в 8 ч, с целью профилактики ИОХВ, и также вводится бупивакаин – помпой со скоростью 2–3 мл/ч. Далее кожа ушивается отдельными узловыми швами (рис. 3). Такое расположение катетеров позволяет обеспечивать непрерывную инфузию анестетика и периодическое введение антисептика, что создает оптимальные условия для обезболивания и эффективной профилактики инфекционных осложнений.
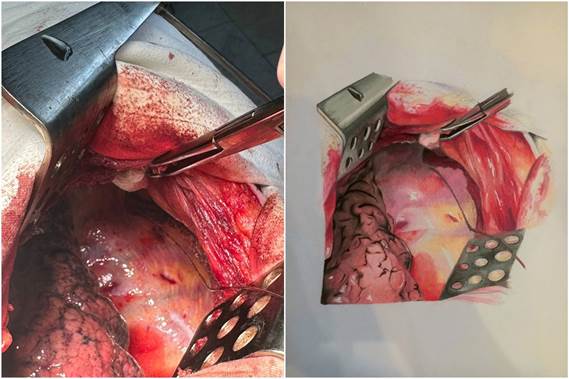
Рис. 1. Вид установленного катетера в субплевральном пространстве.
Источник: фото и иллюстрация авторов
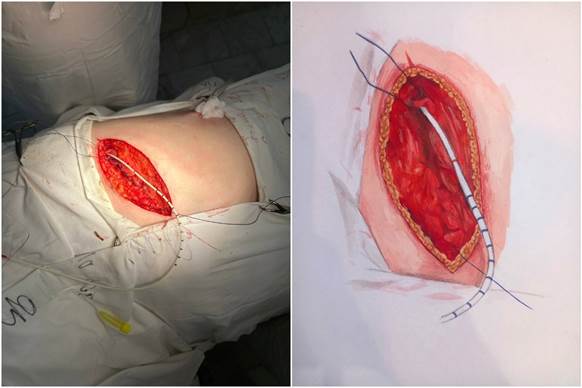
Рис. 2. Введение второго катетера в один из слоев раны.
Источник: фото и иллюстрация авторов
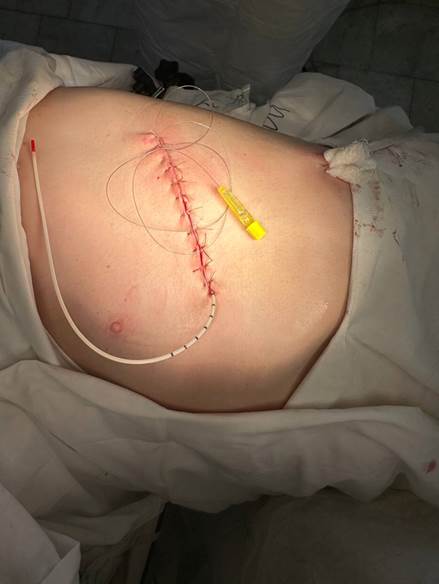
Рис. 3. Вид послеоперационной раны с введенными катетерами.
Источник: фото авторов
Статистический анализ проводился с использованием программы StatTech v. 4.8.2 (разработчик – ООО «Статтех», Россия).
Количественные показатели оценивались на предмет соответствия нормальному распределению с помощью критерия Шапиро – Уилка (при числе исследуемых менее 50) или критерия Колмогорова – Смирнова (при числе исследуемых более 50). Количественные показатели, выборочное распределение которых соответствовало нормальному, описывались с помощью средних арифметических величин (M) и стандартных отклонений (SD). В качестве меры репрезентативности для средних значений указывались границы 95 % доверительного интервала (95 % ДИ). В случае отсутствия нормального распределения количественные данные описывались с помощью медианы (Me) и нижнего и верхнего квартилей (Q1–Q3). Категориальные данные описывались с указанием абсолютных значений и процентных долей. Сравнение двух групп по количественному показателю, распределение которого в каждой из групп соответствовало нормальному, при условии равенства дисперсий выполнялось с помощью t-критерия Стьюдента. Сравнение двух групп по количественному показателю, распределение которого отличалось от нормального, выполнялось с помощью U-критерия Манна – Уитни. Сравнение процентных долей при анализе четырехпольных таблиц сопряженности выполнялось с помощью точного критерия Фишера (при значениях минимального ожидаемого явления менее 10). В качестве количественной меры эффекта при сравнении относительных показателей рассчитывалось отношение шансов с 95 % доверительным интервалом (ОШ; 95 % ДИ). Различия считались статистически значимыми при p < 0,05.
Результаты исследования и их обсуждение
В табл. 2 указаны результаты пациентов при оценке болевого синдрома по ВАШ, а также уровень кортизола в динамике лечения.
Таблица 2
Показатели болевого синдрома
|
Показатели |
M ± SD / Me |
95 % ДИ / Q₁–Q₃ |
|
ВАШ 1 сут, M ± SD |
8,45 ± 1,04 |
7,76–9,15 |
|
ВАШ 5 сут, Me |
5,00 |
4,00–5,00 |
|
Уровень кортизола 1 сут (нг/мл), Me |
177,00 |
171,50–178,00 |
|
Уровень кортизола 5 сут (нг/мл), M ± SD |
144,73 ± 5,29 |
141,17–148,28 |
Источник: составлено авторами на основе собственных данных.
Примечание. ВАШ – визуально-аналоговая шкала.
В табл. 3 представлены показатели функции внешнего дыхания на фоне проводимого лечения с предлагаемым способом.
Таблица 3
Показатели внешнего дыхания
|
Показатели |
M ± SD / Me |
95 % ДИ / Q₁–Q₃ |
|
ОФВ 1 сут, M ± SD |
81,64 ± 8,70 |
75,79–87,48 |
|
ОФВ 5 сут, M ± SD |
90,00 ± 12,98 |
81,28–98,72 |
|
ЖЕЛ 1 сут, M ± SD |
79,18 ± 5,36 |
75,58–82,78 |
|
ЖЕЛ 5 сут, M ± SD |
85,36 ± 8,72 |
79,50–91,22 |
|
ФЖЕЛ 1 сут, Me |
86,00 |
79,50–90,00 |
|
ФЖЕЛ 5 сут, M ± SD |
91,64 ± 6,02 |
87,59 – 95,68 |
Источник: составлено авторами на основе собственных данных.
Примечание. ОФВ – объем форсированного выдоха; ЖЕЛ – жизненная емкость легких; ФЖЕЛ – форсированная жизненная емкость легких.
У всех пациентов послеоперационная рана зажила первичным натяжением, болевой синдром был умеренным и позволил на 3-е сутки после операции отменить прием опиоидных анальгетиков. Послеоперационных осложнений в виде развития ИОВХ не отмечено. Безопасность методики оценивалась согласно критериям CTCAE (Common Terminology Criteria for Adverse Events, версия 5.0). В большинстве случаев наблюдались только легкие нежелательные явления (Grade 1). Данные осложнения были представлены дискомфортом в области постановки катетеров. Данные осложнения не требовали дополнительного лекарственного воздействия и не влияли на общее состояние участников исследования. Указанный профиль осложнений подтверждает приемлемый профиль безопасности предлагаемой методики.
Согласно проведенным исследованиям, направленным на оценку методов обезболивания и профилактики ИОХВ после торакотомии, выявлено, что каждый из известных методов имеет свои ограничения и риски. Так, в работе Д.В. Базарова и соавт. описаны различные методики обезболивания раны, однако ни одна из них не является идеальной [6]. Все это подчеркивает важность дальнейших разработок способов ведения раны после проведенной торакотомии.Болевой синдром является неизбежной составляющей большинства хирургических вмешательств, особенно операций, требующих использования обширного хирургического доступа. Интенсивность и длительность боли, возникающей после таких операций, значительно осложняют течение послеоперационного периода. Эффективное снижение болевого синдрома становится критически важным фактором успешной реабилитации и улучшения общего прогноза лечения. В настоящее время описано множество способов послеоперационного обезболивания пациентов, каждый из которых обладает своими недостатками [7].
Широкое применение в хирургии получили опиоидные анальгетики, что обусловлено их высоким анальгезирующим эффектом. Однако эта группа препаратов сопряжена с серьезными побочными эффектами, поэтому их использование требует тщательного контроля и минимизации дозировок. В крупном метаанализе Izrailtyan и соавт. было наглядно продемонстрировано влияние использования опиоидных анальгетиков на развитие кардиореспираторных осложнений у пациентов [8].
В настоящее время отмечается растущая тенденция к внедрению протокола ускоренного послеоперационного восстановления пациентов (ERAS), важным элементом которого является применение мультимодальной анальгезии. Мультимодальная анальгезия предполагает использование комбинации методов обезболивания, что позволяет минимизировать введение каждого препарата, сокращая количество побочных эффектов. Использование нестероидных противовоспалительных препаратов дает возможность уменьшить дозировку опиоидных анальгетиков, а в некоторых случаях и полностью отказаться от их применения [9, 10]. Современные нестероидные противовоспалительные препараты имеют ряд побочных эффектов, среди которых выделяются риски желудочно-кишечных кровотечений и высокие сердечно-сосудистые риски, особенно у пациентов с предрасположенностью к таким осложнениям. Это подтверждается данными крупного метаанализа, опубликованного в журнале The Lancet в 2013 г., который демонстрирует повышенную вероятность этих побочных эффектов при использовании НПВП [11].
В ряде исследований зарубежных авторов была наглядно продемонстрирована эффективность непрерывной периплевральной инфузии анестетика. Так, в рандомизированном клиническом исследовании Magoon и соавт. средние показатели боли по визуально-аналоговой шкале были статистически значимо ниже в группе пациентов, которым проводилась периплевральная инфузия анестетика, по сравнению с пациентами, у которых применялась блокада межреберных нервов. Эти результаты подтверждают эффективность описанной методики [12].
Торакотомия сопряжена с высоким риском развития ИОХВ, что особенно важно учитывать при ведении пациентов, которые составляют группу высокого риска [13, 14]. В связи с этим возникает необходимость в качественной профилактике данного осложнения. Одним из основных способов профилактики ИОХВ является периоперационная антибиотикопрофилактика, однако ее эффективность снижается с ростом антибиотикорезистентности [15]. Одним из возможных подходов к профилактике ИОХВ у пациентов высокого риска является орошение раны раствором антисептика. Предпочтение отдается раствору повидон-йода, поскольку он обладает наименее выраженным цитотоксическим эффектом. В крупном метаанализе, проведенном Fu и соавт., была доказана эффективность и безопасность ирригации раны раствором повидон-йода на снижение развития ИОХВ после хирургических вмешательств [16].
Предложенный авторами комбинированный способ послеоперационного ведения торакотомной раны обладает рядом преимуществ, к которым относятся эффективность, безопасность, экономическая доступность и относительная простота выполнения. При данном способе ведения торакотомной раны наблюдается ускорение процесса заживления, снижение риска развития инфекционных осложнений, а также эффективное обезболивание.
Заключение
Использование предложенного метода в клинической практике способно уменьшить риск развития инфекции области хирургического вмешательства после оперативных вмешательств на грудной клетке путем использования торакотомного доступа, а также обеспечить эффективное обезболивание.
Работа выполнялась в соответствии с планом научных исследований медицинского факультета им. Т.З. Биктимирова, Института медицины, экологии и физической культуры, ФГБОУ ВО «Ульяновский государственный университет», г. Ульяновск, Россия.
Финансовой поддержки со стороны компаний – производителей лекарственных препаратов авторы не получали.
Исследование одобрено этическим комитетом ГУЗ «Областной клинический онкологический диспансер» и ФГБОУ ВО «Ульяновский государственный университет», г. Ульяновск.
Авторы заявляют, что конфликт интересов отсутствует.
Конфликт интересов
Финансирование
Библиографическая ссылка
Вдовин А.М., Смолькина А.В., Тонеев Е.А., Мухутдинова А.Н., Шагдалеев Р.Ф., Белоногов Н.И., Кешян Э.А., Мамадалеева М.А. КОМПЛЕКСНОЕ ВЕДЕНИЕ ТОРАКОТОМНОЙ РАНЫ ПОСЛЕ ОПЕРАЦИЙ НА ГРУДНОЙ ПОЛОСТИ // Современные проблемы науки и образования. 2025. № 3. ;URL: https://science-education.ru/ru/article/view?id=34097 (дата обращения: 29.04.2026).
DOI: https://doi.org/10.17513/spno.34097



