Введение
Несмотря на многолетние исследования наркотической зависимости, многие клеточно-молекулярные механизмы ее формирования остаются неизвестными, что существенно ограничивает возможности разработки средств для лечения наркомании. В последние годы появилось большое количество работ по изучению участия в развитии зависимости эпигенетических механизмов, таких как посттрансляционные модификации гистонов, метилирование ДНК, изменения экспрессии некодирующих РНК, и на основании полученных данных были предложены новые подходы к терапии зависимости от наркотиков [1, 2]. К некодирующим РНК относятся и молекулы микроРНК, размер которых в зрелом состоянии составляет 18–22 нуклеотида и которые обладают широким спектром действия, регулируя активность генов на уровне трансляции. В развивающейся нервной системе микроРНК участвуют в пролиферации и дифференцировке клеток, в миграции нейробластов и формировании связей, в зрелой нервной ткани – в поддержании ее нормальной функциональной активности, в частности синаптической пластичности [3]. Активно изучается роль микроРНК в обучении и формировании долговременной памяти [4].
В представленной работе для анализа экспрессии были выбраны две микроРНК – miR-9-3p и miR-132-3p. Обе микроРНК высококонсервативны, ортологичны соответствующим микроРНК человека, обладают высоким уровнем экспрессии в нервной ткани и участвуют в регуляции синаптической пластичности [5, 6].
Для хронической зависимости у человека и животных характерно снижение когнитивных способностей с нарушением обучения и памяти, что обусловлено модификацией синаптической пластичности и реорганизацией нейронных систем в связанных с зависимостью структурах мозга [7]. Гиппокамп – структура мозга, непосредственно вовлеченная в обучение и память. Экспериментально доказано, что при опиоидной зависимости нарушается синаптическая пластичность гиппокампа [8]. Если в самых ранних исследованиях гиппокамп рассматривали как однородную структуру, то впоследствии была обнаружена асимметрия гиппокампа вдоль дорзовентральной оси, при этом дорзальный гиппокамп сильнее связан с оценкой новизны информации, пространственной и оперативной памятью, а вентральный – с эмоциональными компонентами памяти [9]. Кроме этого, появились данные о функциональных и клеточно-молекулярных различиях левого и правого гиппокампов [10]. Поэтому в данной работе анализировали изменения экспрессии микроРНК при разделении гиппокампа на отделы – правый вентральный и дорзальный (RV и RD) и левый вентральный и дорзальный (LV и LD).
Цель исследования
Изучение влияния хронического употребления морфина на уровень экспрессии микроРНК miR-9-3p и miR-132-3p в отделах гиппокампа мышей линии C57Bl/6.
Материалы и методы исследования
Работу проводили на самцах мышей инбредной линии C57Bl/6 в возрасте 1,5 месяца, весом 24–26 г, полученных из вивария НИИНМ. Животных содержали при световом режиме 12/12 ч день/ночь при температуре 21–22оС на стандартном рационе кормления со свободным доступом к воде и пище.
Все процедуры проводили в соответствии с законодательством Российской Федерации и Директивой Европейского парламента и Совета Европейского Союза 2010/63/ЕС от 22.09.2010 г. о защите животных, использующихся для научных целей, протокол эксперимента был утвержден Комитетом по биомедицинской этике НИИМББ ФИЦ ФТМ.
Животных с хронической зависимостью от морфина получали в соответствии с протоколами, описанными ранее [11, 12].
Кратко:
Мышей разделяли на две группы: опытную (1) и контрольную (2), по 6 мышей в каждой. В течение 5 дней дважды в сутки (в 9.00 и в 18.00) животным группы 1 делали инъекции морфина гидрохлорида (10 мг/кг веса) (ФГУП «Московский эндокринный завод»), а мышам группы 2 вводили физиологический раствор в том же объеме. На 6-е сутки, в 9.00 мышам делали последнюю инъекцию, через 2 часа производили эвтаназию животных методом цервикальной дислокации, затем от каждого животного брали по 4 образца гиппокампа в соответствии с двумя типами асимметрии (LV, LD, RV, RD). Образцы помещали в пробирки, замораживали в жидком азоте и хранили при температуре –70оС. Затем в образцах определяли уровень экспрессии miR-9-3p и miR-132-3p методом полимеразной цепной реакции (ПЦР) в режиме реального времени. Выделение тотальной РНК производили термоиндуцированным лизисом с помощью лизирующего раствора на основе гуанидина тиоцианата (4 М гуанидин изотиоцианат, 25 мМ цитрат натрия, 0,3%-ный саркозил, 0,1%-ный 2-меркаптоэтанол, 25 мM ацетата натрия).
Реакцию обратной транскрипции проводили с использованием коммерческого набора RT-M-MuLV-RH (БиолабМикс, Россия) и «stem-loop» праймеров, которые подбирали на основе последовательности зрелых исследуемых микроРНК и референсной РНК U68. Использовали следующие последовательности праймеров:
1. U68
5’-GTCGTATCCAGTGCAGGGTCCGAGGTATTCGCACTGGATACGACCATCAGAT - 3’
2. miR-9-3р
5’- GTCGTATCCAGTGCAGGGTCCGAGGTATTCGCACTGGATACGACACTTTCG - 3’
3. miR-132-3р
5’- GTCGTATCCAGTGCAGGGTCCGAGGTATTCGCACTGGATACGACCGACCAT - 3’
Полученную комплементарную ДНК (кДНК) использовали для определения уровней экспрессии miR-9-3р и miR-132-3p методом ПЦР в режиме реального времени с использованием реакционной смеси БиоМастер HS-qPCR SYBR Blue (2×) («БиолабМикс») на системе детекции CFX96™ (Bio-Rad Laboratories, США). Малую ядрышковую РНК U68 использовали для нормализации данных. Каждую реакцию ПЦР проводили с использованием 0,3 мкл кДНК в конечном объеме 25 мкл при следующих условиях: начальная денатурация при 95°С в течение 5 мин, затем 40 циклов: денатурация при 95°С в течение 15 с, отжиг при 60°С в течение 20 с, элонгация и обработка данных флуоресценции при 72°С в течение 30 с. Специфичность ПЦР контролировали кривыми плавления. Относительные уровни экспрессии микроРНК оценивали, используя значения порогового цикла (Ct) с учетом эффективности реакции (E) для исследуемого гена и гена нормировки.
Для ПЦР использовали специфические олигонуклеотиды со следующими последовательностями праймеров:
1. U68
· прямой праймер 5’- GGGCTGTACTGACTTGATGAAAG - 3’
· обратный праймер 5’-AGTGСАGGGТССGAGGTA-3’
2. miR-9-3р
· прямой праймер 5’- TGCCAGATAAAGCTAGATAAC - 3’
· обратный праймер 5’-AGТGСАGGGТССGAGGТА-3’
3. miR-132-3р
· прямой праймер 5’- GCCGTAACAGTCTACAGCC - 3’
· обратный праймер 5’-AGТGСАGGGТССGAGGТА-3’
Для статистической обработки результатов и их графической интерпретации использовали программу OriginPro 9.
Оценку достоверности различий средних значений параметров проводили с использованием t-критерия Стьюдента с поправкой Бонферрони. Различия между группами считались значимыми при p<0,05. Данные представлены в виде арифметического среднего и стандартной ошибки среднего (M±SEM). При нормировке результатов за единицу принимали образцы контрольной группы для каждого из отделов гиппокампа.
Результаты исследования и их обсуждение
В результате поставленного эксперимента от мышей двух групп, в каждой из которой было по 6 животных, было получено 12 образцов гиппокампа. При извлечении гиппокамп подразделяли на 4 части в соответствии с двумя типами асимметрии: LD – левый дорзальный, LV – левый вентральный, RD – правый дорзальный, RV – правый вентральный. Таким образом, общее число образцов гиппокампа для последующего молекулярного анализа составило 24 образца.
У мышей группы 1, которым вводили физиологический раствор, не обнаружено различий в уровнях экспрессии как miR-9-3р, так и miR-132-3р между отделами гиппокампа, то есть отсутствовала асимметрия. Полученные данные представлены на рисунке 1.
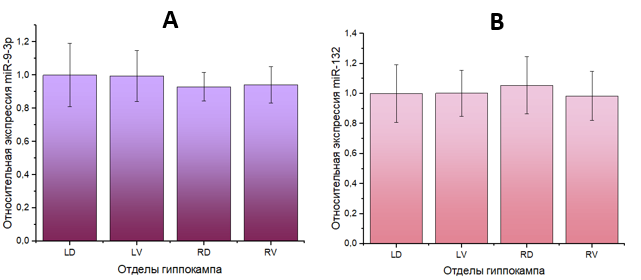
Рис. 1. Уровень экспрессии микроРНК в гиппокампе контрольных мышей: A – miR-9-3p, B – miR-132-3р. Отделы гиппокампа: LD – левый дорзальный, LV – левый вентральный, RD – правый дорзальный, RV – правый вентральный. За единицу по оси ординат приняты значения образцов LD
У мышей группы 2 со сформированной хронической зависимостью от морфина показано статистически значимое снижение экспрессии miR-9-3p во всех отделах гиппокампа, за исключением левого вентрального, однако нужно отметить, что в этом отделе тоже присутствует тенденция к снижению экспрессии (рис. 2А).
Выявлена асимметрия по дорзовентральной оси, поскольку снижение экспрессии miR-9-3p более выражено в дорзальных отделах гиппокампа.
Не обнаружено статистически достоверных различий в изменении экспрессии miR-9-3p между правым и левым гиппокампами.
Для miR-132-3р в тех же условиях не было установлено каких-либо статистически значимых изменений в уровне экспрессии (рис. 2В).
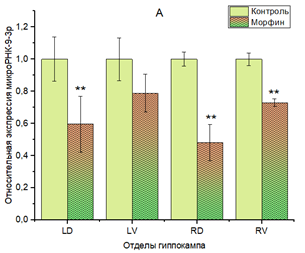
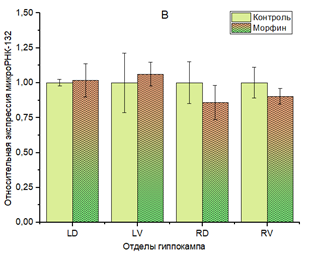
Рис. 2. Относительная экспрессия miR-9-3р (A) и miR-132-3р (B) в гиппокампе мышей линии C57Bl/6 при хронической зависимости от морфина.
** p<0,01. Отделы гиппокампа: LD – левый дорзальный, LV – левый вентральный, RD – правый дорзальный, RV – правый вентральный. В каждом из отделов гиппокампа за единицу приняты образцы контрольной группы
Выбор микроРНК miR-9-3р и miR-132-3p для анализа их экспрессии в гиппокампе был обусловлен тем, что обе они вовлечены в ряд важных процессов на уровне нервной системы. Так, miR-9-3p в гиппокампе контролирует направление роста дендритов, участвует в ветвлении аксонов при формировании нейронных сетей [5] и принимает участие в регуляции синаптической пластичности [13]. Показана роль miR-132-3p в процессах дифференцировки и миграции нейробластов, в регуляции созревания дендритов и аксонов [14]; так же как и miR-9-3p, miR-132-3p участвует в регуляции синаптической пластичности [6]. Развитие хронической зависимости от морфина приводит к достоверному снижению экспрессии miR-9-3р в дорзальных отделах левого и правого гиппокампа, а также в правом вентральном отделе, при этом в левом вентральном отделе имеется выраженная тенденция к снижению экспрессии. В исследовании S.E. Sim и соавторов в 2016 г. [13] было показано, что ингибирование экспрессии miR-9-3p приводило к нарушению формирования долговременной потенциации в области CA1 дорзального гиппокампа без влияния на базовые параметры синаптической передачи, при этом повышалась активность генов Dmd и SAP97, отрицательно коррелирующих с возможностью развития долговременной потенциации: у мышей со сниженной экспрессией Dmd наблюдалась фасилитация долговременной потенциации, в то время как при гиперэкспрессии гена SAP97 развитие долговременной потенциации нарушалось. При этом было отмечено, что подавление экспрессии miR-9-3p у животных приводило к ухудшению памяти и способности к обучению. Это позволяет предположить, что обнаруженное снижение экспрессии микроРНК-9-3p при длительном воздействии морфина является одним из механизмов нарушения синаптической пластичности гиппокампа и снижения когнитивных способностей и памяти при формировании хронической опиоидной зависимости.
Если у мышей группы 1 не выявлено асимметрии в экспрессии miR-9-3р, то у животных с хронической зависимостью от морфина обнаружена дорзовентральная асимметрия, что может свидетельствовать о более глубоких нарушениях пластичности в дорзальном гиппокампе, связанном с рабочей и оперативной памятью. В то же время отсутствуют достоверные различия в уровнях экспрессии miR-9-3р между отделами правого и левого гиппокампа. Это может объясняться тем, что miR-9-3р не участвует в регуляции генов, активность которых связана с латерализацией функций этой структуры мозга. В качестве примера можно привести ген, кодирующий N2B-субъединицу (ε-субъединицу) рецептора глутамата NMDA-типа (рецептор, агонистом которого является N-метил-D-аспартат), экспрессия которого начинается еще в раннем эмбриогенезе и с неравномерным распределением которых связывают этот вариант асимметрии в гиппокампе мышей [15]. В этой же работе было показано, что подавление экспрессии miR-9-3p не влияет на функционирование NMDA-рецепторов.
В представленной работе не было выявлено статистически значимых изменений в уровне экспрессии miR-132-3р у мышей с хронической зависимостью от морфина (рис. 2В), хотя в экспериментах M. Jia и соавторов, проведенных в 2022 г., было обнаружено увеличение экспрессии miR-132-3р в зубчатой фасции у крыс с хронической зависимостью от морфина, за счет чего изменялись показатели структурной нейропластичности [16]. Возможно, что отличия в результатах объясняются разными протоколами получения животных с хронической зависимостью, разным временем забора материала для анализа и, наконец, тем, что экспрессию микроРНК в исследовании [16] изучали только в образцах дорзальной зубчатой фасции, а не в целом дорзальном отделе гиппокампа.
В работах, посвященных изучению участия miR-132-3р в синаптической пластичности, указывается на то, что изменения экспрессии этой микроРНК являются транзиторными и быстро возвращаются к исходному состоянию, а полученные различными методами длительная гиперэкспрессия или, наоборот, подавление экспрессии miR-132-3p приводят к нарушению синаптической пластичности [6, 14]. Поэтому для выяснения вовлеченности miR-132-3р в развитие хронической опиоидной зависимости и вызванное опиоидами нарушение синаптической пластичности необходимы дальнейшие исследования.
Заключение
Таким образом, показано, что у контрольной группы мышей C57BL/6 уровень экспрессии miR-9-3p и miR-132-3р статистически значимо не отличается между отделами гиппокампа, то есть отсутствует дорзовентральная и межполушарная асимметрия. У животных с хронической зависимостью от морфина обнаружено достоверное снижение экспрессии miR-9-3p в трех отделах гиппокампа, за исключением левого вентрального, где все же имеется тенденция к снижению экспрессии. Выявлена дорзовентальная асимметрия экспрессии miR-9-3p в гиппокампе хронически от морфина зависимых мышей. Поскольку miR-9-3p участвует в регуляции синаптической пластичности, высказано предположение о том, что снижение экспрессии этой микроРНК при длительном воздействии морфина может являться одним из механизмов нарушения синаптической пластичности при хронической опиоидной зависимости. Изменений экспрессии miR-132-3р в отделах гиппокампа мышей с хронической зависимостью от морфина не было выявлено, вопрос об участии этой микроРНК в механизмах развития зависимости от опиоидов требует дальнейшего изучения.
Библиографическая ссылка
Леваневская В.А., Конончук В.В., Сорокина Н.С., Валембахов И.С., Старостина М.В. ЭКСПРЕССИЯ МИКРОРНК MIR-9-3P И MIR-132-3Р В ГИППОКАМПЕ МЫШЕЙ ЛИНИИ C57BL/6 В НОРМЕ И ПРИ ХРОНИЧЕСКОЙ ЗАВИСИМОСТИ ОТ МОРФИНА // Современные проблемы науки и образования. 2024. № 6. ;URL: https://science-education.ru/ru/article/view?id=33870 (дата обращения: 10.05.2026).
DOI: https://doi.org/10.17513/spno.33870



